Os interferentes na fase pré-analítica e analítica na qualidade do exame citológico
Interferences in the pre-analytical and analytical phase as part of the cytological examination
Aliny Morgana Ribeiro1, Elaine Araújo Lima1, Carmem Damasceno Balacol1
1 Citopatologia Clínica com Ênfase no Trato Genital Feminino. Belém, PA, Brasil.
Recebido em 12/07/2020
Aprovado em 08/03/2022
DOI: 10.21877/2448-3877.202202038
INTRODUÇÃO
Câncer é o termo dado a doenças de malignidade que têm em comum o crescimento desordenado de células que podem invadir tecidos adjacentes ou órgãos. As rápidas divisões celulares passam a ser incontroláveis e agressivas, passíveis de alterações celulares que podem evoluir para tumores cancerígenos que têm a possibilidade de se espalhar para outras partes do corpo.(1)
O câncer de colo do útero se desenvolve na parte inferior do útero, denominada colo, e está associado à infecção pelo vírus HPV (papilomavírus humano), em especial por subtipos oncogênicos como HPV-16 e o HPV-18. Seu desenvolvimento propaga-se por um período de 15 a 20 anos, no qual 70% dos casos estão relacionados com a infecção pelo HPV e sua progressão para a lesão precursora, até que se desenvolva o câncer invasor.(2)
O câncer de colo do útero é um problema de saúde pública, sendo o quarto tipo de tumor mais recorrente entre as mulheres, com mais de 500.000 novos casos e 250.000 mortes ao ano. No Brasil, é o terceiro tipo de câncer mais incidente no público feminino e a estimativa para o ano de 2022, segundo o INCA, é de 17.010 novos casos. As infecções prevalecem mais no início da atividade sexual em adolescentes e jovens adultas.(3)
Além de ser relacionado à própria infecção pelo HPV, há cofatores que favorecem a infecção e o desenvolvimento para o câncer de colo, como: infecções persistentes por HPV de alto risco, imunidade, genética, tabagismo, hábitos de higiene, má alimentação, comportamento sexual, início da atividade sexual precoce, número de parceiros ou único promíscuo. Para além disso, influenciam também os fatores socioeconômico.(4)
Para prevenir e rastrear o câncer de colo do útero, é realizado o exame de Papanicolaou. De acordo com as diretrizes brasileiras para o rastreamento do câncer do colo do útero (Ministério da Saúde), o público-alvo do referido exame são mulheres a partir dos 25 anos de idade, que já iniciaram atividades sexuais, as quais devem seguir realizando o exame até os 64 anos. Nas mulheres sem nenhum histórico de doenças pré-neoplásicas, só deve ser interrompida a realização do exame quando dois resultados forem negativos nos últimos cinco anos.(5)
O exame preventivo do câncer de colo do útero (PCCU), também chamado de Papanicolaou, é um exame periódico, seguro, eficaz, de baixo custo e de fácil execução. Este diagnóstico citopatológico pode classificar as lesões precursoras, como as intraepiteliais escamosas de alto grau (HSIL) e adenocarcinoma in situ (AIS), que são provocadas pela infecção persistente pelos tipos de HPV de alto risco oncogênico, como também as lesões intraepiteliais escamosas de baixo grau (LSIL), que são provocadas pela infecção pelos tipos de HPV de baixo risco oncogênico. Assim, é um exame citológico que, junto com o tratamento adequado, nos estágios iniciais, pode resultar em uma redução das taxas de evolução de câncer de colo do útero.(6)
Ao preparar a lâmina do preventivo, a amostra é considerada adequada e satisfatória quando possui células escamosas, glandulares e/ou metaplásicas, além de bem distribuídas, fixadas e coradas, que permitam uma conclusão diagnóstica. A análise de uma amostra satisfatória é um indicador de qualidade fundamental.
Há algum tempo que o exame Papanicolaou vem sofrendo algumas críticas, em virtude da sua baixa sensibilidade. As taxas dos falsos negativos variam entre 6% a 56%, que podem ocorrer nas fases pré-analítica e analítica. Para além disso, existe a possibilidade dos falsos negativos ocorrerem em razão de problemas da hora da coleta, falta do uso de fixador, erros no procedimento de coloração, no escrutínio, interpretação e análises.(6)
REFERENCIAL TEÓRICO
O câncer de colo do útero, quando diagnosticado no início da doença, pode chegar a 100% de chance de cura, se houver um diagnóstico realizado com qualidade. Para que o exame citopatológico seja feito corretamente e com segurança há vários processos que devem ser realizados na fase pré-analítica, como: a correta identificação do material, apresentação dos epitélios na lâmina, fixação, coloração, transporte das amostras, capacitação dos profissionais e controle de qualidade, para que a qualidade do exame não seja comprometida.(7)
Capacitação da enfermagem
Quando, por algum motivo, há um problema na realização do exame na fase pré-analítica, perde-se a sensibilidade e especificidade do PCCU. A partir disso, é muito importante ter atenção na qualidade da obtenção do material cervical para que a coleta das amostras citopatológicas seja realizada por profissionais qualificados. De acordo com a Resolução do Conselho Federal de Enfermagem (COFEN) n° 385/2011, a coleta de material para o exame de PCCU deve ser realizada, unicamente, por enfermeiros, visto ser um procedimento que requer a capacitação inerente a estes profissionais, devido ao conhecimento técnico, científico e socioeconômico do câncer de colo do útero.(3)
Assim, o enfermeiro é capacitado para atuar nas diferentes atividades de controle do câncer de colo do útero, principalmente no ato de acolher e sensibilizar a paciente desde o primeiro contato até o diagnóstico, além da atenção básica e da realização da coleta do exame.(3)
A atenção básica à saúde é a entrada da paciente no sistema de saúde, no qual o enfermeiro é uma parte fundamental do grupo multiprofissional da Estratégia Saúde da Família (ESF). Este profissional tem responsabilidade na aplicação de métodos educativos e de ações por meio da relação com as pacientes, no objetivo de tirar dúvidas, medos e repassar conhecimentos sobre a relevância da prevenção ao fazer o exame. Cria-se, portanto, uma relação entre paciente e enfermeiro para promover esclarecimento, confiança, proteção e tranquilidade durante o atendimento.(8)
Coleta do material citopatológico
Antecedendo a coleta do material (Figura 1), há o preenchimento do formulário com os dados de identificação, que deve ser feito corretamente, com o nome completo, data de nascimento, endereço, período menstrual e alguns dados e exames clínicos da paciente. Quando não há obtenção dos dados corretos, pode haver interferência na interpretação do exame, dificultando a localização futura da paciente que venha a apresentar alguma alteração em seu exame.(9)
Fundamental que o rastreio das lesões no colo do útero, na fase pré-analítica, seja desenvolvido de forma adequada, impedindo eventuais falsos negativos, com a necessidade de uma apresentação de células devidamente distribuídas, fixadas e coradas.(10) Ademais, é durante o procedimento da coleta que podem ocorrer erros que mais prejudicam a análise do exame, visto que é uma fase essencial e que necessita de execução com eficácia, pois as falhas podem ser responsáveis por até 62% dos resultados falsos negativos, em razão da falta de representatividade celular, escassez de células malignas e processos inflamatórios, que acabam prejudicando o exame. Um esfregaço é considerado satisfatório quando há representação das células da ectocérvice, do canal endocervical e/ou da zona de transformação analisados corretamente.(11)
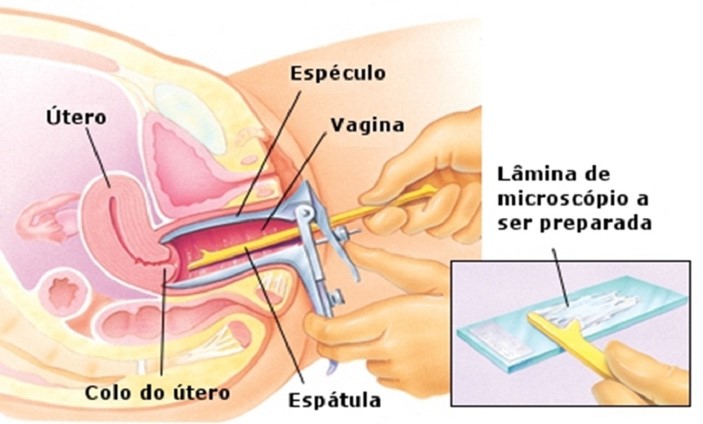
Figura 1
Representação esquemática da coleta na citologia, método convencional.(12)
Fixação das lâminas
O profissional responsável pela coleta do material cervicovaginal é encarregado, também, por realizar uma adequada fixação da amostra, que deve ser feita após a coleta de forma correta e rápida, com o objetivo de preservação da morfologia das células e conservação dos detalhes, prevenindo a deformação celular, a perda da afinidade das células pelos corantes e aparecimento de artefatos.(13) Silva e Assis(9) relatam que os métodos de fixação citopatológicos podem dar-se de três maneiras: fixação úmida, fixação úmida por secagem ao ar e fixação por nebulização.
A fixação úmida ocorre de maneira que as lâminas ficam imersas em álcool a 96%. A principal vantagem é a velocidade de difusão e preservação das estruturas e a desvantagem é que pode ocorrer a retração citoplasmática, com a perda de atividade. Na fixação úmida, com secagem ao ar, os esfregaços são imersos em álcool por, no mínimo, 30 minutos, sendo transportada somente a lâmina para facilitar. A desvantagem é o fato de a lâmina secar na temperatura do ambiente, o que poderá acarretar a perda das características cromáticas, por formação de edema nuclear, ocorrendo, também, coloração limitada.(9)
A fixação por nebulização, entretanto, é realizada por fixadores em spray, contendo polietilenoglicol, que forma uma película de proteção das células. Ademais, utiliza-se, também, o álcool 96%, a uma distância de 15cm a 25cm sobre os esfregaços. A desvantagem deste método é o risco de o spray ser utilizado muito próximo da lâmina, podendo eliminar ou lesar as células ou provocar a formação de artefatos.(9)
Observa-se um maior percentual de dessecamento nas células, resultante da falta de capacitação dos profissionais coletadores, com uma diminuição significativa após a capacitação dos mesmos. Assim, mostra-se essencial que haja a orientação acerca da fixação imediata do material na lâmina, evitando o dessecamento.(10)
Transporte e recebimento das lâminas
As unidades que enviam suas amostras para serem examinadas devem garantir o meio de transporte adequado, ou seja, cada tipo de fixador utilizará um meio de transporte para que possa garantir a adequabilidade das amostras. Para lâminas fixadas com fixador de cobertura, utilizam-se caixas de papelão, madeira ou plástico; para os fixadores com álcool utilizam-se tubetes com tampa de rosca e as lâminas devem ser enviadas em recipientes individualizados. Desaconselha-se, ainda, o compartilhamento de recipientes, mesmo que as amostras sejam separadas por clipes.(13)
Precedendo o início da fase pré-analítica, ressalta-se o recebimento dos esfregaços citopatológicos na recepção do laboratório responsável pela análise a ser procedida. Nesse momento, é confirmado se a amostra está corretamente identificada dentro dos critérios de aceitação. Esta confirmação é fundamental para que não haja o comprometimento da qualidade do exame.(13)
Coloração das lâminas
Em alguns casos em que não há uma coloração com qualidade, há a liberação de resultados falsos negativos, resultante da não identificação de células atípicas durante a análise do material. De acordo com o controle de qualidade do INCA, as lâminas com material cervicovaginal fixadas em álcool são, diretamente, coradas. Aquelas com fixadores em spray, antes de serem coradas, devem ser lavadas em álcool 96%, pelo menos em duas cubas, no mínimo, durante 15 minutos cada, podendo ficar por mais tempo, sem prejudicar a coloração, processo importante para que a película de cobertura seja eliminada, pois inibe a infiltração dos corantes nucleares e citoplasmáticos.
O corante universalmente utilizado é o de Papanicolaou. Uma técnica de coloração multicromática criada por Geórgios Papanicolaou. Ela utiliza três corantes: a hematoxilina de Gill (substituída também pela hematoxilina de Harris), OG-6 e EA-36 ou EA-65. Ainda não há certeza de como acontece o processo pelo qual as células são coradas, mas acredita-se que há duas suposições: a adsorção e as características de compatibilidade química na coloração.
Nas duas hipóteses, a concentração do corante nas soluções e a forma iônica são importantes. Acredita-se que as estruturas celulares de pH ácidos visam atrair corantes de radical catiônico, tanto pelo fenômeno absorção como por fatores químicos. Já as básicas tendem com os corantes de radical aniônico.(14)
O citoplasma celular é constituído por componentes ácidos e básicos e nos núcleos das células prevalecem os ácidos nucleicos. O primeiro corante a ser utilizado é a hematoxilina, responsável pela coloração azulada dos núcleos, reagindo com os ácidos nucleicos. Posteriormente, as lâminas são coradas pelo Orange G (OG-6), um corante ácido que possui afinidade com o componente básico do citoplasma.
Por último, é a solução EA-36 ou EA-65, que são colorações semelhantes, possuindo como diferença a concentração do corante Light Green. A solução EA-36 possui 50% a mais do corante. Estes, por sua vez, são corantes ácidos, que se fixam nos componentes básicos do citoplasma.
Além do Light Green, há um segundo corante que faz parte das soluções EA-36 e EA-65, que é a eosina amarelada, tendo como função a coloração de grânulos do citoplasma, com afinidade por corantes ácidos.(14) Deve-se manter uma rotina de monitoramento diário dos corantes, que devem ser filtrados e trocados regularmente, para evitar contaminações cruzadas. Para além disso, deve-se observar os rótulos com informações sobre armazenamento e datas de vencimento, pois o álcool também entra na rotina de monitoramento, sendo analisada a sua concentração através de um alcoômetro.(13)
Método citopatológico cervicovaginal convencional
A citologia cervicovaginal foi introduzida por Geórgios Papanicolaou e Aureli Babes no ano de 1928. Porém, a partir de 1943, com a ajuda de Herbert Traut, o método passou a ser amplamente utilizado, por ser rápido, indolor e fácil de executar. Ele permite que haja um acompanhamento da inflamação, o diagnóstico de algumas infecções cervicovaginais e, ainda, o rastreamento do câncer de colo do útero e de lesões precursoras.(15)
No exame convencional há algumas restrições, como a distribuição não homogênea das células na lâmina, o baixo número de células e a presença de fundo hemorrágico, leucócitos e restos celulares que prejudicam a análise. Em razão destas restrições foi elaborado o método de coleta em meio líquido, com objetivo de reduzir as falhas do método convencional.(16)
A citologia de base líquida foi aprovada, em 1996, pelo food and drug administration (FDA) dos Estados Unidos, para o uso em ginecologia e outras especialidades. Ela foi desenvolvida para obtenção de uma lâmina com fundo mais limpo, sem sobreposição de células e obscurecimento de outros elementos, o que se deve ao sistema de filtros, no qual apenas células epiteliais ficam retidas, resultando em uma citologia em monocamada ou em camada fina.(15)
Com o mesmo material é possível refazer lâminas e realizar testes moleculares e identificação de HPV, além de permitir a escolha das células que vão ser transferidas para a lâmina, possibilitando que todo o material seja analisado e evitando perdas celulares.(16)
Quanto aos métodos existem vantagens e desvantagens. A citologia convencional tem como vantagem a confortável execução, menor custo e a possibilidade de corar o material assim que é recebido no laboratório. Sua desvantagem é a perda de, aproximadamente, 80% do material coletado, por continuar na escova cervical, além da má distribuição celular, a possibilidade de falso negativo e o esfregaço com material insuficiente.(15) (Figuras 2 e 3)
A citologia em meio líquido tem como vantagem a preservação e disposição celular, a facilidade de fechar um diagnóstico com redução de tempo de leitura, eliminação de muco, hemácias e leucócitos, redução de amostras insatisfatórias e de casos falsos negativos, além da possibilidade de fazer exames adicionais. Como desvantagem, indica-se a necessidade de treinamento para o profissional sobre a técnica, além da necessidade de aparelhos específicos, elevado custo para a execução e a sobrecarga de trabalho da equipe.(15) (Figuras 2 e 3)
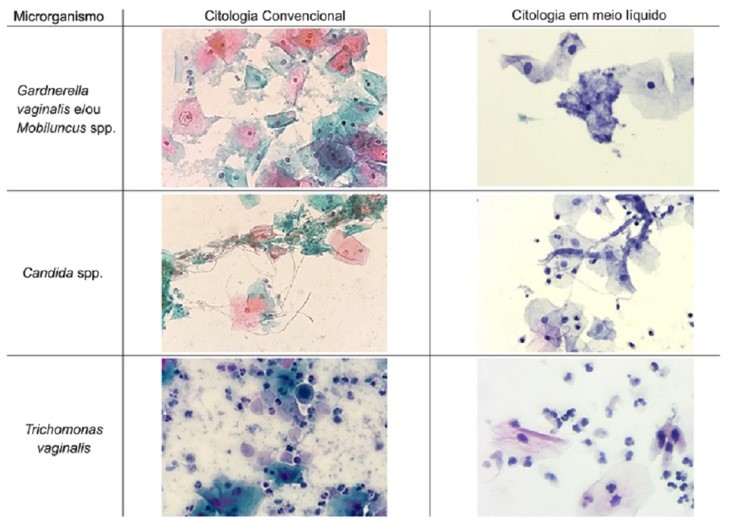
Figura 2
Imagem representativa de comparação entre os métodos.(16)
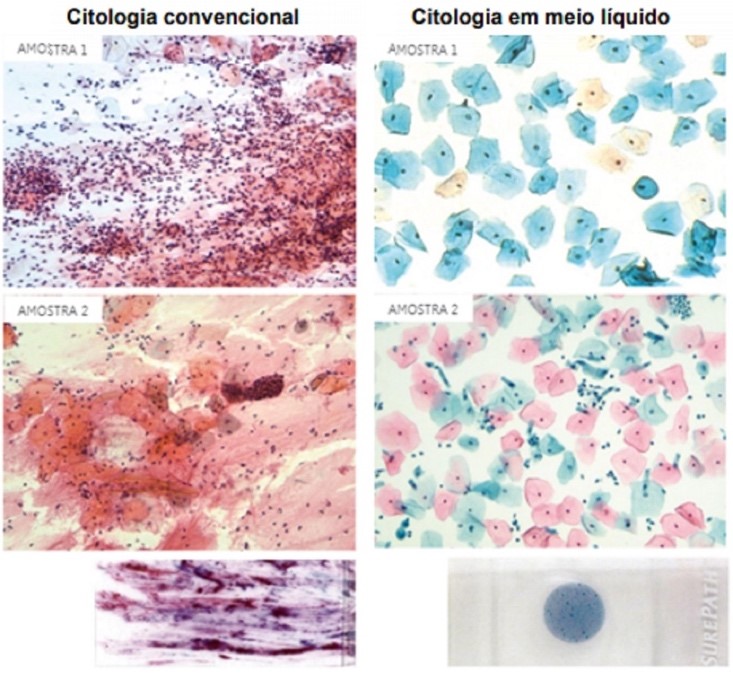
Figura 3
Imagem de Comparação entre os dois métodos.(17)
Controle de qualidade
A Organização Mundial da Saúde (OMS) orienta que o PCCU seja realizado de forma efetiva. Contudo, diante da baixa sensibilidade, vem sofrendo críticas, principalmente em razão de sua taxa de falso negativo, na fase pré-analítica e analítica, variar entre 6% a 56%. De acordo com RDC nº 302, de 13 de outubro de 2005, laboratórios de análises clínicas devem implantar programas de controle de qualidade interno e externo, para impedir erros e reduzir falsos negativos.(6) Além disso, tem como finalidade a identificação, diminuição e correção dos erros no desenvolvimento do exame dentro do laboratório, possuindo mais garantia de qualidade e credibilidade, reduzindo os erros de diagnóstico e ajudando a melhorar a fase pré-analítica e analítica.(7)
A Qualificação Nacional em Citologia (QualiCito) é a ferramenta de avaliação recomendada pela Portaria nº 3.388, de 30 de dezembro de 2013, que se baseia em determinar padrões e avaliar a qualidade do PCCU, acompanhando o trabalho dos profissionais dos laboratórios públicos e privados.(6) O Monitoramento Interno de Qualidade (MIQ) ocorre por intermédio de processos feitos com regularidade, para monitorar a qualidade da amostra, verificar o tempo da análise da lâmina, da carga horária do profissional que faz a análise e as técnicas de revisão de lâmina.(18)
A revisão aleatória de 10% dos esfregaços negativos é a mais utilizada, porém não é eficaz para identificar lesões não diagnosticadas da rotina. Indicada como técnica padrão, a revisão de 100% dos esfregaços, por ser mais cuidadosa, reduz erros da rotina. Além disso, há a revisão rápida de 100% dos esfregaços negativos ou insatisfatórios e esfregaços duvidosos, que depois passaram por outra revisão detalhada por profissional experiente para fechar o diagnóstico.
A técnica de pré-escrutínio rápido de todos os esfregaços tem o objetivo de elevar a sensibilidade do exame, por realizar de forma ágil a leitura de todos os esfregaços em até 120 segundos antes da rotina, provocando uma maior quantidade de falsos positivos, por ser enviado para a revisão detalhada um maior número de esfregaços duvidosos. Entretanto, esta técnica ainda demonstra eficácia para redução de resultados falsos negativos.(18)
O Monitoramento Externo de Qualidade (MED) corresponde à revisão dos esfregaços por outro laboratório, diferente do que realizou a primeira leitura. Tem como objetivo avaliar laboratórios tipo I, por outro laboratório do tipo II e mensurar a qualidade dos exames de PCCU realizados por eles, identificar a desigualdade de interpretação de morfologia das células, elevar a eficácia dos exames citopatológicos do colo do útero e diminuir a quantidade de exames falso negativos, falsos positivos e insatisfatórios.(13)
As lâminas enviadas para o MEQ serão escolhidas pela Secretaria de Estado da Saúde (SISCAN) ou por algum outro sistema de informação repassado pelo Ministério da Saúde. Os critérios de lâminaa a serem enviadas são: todas as lâminas com resultados positivos; todas as lâminas insatisfatórias e, de forma aleatória, 10% dos exames com diagnósticos dados como negativos, selecionados pelo número final do exame. Caso haja uma discordância do laboratório tipo II no diagnóstico do esfregaço enviado, deve-se chegar a um consenso entre este laboratório e o laboratório tipo I, antes da liberação do laudo no sistema de informação, e quando não houver consenso entre os laboratórios (tipos I e II), há a possibilidade de solicitar a análise de outro laboratório tipo II.(13)
OBJETIVOS
Objetivo Geral
Apontar possíveis falhas na fase pré-analítica do exame de Papanicolaou.
Objetivos Específicos
Diminuir casos de rejeição da amostra;
Evitar resultados falsos positivos e/ou falsos negativos;
Chamar atenção para o controle de qualidade na coleta da amostra de PCCU.
MATERIAL E MÉTODOS
O trabalho foi realizado com base em revisão bibliográfica, resultando em uma pesquisa de caráter descritivo, com análise qualitativa. Para obter conhecimento foram incluídos na revisão: artigos, manuais e sites que abordam sobre a qualidade do exame citopatológico, desde a confecção da amostra até a fase de coloração e de montagem das lâminas.
Para a realização desta pesquisa foram utilizados artigos científicos das seguintes plataformas: Instituto Nacional do Câncer (INCA), LILACS, SciELO, PubMed, Google acadêmico, além de livros e revistas cientificas. A bibliografia levantada foi um total de 20 artigos, dos quais 14 foram utilizados para a produção deste trabalho, em que todos foram publicados no período de 2018 a 2020.
DISCUSSÃO
O câncer de colo do útero é o terceiro mais frequente nas mulheres brasileiras, sendo um dos principais problemas de saúde pública. Em razão disso foram elaboradas estratégias para reduzir a sua incidência, através de um programa de rastreamento. Contudo, para obter eficácia é fundamental que seja realizado corretamente desde a fase pré-analítica.
Jakobczynski et al.(10), em seus estudos, comprovam que após os profissionais passarem por devida capacitação houve um aumento nas amostras satisfatórias e da representatividade da JEC, evidenciando que coletas não adequadas podem resultar em laudos falsos negativos. Aoyama et al.(8) relatam a importância do papel da enfermagem na prevenção do câncer de colo do útero, tendo como primeiro contato a atenção básica primária seguida do ingresso da paciente no sistema de saúde, e posterior acompanhamento da mesma.
Oliveira et al.(3) abordam que, de acordo com a Resolução do Conselho Federal de Enfermagem (COFEN) n° 385/2011, somente enfermeiros podem realizar a coleta do exame, visto a necessidade de uma conduta técnica científica. Porém os estudos relatam as contradições da resolução, visto que não leva em consideração particularidades de cada região e nem as estruturas do sistema de saúde de todo o território nacional.
Assim, o INCA é levado a alertar sobre as possíveis consequências e considerar que a coleta poderia ser realizada por técnicos e auxiliares de enfermagem, desde que passem por uma capacitação. Entretanto, permanece em vigor a resolução aos profissionais da enfermagem.
De acordo com o manual produzido pelo Ministério da Saúde(13), o método mais utilizado para o rastreamento das lesões precursoras de câncer de colo do útero é o teste de Papanicolaou. Além disso, para garantir a qualidade do exame, é realizado um controle de qualidade para detectar, corrigir, minimizar erros e aperfeiçoar o teste, como também para melhorar a coleta e o preparo do escrutínio.
Segundo Santos e Ribeiro(6), o preventivo possui falhas nos diagnósticos, como resultados falsos, devido a sua baixa sensibilidade. Por isso, é necessário que sejam implementados programas de controle de qualidade. Magalhães et al.(7) afirmam que, com o controle, o teste de Papanicolaou passa a ter mais garantia, credibilidade e melhoria nas fases pré-analitica e analítica.
Machado et al.(18) mencionam que, em razão da recorrência elevada de resultados falsos negativos, é necessária a implantação do controle interno de qualidade, no qual o mais eficiente é a revisão de 100% dos esfregaços negativos, sendo possível alcançar maior quantidade de lâmina.
Conforme Flora e Colturato,(15) a citologia por meio líquido foi criada, em razão de a técnica da citologia convencional (Papanicolaou) ter limitações. Com isso, mostrou-se necessária a procura de um método com mais sensibilidade, baixo número de resultados falsos negativos, melhor método de coleta e preparo da amostra. Em estudos comparativos, a citologia por meio líquido possui maior sensibilidade e menor especificidade que a citologia convencional, entretanto Silva et al.(16) mencionam a qualidade da citologia em meio líquido e as falhas do método convencional, evidenciando que tem um melhor desempenho para a identificação de Trichomonas vaginalis.
CONCLUSÃO
Este estudo evidencia a necessidade de capacitação e qualificação dos profissionais responsáveis pela coleta de material, com a finalidade de aprimorar e garantir a qualidade das amostras, sendo o enfermeiro o profissional capacitado para desenvolver o procedimento da coleta. Além de tornar os profissionais capacitados, é essencial que eles passem por uma atualização, que pode acontecer a cada dois, três anos ou quando o Ministério da Saúde e o INCA atualizarem seus manuais ou a diretriz para a realização do PCCU.
Quanto à relevância da implantação de um programa de controle de qualidade em Citopatologia, os indicadores de controle de qualidade devem ser adotados e avaliados por todos do laboratório, procurando minimizar erros e os resultados falsos.
REFERÊNCIAS
- Brasil. Ministério da saúde. Instituto Nacional do Câncer (INCA). O que é câncer?, 2020. Disponível em: <https://www.inca.gov.br/o-que-e-cancer> Acesso em: 10 de agosto 2021.
- _______. Ministério da saúde. Instituto Nacional do Câncer (INCA). Câncer do colo do útero – versão para Profissionais de Saúde, 2021. Disponível em: <https://www.inca.gov.br/tipos-de-cancer/cancer-do-colo-do-utero/profissional-de-saude>. Acesso em: 10 de agosto 2021.
- Oliveira LL, et al. Exclusividade na coleta de material para exame de colpocitologia oncótica: percepção dos enfermeiros. Revista Enfermagem da UFSM. V.10, p. 1-17, 2020. Disponível em: <https://periodicos.ufsm.br/reufsm/article/view/33721/html>. Acesso em: 05 de agosto 2021.
- Siqueira LC, Oliveira RF dos S. A importância do enfermeiro na concientização e prevenção do HPV. Psicologia e Saúde em debate, [S. l.], v. 5, n. 1, p. 80–109, 2019. Disponível em: <http://psicodebate.dpgpsifpm.com.br/index.php/periodico/article/view/V5N1A8>. Acesso em: 20 de agosto 2021.
- Oliveira AK, et al. Infecção pelo HPV – Rastreamento, diagnóstico e conduta nas lesões HPV-induzidas. Revista Feminina, n. 3, v. 49, p.166-172, 2021. Disponível em: <https://docs.bvsalud.org/biblioref/2021/05/1224082/femina-2021-493-p166-172-infeccao-pelo-hpv-rastreamento-diagno_yCxEoCJ.pdf > Acesso em: 16 de agosto 2021.
- Santos MJS, Ribeiro AA. Estratégias Utilizadas para Melhorar a Qualidade dos Exames Citopatológicos. Revista Brasileira de Cancerologia, v. 66, n. 1, p. e- 05104, 16 mar. 2020. Disponível em: <https://rbc.inca.gov.br/revista/index.php/revista/article/view/104 > Acesso em: 20 de agosto 2021.
- Magalhães JC, et al. Avaliação dos indicadores de qualidade dos exames citopatológicos do colo do útero realizados em um município do Paraná, Brasil. Jornal Brasileiro de Patologia e Medicina Laboratorial. v. 56, p. 1-7, 2020. Disponível em: <https://doi.org/10.5935/1676- 2444.20200041>. Acesso em: 10 de agosto 2021.
- Aoyama EA, et al. Assistência de enfermagem na prevenção do câncer de colo do útero. Brazilian Journal of Health Review. v.2, n.1, p.162-170, 2018.
- Silva IC da, Assis IB de. Os efeitos das incorreções pré-analíticas para o exame de Papanicolau. Revista Saúde em Foco, n. 11, p. 876-890, 2019. Disponível em: <https://portal.unisepe.com.br/unifia/wpcontent/uploads/sites/10001/2019/10/078_Osefeitosdasincorre%C3%A7%C3%B5espr%C3%A9-anal%C3%ADticas-para-o-exame-de-Papanicolau-Isabelle.pdf> Acesso em: 10 de agosto 2021.
- Jakobczynski J, et al. Capacitação dos profissionais de saúde e seu impacto no rastreamento de lesões precursoras do câncer de colo uterino. Rev. Brasileira de Análises Clínicas, v. 50, n. 1, p. 244-249, 2018. Disponível em: <http://www.rbac.org.br/artigos/capacitacao-dos-profissionais-de-saude-e-seu-impactonoastreamento-de-lesoes-precursoras-do-cancer-de-colo-uterino/> Acesso em: 02 de agosto 2021.
- Alves PBC. Método de coleta convencional para o diagnóstico do exame preventivo do câncer de colo do útero. 2019. 31 f. Trabalho de Conclusão de Curso (Especialização em Citologia Clínica) – Curso de Especialização em Citologia Clínica, Centro Universitário CESMAC, Maceió – AL, 2019.
- Miranda E. Exame citopatológico (papanicolau ou preventivo). Estratégia Saúde da Família. Disponível em: <https://estrategiasaudedafamilia.comunidades.net/exame-preventivo> Acesso em: 11de julho 2021.
- Brasil. Ministério da Saúde. Instituto Nacional do Câncer (INCA). Manual de Gestão da Qualidade para Laboratório de Citopatologia. 2 ed. Rio de Janeiro, 2016. Disponível em:<https://www.inca.gov.br/bvscontrolecancer/publicacoes/livro_completo_manual_citopatologia.p df> Acesso em: 12 de agosto 2021.
- Laborclin. 2018. Disponível em: <www.laborclin.com.br> Acesso em: 02 de julho 2021.
- Flora VMS, Colturato PL. Estudo comparativo entre citologia oncótica cérvico vaginal convencional e em meio líquido para rastreamento de câncer do útero e lesões precursoras, Revista Científica Eletrônica de Ciências Aplicadas da FAIT. n. 2, maio, 2020
- Silva RCG, et al. Desempenho da citologia em meio líquido na identificação de agentes microbiológicos cérvico-vaginais, Revista Brasileira de Análises Clínicas. v.50, n. 2, 2018. Disponível em: <http://www.rbac.org.br/artigos/desempenho-da-citologia-em-meio-liquido-na- identificacao-de-agentes-microbiologicos-cervico-vaginais/>. Acesso em: 12 de agosto 2021.
- Diagnósticos do Brasil. Citologia em Meio Líquido. Disponível em: <https://docplayer.com.br/6906239-Citologia-em-meio-liquido.html> Acesso em: 10 de julho 2021.
- Machado EP, et al. Controle interno da qualidade em citopatologia: o dilema da subjetividade. Rev. Brasileira de Análises Clínicas, v. 50, n. 3, p. 244-249, 2018. Disponível em: <http://www.rbac.org.br/artigos/controle-interno-de-qualidade-em-citopatologia-o-dilema-da- subjetividade/> Acesso em: 10 de agosto 2021.
Correspondência
Aliny Morgana Ribeiro
E-mail: [email protected]
