Micosis en tiempos de COVID-19
Mycosis in times of COVID-19
Luis Zaror1
Alexandra Aravena1
Alejandra Valenzuela1
1Escuela de Tecnología Médica, Facultad de Ciencias, Universidad Mayor, Temuco, Chile.
Recebido em 10/03/2021
Aprovado em 29/04/2021
DOI: 10.21877/2448-3877.202100965
INTRODUCCIÓN
En diciembre del 2019, un nuevo Coronavirus, denominado SARS-CoV-2 productor de la enfermedad COVID-19, se propagó en la ciudad de Wuhan, China, provocando una pandemia.(1) Este, forma parte de la familia de virus que producen el síndrome de distrés respiratorio agudo (SARS-CoV) y el Coronavirus del síndrome respiratorio de Oriente Medio (MERS-CoV).(2) Tiene 100-160 nanómetros de diámetro y está envuelto en una bicapa lipídica Presenta ARN de cadena positiva (Figura 1).(3) Los coronavirus, se dividen en cuatro géneros: α, β, ɣ y δ, siendo seis especies las que causan enfermedades en humanos; del género α: 229E y NL63 y del género β: OC43, HKU1, SARS-CoV y MERS-CoV.(4) El SARS-CoV-2 pertenece a la familia de los β – Coronavirus.(2)
En los pacientes infectados por SARS-CoV-2 encontramos diversos causantes de coinfecciones como virus, bacterias y hongos.(5) Dentro de las coinfecciones están las micosis, las cuales podrían ser graves y una de las causas directas de muerte en pacientes COVID-19. Los principales hongos que afectan a estos pacientes son especies de Aspergillus y Candida.(6) Las micosis aumentan la dificultad de diagnóstico, tratamiento y pronóstico, e incluso intensificarán los síntomas y mortalidad por la enfermedad.(5) Por ello, los médicos y microbiólogos deben centrarse en las coinfecciones, en los pacientes, con comorbilidades, inmunodeprimidos, especialmente en la fase intermedia y tardía, realizando vigilancia de patógenos fúngicos.(6)
Debido a las condiciones sanitarias actuales, es importante profundizar sobre las coinfecciones que podrían presentar, los pacientes con COVID-19 que desarrollan micosis, que es el objetivo de esta revisión bibliográfica sistemática.
Metodología
Se realizó, una revisión bibliográfica sistemática, en la base de datos “PubMed-NCBI”. Inicialmente, se utilizaron palabras claves: “COVID-19”, “SARS-CoV-2”, “Coronavirus”. Para la segunda búsqueda, se filtró la información con los siguientes encabezamientos: “COVID-19 and coinfection”, “Mycosis”, “Aspergillus spp.”, “Candida spp.” “COVID-19 and Aspergillus spp.”, “COVID-19 and Candida spp.”. En ambas búsquedas se utilizó como criterio temporal los años 2019 al 2021. Se limitó la búsqueda en relación con SARS-CoV-2, COVID-19 y micosis, seleccionando para esta revisión bibliográfica 75 artículos.
Resultados y Discusión
El brote mundial del virus SARS-CoV-2, descrito a partir del 2019, y que provocó la pandemia de COVID-19, ha originado un riesgo para la salud de las personas. La enfermedad presenta formas clínicas asintomáticas y sintomáticas, pudiendo generar un cuadro infeccioso potencialmente mortal, con distintos niveles de gravedad. Según la OMS, el virus se transmite principalmente a través de gotitas de saliva o secreciones nasales, predominantemente por la nariz, la boca o contacto con los ojos.(7) Además, se deben considerar las graves secuelas que deja en los sobrevivientes. Esto representa una amenaza a la vida y una crisis de salud pública internacional, debido a la propagación del virus por infectados, considerando la poca preparación planetaria ante esta emergencia.(8)
Este nuevo virus, presenta un genoma casi idéntico al coronavirus del murciélago de herradura, Rhinolophus affinis, del sur de China.(2) Se sospecha que el murciélago es el hospedador natural del virus y se puede transmitir desde éste, a través, de hospedadores intermedios desconocidos para infectar a humanos.(9) Se ha especulado que existen varios reservorios, no confirmados(10) El hecho de que SARS-CoV-2 haya llegado a los humanos, implica la probabilidad de futuros brotes zoonóticos con virus similares.(11) La secuencia del genoma de este virus es 96,2% idéntica al CoV RaTG13 del murciélago, y comparte un 79,5% de identidad con el SARS-CoV.(4)
La proteína S, Spike, permite la entrada y la infección en el huésped ya que, contiene el dominio de unión al receptor de las células que infecta, y es la determinante del tropismo del virus. Consta de dos dominios: el dominio S1, encargado de la unión al receptor y el dominio S2, responsable de la fusión con la membrana celular (Figura 1).(3,11)
Dentro de la célula, el genoma del SARS-CoV-2 codifica una poliproteína (ORF1ab), involucrada en la transcripción y replicación del ARN viral,(4) usando la angiotensina II humana (ACE2) como receptor de entrada celular (Figura 2).(12) La ACE2 se distribuye en las células epiteliales de los alvéolos, tráquea, bronquios, glándulas bronquiales serosas, monocitos alveolares y macrófagos del tracto respiratorio. Además, se expresa en menor frecuencia en células cardíacas, renales e intestinales.(13) La ACE2 también podría expresarse en las glándulas salivales y lengua, sugiriendo que la cavidad oral sería un reservorio del SARS-CoV-2, y por ello, la importancia de la saliva como biofluido transmisor del virus y su uso como muestra para su detección.(7)
La respuesta del sistema inmunológico se manifiesta con la inflamación y el reclutamiento de células presentadoras de antígenos; participando en esto, las células inmunitarias innatas, que son la primera línea de defensa, liberando citocinas y quimiocinas inflamatorias. Las células dendríticas son importantes para iniciar la respuesta inmune adaptativa, principalmente los linfocitos T helper (CD4+). La fuerte activación del sistema inmunológico induce una producción anormal de citocinas, conocida como “tormenta de citocinas”, especialmente en casos severos, afectando mayoritariamente a personas de mediana edad (50-69 años) y adultos mayores (≥70 años).(14,15) Una de las posibles razones de esto es, el envejecimiento pulmonar que está asociado con la incapacidad de las células para multiplicarse a una velocidad normal, lo que resulta en cambios estructurales y funcionales en el tracto respiratorio, dando lugar a una función disminuida de este órgano, remodelación de células alteradas, regeneración deficiente y mayor susceptibilidad a la enfermedad.(16)
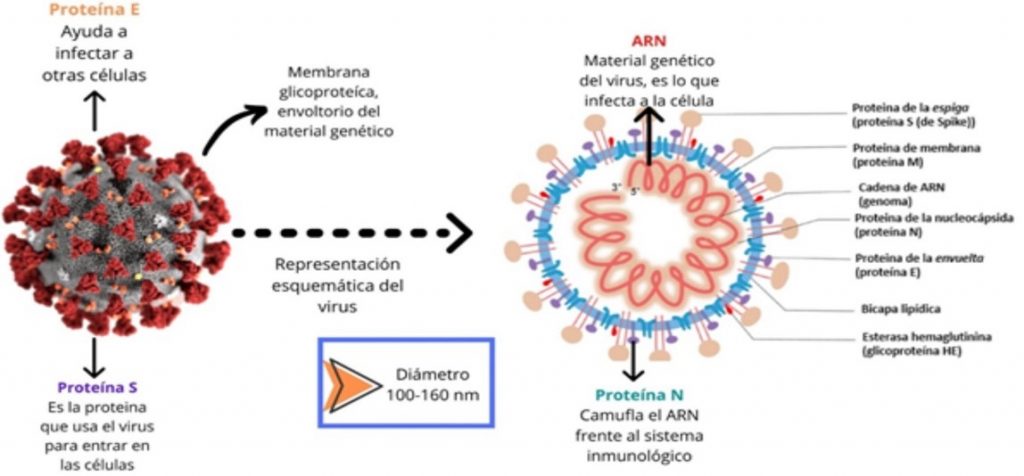
Figura 1. Estructura del virus SARS-CoV-2.
Representación esquemática del virus SARS-COV-2. Se ve el genoma, que contiene siete marcos de lectura abiertos (ORF) que codifican para proteínas virales no estructurales 1a y 1b, y proteínas estructurales (S, espícula; E, envoltura; M, membrana; N, nucleocápside y ORF3, proteína accesoria). La glicoproteína S está presente en la superficie del virión en forma de picos o espigas, por la cual presenta una forma de corona cuando se observa al microscopio electrónico, la glicoproteína S es el mediador de la unión y entrada a la célula huésped, utilizando receptores presentes en las células del hospedero. Hernández SF, et al, 2020.(3)
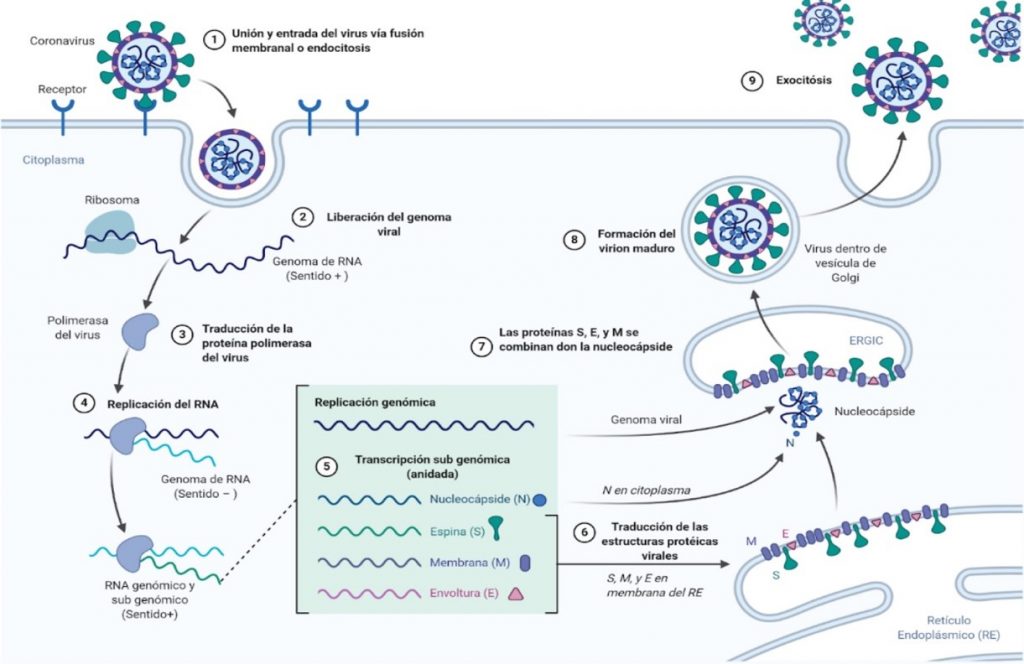
Figura 2. Patogénesis del virus SARS-CoV-2.
Esquema simplificado de replicación del SARS-CoV-2. Traducción en el ribosoma de una proteína esencial, que es la replicasa (RNA polimerasa dependiente de RNA), formación del complejo de transcripción, fabricación del mRNA con las instrucciones para sintetizar las proteínas virales en los ribosomas de la célula, y fase final de ensamblaje, maduración y exocitosis. Apaza A, et al, 2020.(28)
La mayoría de los pacientes con COVID-19 presentan síntomas inespecíficos y signos respiratorios típicos, variando de leves a severos.(17) Inicialmente, se caracterizan por presentar fiebre, tos y anosmia. Hay mialgia y fatiga aproximadamente en un 50% de los casos. Con menos frecuencia, hay odinofagia, cefalea, náuseas, anorexia, vómitos, dolor abdominal, miocarditis aguda, gastroenteritis, diarrea, ageusia, eructos y reflujos. En los enfermos graves, se observa disnea, la cual puede progresar hasta la muerte.(18,19)
Las principales anomalías de laboratorio son la linfopenia, leucocitosis con predominio de neutrófilos y trombocitopenia. Los pacientes que mueren debido a la virosis tienen una linfopenia mayor que los supervivientes o en aquellos con enfermedad leve, siendo el principal hallazgo en el 85% de los pacientes críticos y un marcador de mal pronóstico.(19) Además, hay hipoalbuminemia y marcadores inflamatorios elevados, como la proteína C reactiva, lactato deshidrogenasa, velocidad de sedimentación globular, alanina transaminasa, aspartato aminotransferasa, creatincinasa, entre otras.(20)
La prueba “Gold Standard” para identificar al SARS-CoV-2 es la PCR, siendo la más utilizada la PCR transcriptasa reversa en tiempo real (RT-qPCR). Tendría una sensibilidad y especificidad del 100%, no exenta de resultados erróneos. Para Yang y Zhao, la sensibilidad sería 70%. Describieron en muestras nasales, un 27% de falsos negativos y un 40% en muestras faríngeas. Estos resultados, se deben con mayor frecuencia a errores en la fase pre-analitica, a diferencia, de los falsos positivos, los cuales, son debido en mayor proporción al proceso analítico.(21)
En el año 2020, aparecieron test rápidos de inmunocromatografía para la detección del virus, que detectan IgG e IgM, que tienen alto rendimiento y son más adecuadas para laboratorios de diagnóstico de mayor complejidad. La utilidad de los test está limitada por la respuesta inmune de cada individuo y se vería afectada por la posible pérdida de anticuerpos con el tiempo.(22)
Las pruebas de detección rápida de antígenos (Ag-RDT), diagnostican la infección activa mediante el hallazgo de proteínas virales del SARS-CoV-2, en las secreciones respiratorias. A menudo, se detecta la proteína N de la nucleocápside del virus, debido a su abundancia y estructura conservada. También, detecta otras proteínas virales, como la proteína S. Proporcionan resultados entre 15-20 minutos. El virus se puede detectar dentro de los primeros 8 días después de la aparición de los síntomas, recomendando el uso de estos test dentro de este periodo de tiempo. En septiembre del 2020, la OMS recomendó una sensibilidad mínima del 80% y una especificidad del 97% para las pruebas de antígenos, en comparación con la RT-PCR.(23,24)
La muestra de elección para este diagnóstico de COVID-19, es el hisopado nasofaríngeo, ya que la carga viral es superior en las fosas nasales que en la orofaringe. Los hisopos orales como método de recolección de la muestra probablemente sean aplicables en la detección temprana del virus, mientras que la de saliva, tiene la ventaja de una recolección más aceptable para los pacientes y más segura para los trabajadores de la salud. Hasta ahora, se ha informado de tres métodos para recolectar saliva: toser, hisopos de saliva y directamente de la glándula salival. Para aplicaciones clínicas, la saliva de la garganta profunda tiene la tasa positiva más alta, lo que puede representar un diagnóstico temprano de COVID-19. La saliva, directamente de las glándulas salivales, se asocia con la severidad de la enfermedad y posiblemente podría ser una prueba predictiva.(7)
Coinfecciones en pacientes con COVID-19
La tasa de mortalidad descrita por Botti, et al, es del 3,4% de los pacientes diagnosticados con COVID-19. Aproximadamente el 5% de estos, presentan SDRA grave y requieren ingreso en UCI. Los críticamente enfermos tienen una alta probabilidad (42%) de necesitar intubación prolongada, ventilación mecánica (VM) y posteriormente puede requerir traqueotomía.(25)
Los estudios sobre coinfecciones por bacterias, hongos u otros virus en pacientes con COVID-19 son escasos, lo que puede deberse a que la mayoría de las publicaciones sobre este tema son recientes.(26)
Las infecciones secundarias, son un factor importante que no puede ser ignorado en estos pacientes, principalmente, en aquellos que presentan comorbilidades como diabetes mellitus, hipertensión, obesidad, enfermedad cardiovascular y enfermedad pulmonar obstructiva crónica (EPOC). Los pacientes que presentan este tipo de condiciones tienen un mayor riesgo de enfermar gravemente y requerir ingreso en la UCI, necesitando VM, nutrición parenteral, tratamiento antimicrobiano de amplio espectro, catéteres venosos centrales permanentes o vesicales, corticosteroides, entre otros. Una mayor hospitalización, los hace más propensos a desarrollar coinfecciones bacterianas o fúngicas.(5,6)
Los datos clínicos muestran que la tasa de coinfección bacteriana o fúngica de los infectados por SARS-CoV-2 es menor, comparada con la de otras infecciones, por ejemplo, la del virus de la influenza.(5) Esto, puede deberse a los pocos informes clínicos relevantes y al uso extenso de antibióticos en el diagnóstico temprano de la infección, y porque, los estudios sobre este tipo de infecciones son escasos, y en la mayoría de las publicaciones no se incluye un análisis de pronóstico, aun cuando se han encontrado infecciones secundarias en el 50% de los pacientes con COVID-19, no supervivientes. La cifra de coinfección bacteriana y fúngica con SARS-CoV-2 es proporcional a la gravedad de la enfermedad y esto irá deteriorando el estado de los pacientes.(19)
Los patógenos más frecuentes productores de coinfecciones incluyen bacterias, como Streptococcus pneumoniae, Staphylococcus aureus, Klebsiella pneumoniae, Mycoplasma pneumoniae, Chlamydia pneumoniae, Legionella pneumophila y Acinetobacter baumannii. Dentro de los hongos están, Candida albicans, Candida glabrata, Aspergillus fumigatus y Aspergillus flavus y virus como el de la influenza A y B, Coronavirus, Rinovirus/Enterovirus, virus Parainfluenza, Metapneumovirus humano y virus de inmunodeficiencia humana (VIH).(27)
Micosis en pacientes COVID-19
A partir del 2019, se han publicado artículos que hacen referencia a micosis oportunistas en pacientes críticos con COVID-19. Según algunos, parece haber una asociación entre estas dos patologías.(28)
La Sociedad Francesa de Micología Médica, ha descrito, que las coinfecciones fúngicas invasivas en estos pacientes podrían estar siendo infra-diagnosticadas, y ha establecido que las enfermedades respiratorias crónicas, el tratamiento con corticosterioides, la tormenta de citoquinas y la intubación, son factores de riesgo para desarrollar micosis, llegando a tener una incidencia de 10-30%.(29)
Las micosis presentan una amenaza adicional en la tarea de tratar a los pacientes con COVID-19, debido a que los hongos son una importante causa de morbilidad y mortalidad en inmunodeprimidos; como en el caso de una infección pulmonar grave que afecta a ambos lóbulos del pulmón, infecciones viscerales graves de dos o más sistemas orgánicos, incluidos los que afectan al SNC, infección sistémica multiorgánica de tres o más órganos, o fungemia.(30)
Si bien, no se ha enfatizado en las infecciones secundarias en pacientes críticos con COVID-19, el impacto a largo plazo de estas coinfecciones puede llevar a la muerte del paciente, en particular aquellos que requieren VM o que continúen necesitando terapia inmunomoduladora.(31) También, debe darse la misma importancia a las infecciones pulmonares ocasionadas por hongos oportunistas, poco frecuentes, como Histoplasma capsulatum, Mucor spp y Cryptococcus spp. Se han informado pocos casos de mucoromicosis invasiva en pacientes con COVID-19. Recientemente, en India, se ha reportado un aumento explosivo de casos de esta afección altamente letal, que podría estar relacionada con el número de diabéticos y el uso de esteroides para el SARS-CoV-2.(32)
Los enfermos con COVID-19 que se encuentran en estado crítico, presentan niveles más altos de citocinas proinflamatorias (IL-1, IL-2, IL-6, factor de necrosis tumoral alfa) y antiinflamatorias (IL-4, IL-10), produciendo una desregulación en el sistema inmune, que afecta tanto a las células T helper 1 (Th1) y T helper 2 (Th2), siendo Th17 el subtipo más relevante. Estas células, actúan principalmente en la barrera de la mucosa pulmonar, produciendo y liberando interleucina-17 (IL-17), que contribuye a mejorar la organización de las células B y T en el tejido linfoide, asociado a los bronquios, interviniendo en la mediación de las respuestas inmunitarias secundarias, y la liberación de β-defensinas antifúngicas. Para esto, los pacientes con deficiencia en la producción o señalización de IL-17 parecen ser más susceptibles a micosis, además, de contribuir con la patología pulmonar, promoviendo la proliferación microbiana y una infección posterior. A su vez, aumenta el riesgo de infecciones fúngicas invasivas (IFI), tales como aspergilosis invasiva pulmonar (IPA), aspergilosis pulmonar asociada a COVID-19 (CAPA), candidiasis invasiva (IC) o neumonía por Pneumocystis jirovecii.(26)
La IL-6 es responsable de causar daño pulmonar y la eventual falla multiorgánica en pacientes en estado crítico. Debido a esto, es necesario para el tratamiento la administración de Tocilizumab (anticuerpo monoclonal, humanizado, recombinante), contra el receptor de IL-6. Este fármaco disminuye los altos niveles de IL-6 para prevenir la disfunción multiorgánica causada por una tormenta de citocinas. Sin embargo, las consecuencias asociadas al tratamiento son el aumento del riesgo de infecciones bacterianas y fúngicas después de la terapia inmunosupresora, lo que incrementa el riesgo de producir CAPA. Aún no se ha estudiado completamente si el uso de terapias inmunomoduladoras y antibióticos podrían ser responsable del aumento de la susceptibilidad de los pacientes con COVID-19 y de la enfermedad micótica invasiva pulmonar.(26,33)
En noviembre del 2020, fue notificada una neumonía por Rhizopus azygosporus, en un estadounidense, de 56 años, que había recibido metilprednisolona y tocilizumab como tratamiento. La administración de estos dos inmunosupresores probablemente contribuyó al riesgo de micosis.(34)
Aspergillus spp.
Los Aspergillus, son hongos ubicuos en el medio ambiente y causan infecciones en los humanos, incluida la IPA, la aspergilosis pulmonar crónica (CPA), la aspergilosis broncopulmonar alérgica (ABPA), la rinosinusitis crónica, el asma fúngica, la bronquitis por Aspergillus spp. y CAPA.(35)
La CAPA, afecta principalmente a pacientes de UCI con anomalías pulmonares graves. Los factores de riesgo descritos en estos casos, incluyen la edad avanzada, linfopenia, enfermedades respiratorias crónicas, terapia con corticosteroides, terapia antimicrobiana, VM o tormenta de citocinas. La mortalidad reportada para esta nueva entidad es del 65%.(36)
Los datos sobre cambios patológicos en pacientes con SARS-CoV-2, son escasos. Se han informado lesiones alveolares difusas, incluida la formación de membranas hialinas combinadas con infiltración neutrofílica intraalveolar y congestión vascular. Estos daños histológicos podrían orientar a posibles infecciones secundarias como CAPA. Los pacientes bajo VM no comienzan inmediatamente con esta enfermedad; generalmente la colonización de Aspergillus spp., ocurre más tarde. En el caso de IPA, esta colonización sucede poco después de que el paciente se colocó bajo VM.(26)
Se ha demostrado que las infecciones pulmonares virales graves se asocian con un mayor riesgo de IPA, aumentando la probabilidad de coinfecciones fúngicas en pacientes con COVID-19, con una alta incidencia en pacientes UCI.(37)
Los factores de riesgo para producir IPA, incluyen neutropenia prolongada, EPOC, trasplante alogénico de células madre hematopoyéticas (alo-TCMH), trasplante de órganos sólidos (SOT), inmunodeficiencias hereditarias, enfermedades hematopoyéticas malignas (HM), fibrosis quística (FQ).(6) Otro factor importante, es la liberación de patrones moleculares como citocinas pro-inflamatorias asociados a COVID-19, dando como resultado un daño epitelial pulmonar.(35)
En pacientes con enfermedad pulmonar relacionada con COVID-19, se debe considerar realizar pruebas para detectar la presencia de Aspergillus spp., en las secreciones de las vías respiratorias inferiores y de galactomanano (GM) en muestras de suero consecutivas o lavado bronqueoalveolar (LBA). Aspergillus fumigatus y Aspergillus flavus, son los agentes más frecuentes(38) (Tabla 1).
Los criterios diagnósticos de consenso para la aspergilosis invasiva, a menudo no se cumplen en pacientes críticamente enfermos previamente inmunocompetentes, debido a la falta de factores de riesgo del huésped, confusión en la interpretación de las imágenes de tórax y la dificultad para realizar biopsias pulmonares en pacientes con VM invasiva.(38)
Uno de los primeros casos de IPA por A. fumigatus, comprobada, en un paciente con COVID-19, fue en un varón de 79 años, con diabetes mellitus tipo 2, hipertensión, fibrilación auricular paroxística e insuficiencia cardíaca crónica, en un hospital de Amstelveen, Holanda(39) (Tabla 1).
El diagnóstico para CAPA e IPA, se basa en la detección de pruebas positivas de GM y 1,3-β-d-glucano (BDG) en suero, evidencia histopatológica y crecimiento de Aspergillus spp. en cultivo. El GM de LBA es importante para diagnosticar a estos pacientes, observándose niveles altos en aquellos con presunta IPA, así como, la sospecha clínica primaria para una terapia antimicótica adecuada y dirigida con los protocolos nacionales e internacionales.(40,41)
Algunos métodos de diagnóstico para apoyar el reconocimiento de estas micosis son la tomografía computarizada, la biopsia y la broncoscopia. Esta última, está indicada en pacientes críticamente enfermos, ya que, junto con la biopsia se consideran métodos invasivos.(42)
Tabla 1 – Resumen de casos de aspergilosis asociadas a COVID-19
| Autores | País | Microorganismo | Casos (%) |
| Van Someren G, et al., 2021(39) | Holanda | A. fumigatus (IPA) | 1 |
| Bartoletti, et al., 2020(55) | Italia | Aspergillus spp. (CAPA) | 30 (27,7%) |
| Gangneux, et al., 2020(56) | Francia | Aspergillus spp. (IPA) | 15 (33%) |
| Alanio, et al., 2020(57) | Francia | Aspergillus spp. (CAPA) | 29 (33%) |
| Nasir, et al, 2020(58) | Pakistán | Aspergillus spp. (CAPA) (colonizados) | 5 (22%)
4 (17%) |
| Wang, et al., 2020(59) | China | A. fumigatus (IPA) | 8 (8%) |
| Rutsaert, et al., 2020(60) | Bélgica | Aspergillus spp. (CAPA) | 7 (35%) |
| Van Arkel A, et al., 2020(61) | Holanda | A. fumigatus (CAPA) | 5 (45%) |
| Koehler, et al., 2020(62) | Alemania | A. fumigatus (CAPA) | 5 (26%) |
| Blaize, et al., 2020(63) | Francia | A. fumigatus | 1 |
| Lescure, et al., 2020(64) | Francia | A. flavus (CAPA) | 1 (20%) |
| Antinori, et al., 2020(65) | Italia | A. fumigatus (IPA) | 1 |
| Meijer, et al., 2020(66) | Holanda | A. fumigatus (CAPA) | 1 |
| Prattes, et al., 2021(37) | Austria | Aspergillus fumigatus (IPA) | 1 |
| Fernández, et al., 2021(67) | Argentina | A. flavus (IPA) | 1 |
| Santana, et al., 2020(68) | Brasil | A. penicillioides (IPA) | 1 |
| Sharma, et al., 2021(69) | Australia | A. fumigatus (CAPA) | 1 |
| Hughes, et al., 2020(70) | Inglaterra | A. fumigatus | 3 (2,6%) |
| Zhu X, et al., 2020(71) | China | Aspergillus spp. | 60 (23,3%) |
| Yang X, et al., 2020(72) | China | A. flavus
A. fumigatus |
1 (1,9%)
1 (1,9%) |
| Freire, et al., 2020(73) | Brasil | A. penicillioides (IPA) | 1 |
IPA: Aspergilosis pulmonar invasiva, CAPA: Aspergilosis asociada a COVID-19. Fuente: Elaboración propia.
Candida spp.
Las especies de Candida, son la causa más importante de micosis oportunistas en el mundo. Constituyen un problema de salud pública, con una alta mortalidad cuando se complica con shock séptico.(43) Estas levaduras se encuentran en superficies mucosas y cutáneas del cuerpo humano. Pocas especies están asociadas con la enfermedad, que incluyen a C. albicans, C. glabrata, C. tropicalis, C. parapsilosis, C. krusei y C. dubliniensis. La especie más aislada sigue siendo C. albicans.(44)
En pacientes graves con COVID-19, la candidiasis orofaríngea (OPC) podría ser una causa probable de morbilidad en estos, la que comienza con la colonización de Candida spp. en la mucosa oral. Los enfermos pueden sentir malestar local, una sensación alterada del gusto, ardor bucal, glosodinia, disfagia y dificultad para respirar. En la mayoría de los casos, esta candidiasis se adquiere de forma endógena, cuando el paciente está inmunodeprimido.(45)
En un estudio, en la Universidad de Ciencias Médicas de Teherán, Irán, se investigaron 53 pacientes hospitalizados con COVID-19 y OPC, encontrando que C. albicans era el patógeno más común, representando el 70,7%, seguido de C. glabrata 10,7%, C. dubliniensis 9,2%, C. parapsilosis sensu stricto 4,6%, C. tropicalis 3% y C. krusei 1,5%(5) (Tabla 2).
La candidiasis invasiva es rara, pero se asocia con mortalidad alta en los enfermos críticos, tratados con antimicrobianos de amplio espectro, nutrición parenteral y exámenes invasivos, o en aquellos con neutropenia prolongada y deterioro inmunológico. En estos, el riesgo de infección por especies de Candida puede aumentar significativamente, surgiendo la necesidad de un reconocimiento temprano de la micosis, de terapia antifúngica y una intervención adecuada, que son requisitos básicos para mejorar el resultado en los pacientes en UCI.(6,46)
Hay especies de Candida que se aíslan en menor frecuencia, como Candida auris. En Brasil, en Bahía, en el año 2020, se encontraron los primeros cultivos de pacientes en un hospital terciario, mostrando crecimiento de C. auris(47) (Tabla 2). Esta especie fue diferenciada de otras por MALDI-TOF, en un grupo de pacientes hospitalizados en UCI COVID-19. La identificación mostró un nivel de confianza del 99,9%.(47) Esta técnica, se ha utilizado con éxito en entornos clínicos, como herramienta de diagnóstico para detectar bacterias, hongos y virus, y su patogénesis, pudiendo identificar también al SARS-CoV-2.(48)
Tabla 2 – Resumen de casos de candidiasis asociadas a COVID-19.
| Autores y referencias | País | Microorganismo | Casos (%) |
| Salehi et al. 2020(5) | Irán | C. albicans
C. glabrata C. dubliniensis C. parapsilosis sensu strictus C. tropicalis (OPC) |
46 (70,7%)
7 (10,7%) 6 (9,2%) 3 (4,6%) 2 (3%) |
| Chowdhary et al. 2020(74) | India | C. auris
C. albicans C. tropicalis Candida krusei (Candidemia) |
10 (67%)
3 (20%) 1 (6,6%) 1 (6,6%) |
| Hughes et al. 2020(70) | Inglaterra | C. albicans (Candidemia) | 3 (2,7%) |
| Zhu X et al. 2020(71) | China | C. albicans (Candidemia) | 2 (0.8%) |
| Chen N et al. 2020(75) | China | C. albicans
C. glabrata |
3 (3%)
1 (1%) |
| Almeida et al. 2021(47) | Brasil | C. auris (Colonizados) | 11 |
OPC: Candidiasis orofaríngea. Fuente: Elaboración propia.
Hay que tener en consideración otros microorganismos en Latinoamérica, ya que, a medida que avanza COVID-19, se podrían presentar casos de micosis endémica. En Argentina, en el 2020, una mujer de 36 años, con VIH, ingresó a un servicio de urgencias, tras sufrir 15 días de disnea, tos y sudores nocturnos. En la paciente se encontró Histoplasma capsulatum y la RT-PCR fue negativa para SARS-CoV-2. Después de 7 días de tratamiento, la prueba fue positiva y la paciente fue trasladada a una sala de COVID-19.(49) En Brasil, un varón de 43 años, con infección por VIH, presentaba los mismos síntomas que el caso anterior. Cuarenta y ocho horas, después del ingreso del paciente, en su cultivo de piel y hemocultivo de una muestra previa, hubo crecimiento de Histoplasma capsulatum y se obtuvo un resultado positivo de RT-PCR para SARS-CoV-2, a partir de la muestra tomada al ingreso hospitalario.(50)
Existe un alto riesgo de propagación del SARS-CoV-2 en los centros hospitalarios, por lo que el CDC actualiza constantemente las recomendaciones para el control de la infección. Asimismo, hay que fortalecer las prácticas estándares de control de infecciones hospitalarias, teniendo como objetivo reducir la propagación nosocomial.(49) A partir de mayo de 2021, hay informes de numerosos casos de COVID-19, en la India, otros en Brasil, Paraguay, Uruguay, México asociados a mucoromicosis, en diabéticos o con tratamiento con corticoides, parte de los cuales han sido revisados por Singh et al.(51)
Es importante destacar la labor invisible de los Laboratoristas clínicos (Tecnólogos Médicos, Biomédicos, Farmacéuticos, Médicos Laboratoristas) en la actual pandemia para detectar al SARS-CoV-2, ya que son estos profesionales quienes realizan los exámenes de PCR para el diagnóstico de COVID-19. El primer caso descrito en Chile, en Talca, fue realizado por un Tecnólogo médico.(52,53)
En Chile, hay más de 130 laboratorios que realizan PCR, informando resultados de exámenes de COVID-19, en todas las regiones del país. La implementación de estos laboratorios en distintos países que realicen PCR, tiene un efecto positivo, al permitir ejecutar exámenes por esta técnica que probablemente no habrían sido implementados si no fuese por la pandemia.
En Chile, en la ciudad de Valparaíso, Cruz R, et al, evidenció un aumento de la positividad del biomarcador GM durante el año 2019-2020, viéndose un incremento de solicitudes de este marcador en muestra de LBA, lo que demostró un acrecentamiento de las micosis en pacientes críticos en la pandemia de COVID-19.(54)
Es necesario mejorar los flujogramas para el diagnóstico de la coinfección en estos pacientes, para tener una sospecha oportuna, proporcionando un tratamiento eficiente y, además; de mantener a la población informada, adhiriéndose a las normas sanitarias para fortalecer la prevención de la COVID-19 y de infecciones secundarias.
Abstract
The global outbreak of SARS-CoV-2, described as of 2019 whose expansion caused the COVID-19 pandemic, has created a risk to people’s health, presenting itself as a threat to life and an international public health emergency, which to the date cannot be controlled. Coinfection in these patients, by viruses, bacteria and fungi, increases the difficulty of diagnosis, treatment and prognosis of the disease. It’s important to deepen the knowledge about the SARS-CoV-2 virus and the co-infections that could occur, in particular, in patients with COVID-19 who present with mycosis. The objective of this bibliographic review is to determine the importance of mycosis, as an opportunistic disease, in patients affected by SARS-CoV-2. A systematic bibliographic review was carried out in the “PubMed-NCBI” database, using the keywords and / or headings: “COVID-19”, “SARS-CoV-2”, “Coronavirus”, “COVID-19 and coinfection” ,“Mycosis”, “Aspergillus spp.”, “Candida spp.” COVID-19 and Aspergillus spp.”, “COVID-19 and Candida spp.”. From the analysis of the literature, one can conclude the importance of respiratory mycoses, caused by various fungal pathogens in patients with COVID-19. The disease was described in 2019 and there is few a information on cases and their management, making it necessary to strengthen the investigation of coinfection in these patients, in order to improve the flow charts of clinical suspicion, contributing to diagnoses, accurate treatments and promoting prevention against to this pandemic.
Keywords
SARS-CoV-2; Immunosuppression; Coinfection; Aspergillus spp.; Candida spp.
Bibliografía
- Esakandari H, Nabi-Afjadi M, Fakkari-Afjadi J, Farahmandian N, Miresmaeili SM, Bahreini E. A comprehensive review of COVID-19 characteristics. Biol Proced Online. 2020, 22(1):19.
- Pascarella G, Strumia A, Piliego C, Bruno F, Del Buono R, Costa F, et al. COVID-19 diagnosis and management: a comprehensive review. J Intern Med. 2020, 288(2):192-206.
- Selene Fernández Hernández, Rosa Elena Sarmiento Silva, María Elena Trujillo Ortega. Coronavirus en las diferentes especies. porcicultura.com. Jul 6;2020. Available from: https://www.porcicultura.com/destacado/Coronavirus-en-las-diferentes-especies
- Zhang XY, Huang HJ, Zhuang DL, Nasser MI, Yang MH, Zhu P, Zhao MY. Biological, clinical and epidemiological features of COVID-19, SARS and MERS and AutoDock simulation of ACE2. Infect Dis Poverty. 2020;9(1):99.
- Chen X, Liao B, Cheng L, Peng X, Xu X, Li Y, Hu T, Li J, Zhou X, Ren B. The microbial coinfection in COVID-19. Appl Microbiol Biotechnol. 2020;104(18):7777-7785.
- Song G, Liang G, Liu W. Fungal Co-infections Associated with Global COVID-19 Pandemic: A Clinical and Diagnostic Perspective from China. Mycopathologia. 2020;185(4):599-606.
- Xu R, Cui B, Duan X, Zhang P, Zhou X, Yuan Q. Saliva: potential diagnostic value and transmission of 2019-nCoV. Int J Oral Sci. 2020;12(1):11-12.
- Deshmukh V, Tripathi SC, Pandey A, Deshmukh V, Vykoukal J, Patil A, Sontakke B. COVID-19: a conundrum to decipher. Eur Rev Med Pharmacol Sci. 2020;24(10):5830-5841.
- Vellas C, Delobel P, de Souto Barreto P, Izopet J. COVID-19, Virology and Geroscience: A Perspective. J Nutr Health Aging. 2020;24(7):685–691.
- Kannan S, Shaik Syed Ali P, Sheeza A, Hemalatha K. COVID-19 (Novel Coronavirus 2019) – recent trends. Eur Rev Med Pharmacol Sci. 2020;24(4):2006-2011.
- Fernández-Rodríguez A, Casas I, Culebras E, Morilla E, Cohen MC, Alberola J. COVID-19 y estudios microbiológicos post mortem. Rev Española Med Leg. 2020;46(3):127-138.
- Introducción a la biología molecular del Coronavirus SARS-CoV-2. Biología Molecular, Evolución Química y Astrobiología. Jul 8, 2020. Available from: http://www3.uah.es/chemevol/index.php/introduccion-a-la-biologia-molecular-del-coronavirus-sars-cov-2/
- Lee I-C, Huo T-I, Huang Y-H. Gastrointestinal and liver manifestations in patients with COVID-19. J Chin Med Assoc. 2020;83(6):521–523.
- Sanz JM, Gómez Lahoz AM, Martín RO. Papel del sistema inmune en la infección por el SARS-CoV-2: inmunopatología de la COVID-19 [Role of the immune system in SARS-CoV-2 infection: immunopathology of COVID-19]. Medicine (Madrid). 2021;13(33):1917-1931.
- García-Salido A. Revisión narrativa sobre la respuesta inmunitaria frente a coronavirus: descripción general, aplicabilidad para SARS-COV-2 e implicaciones terapéuticas [Narrative review of the immune response against coronavirus: An overview, applicability for SARS-COV-2, and therapeutic implications]. An Pediatr (Engl Ed). 2020;93(1):60.e1-60.e7.
- Salehi M, Ahmadikia K, Badali H, Khodavaisy S. Opportunistic Fungal Infections in the Epidemic Area of COVID-19: A Clinical and Diagnostic Perspective from Iran. 2020;185(4):607-611.
- Oliveira BA, Oliveira LC de, Sabino EC, Okay TS. SARS-CoV-2 and the COVID-19 disease: a mini review on diagnostic methods. Rev Inst Med Trop Sao Paulo. 2020;62:e44.
- Berger JR. COVID-19 and the nervous system. J Neurovirol. 2020;26(2):143-148.
- Schmulson M, Dávalos MF, Berumen J. Beware: Gastrointestinal symptoms can be a manifestation of COVID-19. Rev Gastroenterol Mex. 2020;85(3):282–287.
- Rodriguez-Morales AJ, Cardona-Ospina JA, Gutiérrez-Ocampo E, Villamizar-Peña R, Holguin-Rivera Y, Escalera-Antezana JP, et al. Clinical, laboratory and imaging features of COVID-19: A systematic review and meta-analysis. Travel Med Infect Dis. 2020;34:101623.
- Accini Mendoza JL, Nieto Estrada VH, Beltrán López N, Ramos Bolaños E, Molano Franco D, Dueñas Castell C, Valencia Moreno AA, Alarcón Amaya IC, Serna Flórez J, Gil Valencia BA, Pizarro C, Zabaleta Polo YM, Chica Meza CL. Actualización de la Declaración de consenso en medicina critica para la atención multidisciplinaria del paciente con sospecha o confirmación diagnóstica de COVID-19. Acta Colombiana de Cuidado Intensivo. 2020;20:1-112.
- Batra R, Olivieri LG, Rubin D, Vallari A, Pearce S, Olivo A, et al. A comparative evaluation between the Abbott PanbioTM COVID-19 IgG/IgM rapid test device and Abbott ArchitectTM SARS CoV-2 IgG assay. J Clin Virol. 2020;132:104645.
- Peeling RW, Olliaro PL, Boeras DI, Fongwen N. Scaling up COVID-19 rapid antigen tests: promises and challenges. Lancet Infect Dis. 2021;S1473-3099(21)00048-7.
- Mboumba Bouassa R-S, Veyer D, Péré H, Bélec L. Analytical performances of the point-of-care SIENNATM COVID-19 Antigen Rapid Test for the detection of SARS-CoV-2 nucleocapsid protein in nasopharyngeal swabs: A prospective evaluation during the COVID-19 second wave in France. Int J Infect Dis. 2021;106:8-12.
- Botti C, Lusetti F, Neri T, Peroni S, Castellucci A, Salsi P, et al. Comparison of percutaneous dilatational tracheotomy versus open surgical technique in severe COVID-19: Complication rates, relative risks and benefits. Auris Nasus Larynx. 2021;48(3):511-517.
- Pemán J, Ruiz-Gaitán A, García-Vidal C, Salavert M, Ramírez P, Puchades F, et al. Fungal co-infection in COVID-19 patients: Should we be concerned? Rev Iberoam Micol. 2020;37(2):41-46.
- Lai C-C, Wang C-Y, Hsueh P-R. Co-infections among patients with COVID-19: The need for combination therapy with non-anti-SARS-CoV-2 agents? J Microbiol Immunol Infect. 2020;53(4):505-512.
- Agrifoglio A, Cachafeiro L, Figueira JC, Añón JM, García de Lorenzo A. Critically ill patients with COVID-19 and candidaemia: We must keep this in mind. J Mycol Med. 2020;30(4):101012.
- Lansbury L, Lim B, Baskaran V, Lim WS. Co-infections in people with COVID-19: a systematic review and meta-analysis. J Infect. 2020;81(2):266-275.
- Yamazaki T, Kume H, Murase S, Yamashita E, Arisawa M. Epidemiology of visceral mycoses: analysis of data in annual of the pathological autopsy cases in Japan. J Clin Microbiol. 1999;37(6):1732-1738.
- Zhang H, Zhang Y, Wu J, Li Y, Zhou X, Li X, et al. Risks and features of secondary infections in severe and critical ill COVID-19 patients. Emerg Microbes Infect. 2020;9(1):1958-1964.
- Grens K. Infección fúngica rara que afecta a pacientes con COVID-19 en la India. TheScientist explorando la vida, inspirando innovación. May 11, 2021. Available from: https://www.the-scientist.com/news-opinion/rare-fungal-infection-affecting-covid-19-patients-in-india
- Deana C, Vetrugno L, Bassi F, De Monte A. Tocilizumab administration in COVID-19 patients: Water on the fire or gasoline? Med Mycol Case Rep. 2021;31:32-34.
- Kanwar A, Jordan A, Olewiler S, Wehberg K, Cortes M, Jackson BR. A Fatal Case of Rhizopus azygosporus Pneumonia Following COVID-19. J fungi (Basel, Switzerland). 2021;7(3):174.
- Arastehfar A, Carvalho A, van de Veerdonk FL, Jenks JD, Koehler P, Krause R, et al. COVID-19 Associated Pulmonary Aspergillosis (CAPA) — From Immunology to Treatment. J Fungi. 2020;6(2):91.
- Machado M, Valerio M, Álvarez-Uría A, Olmedo M, Veintimilla C, Padilla B, et al. Invasive pulmonary aspergillosis in the COVID-19 era: An expected new entity. Mycoses. 2021;64(2):132-143.
- Prattes J, Valentin T, Hoenigl M, Talakic E, Reisinger AC, Eller P. Invasive pulmonary aspergillosis complicating COVID-19 in the ICU – A case report. Med Mycol Case Rep. 2021;31:2-5.
- Verweij PE, Gangneux JP, Bassetti M, Brüggemann RJM, Cornely OA, Koehler P, Lass-Flörl C, van de Veerdonk FL, Chakrabarti A, Hoenigl M; European Confederation of Medical Mycology; International Society for Human and Animal Mycology; European Society for Clinical Microbiology and Infectious Diseases Fungal Infection Study Group; ESCMID Study Group for Infections in Critically Ill Patients. Diagnosing COVID-19-associated pulmonary aspergillosis. Lancet Microbe. 2020;1(2):e53-e55.
- Van Someren Gréve F, du Long R, Talwar R, Beurskens CJP, Voerman HJ, van Dijk K. Proven Fatal Invasive Aspergillosis in a Patient with COVID-19 and Staphylococcus aureus Pneumonia. J Fungi. 2021;7(3):230.
- Borman AM, Palmer MD, Fraser M, Patterson Z, Mann C, Oliver D, Linton CJ, Gough M, Brown P, Dzietczyk A, Hedley M, McLachlan S, King J, Johnson EM. COVID-19-Associated Invasive Aspergillosis: Data from the UK National Mycology Reference Laboratory. J Clin Microbiol. 2020;59(1):e02136-20.
- García-Salido A. Revisión narrativa sobre la respuesta inmunitaria frente a coronavirus: descripción general, aplicabilidad para SARS-COV-2 e implicaciones terapéuticas [Narrative review of the immune response against coronavirus: An overview, applicability for SARS-COV-2, and therapeutic implications]. An Pediatr (Engl Ed). 2020;93(1):60.e1-60.e7.
- Segrelles-Calvo G, de S Araújo GR, Frases S. Systemic mycoses: a potential alert for complications in COVID-19 patients. Future Microbiol. 2020;15(14):1405-1413.
- Fidler G, Leiter E, Kocsube S, Biro S, Paholcsek M. Validation of a simplex PCR assay enabling reliable identification of clinically relevant Candida species. BMC Infect Dis. 2018;18(1):393.
- Whibley N, Gaffen SL. Beyond Candida albicans: Mechanisms of immunity to non-albicans Candida species. Cytokine. 2015;76(1):42-52.
- Salehi M, Ahmadikia K, Mahmoudi S, Kalantari S, Jamalimoghadamsiahkali S, Izadi A, et al. Oropharyngeal candidiasis in hospitalised COVID-19 patients from Iran: Species identification and antifungal susceptibility pattern. Mycoses. 2020;63(8):771-778.
- Al-Hatmi AMS, Mohsin J, Al-Huraizi A, Khamis F. COVID-19 associated invasive candidiasis. J Infect. 2021;82(2):e45-e46.
- Almeida JN, Francisco EC, Hagen F, Brandão IB, Pereira FM, Presta Dias PH, et al. Emergence of Candida auris in Brazil in a COVID-19 Intensive Care Unit. J Fungi. 2021;7(3):220.
- Mahmud I, Garrett TJ. Mass Spectrometry Techniques in Emerging Pathogens Studies: COVID-19 Perspectives. J Am Soc Mass Spectrom. 2020;31(10):2013-2024.
- Messina FA, Marin E, Caceres DH, Romero M, Depardo R, Priarone MM, et al. Coronavirus Disease 2019 (COVID-19) in a Patient with Disseminated Histoplasmosis and HIV-A Case Report from Argentina and Literature Review. J fungi (Basel, Switzerland). 2020;6(4):275.
- Bertolini M, Mutti MF, Barletta JAE, Falak A, Cuatz D, Sisto A, et al. COVID-19 associated with AIDS-related disseminated histoplasmosis: a case report. Int J STD AIDS. 2020;31(12):1222-1224.
- Singh AK, Singh R, Joshi SR, Misra A, Mucormycosis in COVID-19: Asystematic review of cases reported worldwide and in India, Diabetes & Metabolic Syndrome: Clinical Research & Reviews. 2021;15(4):102146.
- Clínicas de Chile A.G. Dimensionamiento del sector de salud privado en Chile. 2016;1(69):1-108.
- Superintendencia de Salud. Estadísticas de Prestadores Individuales de Salud. Supt Salud. 2019;1(5):1-10.
- Choappa RC, Vieille P, Leiva Y, Noguera M. Aumento en la positividad del biomarcador galactomanano durante la pandemia de COVID-19 en la Quinta Región: Valparaíso. 2021;38(3):340-343.
- Bartoletti M, Pascale R, Cricca M, Rinaldi M, Maccaro A, Bussini L, Fornaro G, Tonetti T, Pizzilli G, Francalanci E, Giuntoli L, Rubin A, Moroni A, Ambretti S, Trapani F, Vatamanu O, Ranieri VM, Castelli A, Baiocchi M, Lewis R, Giannella M, Viale P; PREDICO study group. Epidemiology of invasive pulmonary aspergillosis among COVID-19 intubated patients: a prospective study. Clin Infect Dis. 2020;1065.
- Gangneux JP, Reizine F, Guegan H, Pinceaux K, Le Balch P, Prat E, Pelletier R, Belaz S, Le Souhaitier M, Le Tulzo Y, Seguin P, Lederlin M, Tadié JM, Robert-Gangneux F. Is the COVID-19 Pandemic a Good Time to Include Aspergillus Molecular Detection to Categorize Aspergillosis in ICU Patients? A Monocentric Experience. J Fungi (Basel). 2020;6(3):105.
- Alanio A, Dellière S, Fodil S, Bretagne S, Mégarbane B. Prevalence of putative invasive pulmonary aspergillosis in critically ill patients with COVID-19. Lancet Respir Med. 2020;8(6):e48-e49.
- Nasir N, Farooqi J, Mahmood SF, Jabeen K. COVID-19-associated pulmonary aspergillosis (CAPA) in patients admitted with severe COVID-19 pneumonia: An observational study from Pakistan. Mycoses. 2020;63(8):766-770.
- Wang J, Yang Q, Zhang P, Sheng J, Zhou J, Qu T. Clinical characteristics of invasive pulmonary aspergillosis in patients with COVID-19 in Zhejiang, China: a retrospective case series. Crit Care. 2020;24(1):299.
- Rutsaert L, Steinfort N, Van Hunsel T, Bomans P, Naesens R, Mertes H, Dits H, Van Regenmortel N. COVID-19-associated invasive pulmonary aspergillosis. Ann Intensive Care. 2020;10(1):71.
- Van Arkel ALE, Rijpstra TA, Belderbos HNA, van Wijngaarden P, Verweij PE, Bentvelsen RG. COVID-19-associated Pulmonary Aspergillosis. Am J Respir Crit Care Med. 2020;202(1):132-135.
- Koehler P, Cornely OA, Böttiger BW, Dusse F, Eichenauer DA, Fuchs F, Hallek M, Jung N, Klein F, Persigehl T, Rybniker J, Kochanek M, Böll B, Shimabukuro-Vornhagen A. COVID-19 associated pulmonary aspergillosis. Mycoses. 2020;63(6):528-534.
- Blaize M, Mayaux J, Nabet C, Lampros A, Marcelin A-G, Thellier M, et al. Fatal Invasive Aspergillosis and Coronavirus Disease in an Immunocompetent Patient. Emerg Infect Dis. 2020;26(7):1636-1637.
- Lescure FX, Bouadma L, Nguyen D, Parisey M, Wicky PH, Behillil S, Gaymard A, Bouscambert-Duchamp M, Donati F, Le Hingrat Q, Enouf V, Houhou-Fidouh N, Valette M, Mailles A, Lucet JC, Mentre F, Duval X, Descamps D, Malvy D, Timsit JF, Lina B, van-der-Werf S, Yazdanpanah Y. Clinical and virological data of the first cases of COVID-19 in Europe: a case series. Lancet Infect Dis. 2020;20(6):697-706.
- Antinori S, Rech R, Galimberti L, Castelli A, Angeli E, Fossali T, Bernasconi D, Covizzi A, Bonazzetti C, Torre A, Carsana L, Tonello C, Zerbi P, Nebuloni M. Invasive pulmonary aspergillosis complicating SARS-CoV-2 pneumonia: A diagnostic challenge. Travel Med Infect Dis. 2020;38:101752.
- Meijer EFJ, Dofferhoff ASM, Hoiting O, Buil JB, Meis JF. Azole-Resistant COVID-19-Associated Pulmonary Aspergillosis in an Immunocompetent Host: A Case Report. J Fungi (Basel). 2020;6(2):79.
- Fernandez NB, Caceres DH, Beer KD, Irrazabal C, Delgado G, Farias L, Chiller TM, Verweij PE, Stecher D. Ventilator-associated pneumonia involving Aspergillus flavus in a patient with coronavirus disease 2019 (COVID-19) from Argentina. Med Mycol Case Rep. 2021;31:19-23.
- Santana MF, Pivoto G, Alexandre MAA, Baía-da-Silva DC, Borba MGDS, Val FA, Brito-Sousa JD, Melo GC, Monteiro WM, Souza JVB, Pinheiro SB, Ferreira LCL, Naveca FG, Nascimento VA, Corado ALG, Hajjar LA, Silva Neto JR, Siva GAV, Pasqualotto AC, Lacerda MVG. Confirmed Invasive Pulmonary Aspergillosis and COVID-19: the value of postmortem findings to support antemortem management. Rev Soc Bras Med Trop. 2020;53:e20200401.
- Sharma A, Hofmeyr A, Bansal A, Thakkar D, Lam L, Harrington Z, Bhonagiri D. COVID-19 associated pulmonary aspergillosis (CAPA): An Australian case report. Med Mycol Case Rep. 2021;31:6-10.
- Hughes S, Troise O, Donaldson H, Mughal N, Moore LSP. Bacterial and fungal coinfection among hospitalized patients with COVID-19: a retrospective cohort study in a UK secondary-care setting. Clin Microbiol Infect. 2020;26(10):1395-1399.
- Zhu X, Ge Y, Wu T, Zhao K, Chen Y, Wu B, Zhu F, Zhu B, Cui L. Co-infection with respiratory pathogens among COVID-2019 cases. Virus Res. 2020;285:198005.
- Yang X, Yu Y, Xu J, Shu H, Xia J, Liu H, Wu Y, Zhang L, Yu Z, Fang M, Yu T, Wang Y, Pan S, Zou X, Yuan S, Shang Y. Clinical course and outcomes of critically ill patients with SARS-CoV-2 pneumonia in Wuhan, China: a single-centered, retrospective, observational study. Lancet Respir Med. 2020;8(5):475-481.
- Santana MF, Pivoto G, Alexandre MAA, Baía-da-Silva DC, Borba MGDS, Val FA, Brito-Sousa JD, Melo GC, Monteiro WM, Souza JVB, Pinheiro SB, Ferreira LCL, Naveca FG, Nascimento VA, Corado ALG, Hajjar LA, Silva Neto JR, Siva GAV, Pasqualotto AC, Lacerda MVG. Confirmed Invasive Pulmonary Aspergillosis and COVID-19: the value of postmortem findings to support antemortem management. Rev Soc Bras Med Trop. 2020;53:e20200401.
- Chowdhary A, Tarai B, Singh A, Sharma A. Multidrug-Resistant Candida auris Infections in Critically Ill Coronavirus Disease Patients, India, April-July 2020. Emerg Infect Dis. 2020;26(11):2694-2696.
- Chen N, Zhou M, Dong X, Qu J, Gong F, Han Y, Qiu Y, Wang J, Liu Y, Wei Y, Xia J, Yu T, Zhang X, Zhang L. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. 2020;395(10223):507-513.
Correspondência
Luis Zaror
Escuela de Tecnología Médica,
Facultad de Ciencias, Universidad Mayor, Temuco-Chile. Avenida Alemania N° 281 Temuco-Chile, e-mail: [email protected]
