Leishmaniose Tegumentar Americana: uma análise histopatológica e molecular em lesões de dermatites no estado de Pernambuco, Brasil
American Cutaneous Leishmaniasis: a histopathological and molecular analysis of dermatitis lesions in the State of Pernambuco, Brazil
Maria Auzenir de Anastácio e Silva1
Cynthia Regina Pedrosa Soares2
Fábio Lopes de Melo3
Francisca Janaína Soares Rocha4
1Farmacêutica, especialista em Análises Clínicas e Toxicológicas pela Universidade Federal de Pernambuco (UFPE) – Recife-PE, Brasil.
2Bióloga. Msc em Medicina Tropical. Universidade Federal de Pernambuco (UFPE) – Recife-PE, Brasil.
3Biólogo, Doutor, Pesquisador em Saúde Pública pelo Centro de Pesquisas Aggeu Magalhães, Fiocruz Pernambuco – Recife-PE, Brasil. Brasil.
4Farmacêutica, Doutora em Human Biology pela University of Erlangen-Nuremberg, Alemanha e Professora da Universidade Federal de Pernambuco
(UFPE) – Recife-PE, Brasil.
Instituição: Universidade Federal de Pernambuco (UFPE) – Recife-PE, Brasil.
Recebido em 12/09/2018
Artigo aprovado em 09/08/2019
DOI: 10.21877/2448-3877.201900774
INTRODUÇÃO
Leishmanioses são zoonoses causadas pelo protozoário da família Trypanosomatidae do gênero Leishmania, o qual possui várias formas clínicas diferentes, dependentes da espécie. Leishmaniose Tegumentar Americana (LTA) é uma doença parasitária, crônica, infecciosa e não contagiosa,(1) negligenciada, com risco mundial de aproximadamente 350 milhões de indivíduos e uma incidência de dois milhões de novos casos por ano no mundo.
No Brasil, a LTA encontra-se presente em todos os estados da federação, onde 34% dos municípios pernambucanos são endêmicos para a doença.(2) Nas Américas, a LTA é causada principalmente por Leishmania (Viannia) braziliensise, e L. (Leishmania) mexicana.(3) A LTA apresenta-se em quatro continentes – Américas, Europa, Ásia e África, totalizando 88 países, com um registro anual de 1 milhão a 1,5 milhões de casos. A prevalência real da LTA nas Américas é difícil de ser mensuradas, principalmente por ser uma doença subdiagnosticada, com a ocorrência de diagnósticos incorretos, afecção não aparente, variações de resposta do hospedeiro e multiplicação de agentes etiológicos envolvidos. A distribuição da LTA em todo o território brasileiro é resultado de diferentes condições ecológicas ou geográficas que favorecem de alguma forma a ocorrência dessa doença.(4)
No Brasil, a LTA é endêmica em todas as regiões e foram registrados no país, no período de 1998 a 2008, aproximadamente 282 mil casos.(5) No período de 1995 a 2014, verificou-se uma média anual de 25.763 casos novos registrados e coeficiente de detecção médio de 14,7 casos/100 mil habitantes.(6)
O diagnóstico da LTA, desde a Antiguidade, é um grande desafio para equipes de saúde, pois abrange aspectos epidemiológicos clínicos e laboratoriais, imunológicos e parasitológicos.(7) O diagnóstico da LTA é rotineiramente baseado em evidências clínicas, epidemiológicas, parasitológicas e imunológicas. No exame histopatológico direto deve-se realizar a aspiração ou escarificação da borda interna da úlcera, e, em forma de esfregaço, colocar a amostra sobre uma lâmina, fixando com metanol a 70% e logo em seguida corado com solução de Wright ou Giemsa leishman.(3)
O exame histopatológico direto pode ser confirmado por meio da presença de formas amastigotas no interior do citoplasma de macrófagos na derme e também pelo estudo imunohistoquímico ou por Reação de Polimerase em Cadeia (PCR). Nos exames indiretos pode ser confirmado através da reação sorológica de imunofluorescência indireta (RIFI), reação intradérmica de Montenegro e ensaio imunoenzimático (ELISA).(3) O método mais utilizado para fins de pesquisa para diagnosticar a LTA é o método molecular de PCR por apresentar alta sensibilidade e especificidade, porém, no diagnóstico de rotina, é menos utilizado pela equipe de saúde por ser dispendioso e necessitar de profissionais habilitados.(7)
Um estudo realizado por Vasconcelos et al,(8) no município de Vicência, em Pernambuco, evidenciou que o diagnóstico da LTA foi confirmado através do método clínico e epidemiológico, correspondendo a 207 casos (95,4%), e apenas dez casos (4,6%) foram confirmados com exames laboratoriais apropriados para diagnosticar a LTA. Verificou que 59,4% eram do sexo masculino e possuíam idade menor de 12 anos.(8)
Esse trabalho teve como objetivo a análise histopatológica e molecular em biópsia de pele entre as lesões de dermatites de pacientes com suspeita de Leishmaniose Tegumentar Americana (LTA) no hospital de referência do estado de Pernambuco entre o período de 2016 e 2017.
MATERIAL E MÉTODOs
Trata-se de um estudo descritivo observacional, realizado no setor de dermatologia do Hospital das Clínicas da Universidade Federal de Pernambuco HC/UFPE, Brasil, com o objetivo de descrever as características histopatológicas e detecção molecular de LTA em biópsias de pele de pacientes de um hospital de referência de Pernambuco, Brasil. Pacientes com suspeita de LTA foram atendidos na Dermatologia HC/UFPE. Este estudo foi realizado no período de janeiro de 2016 a dezembro de 2017. Todos os pacientes incluídos no estudo eram adultos e aceitaram participar do estudo por meio da assinatura no Termo de Consentimento Livre e Esclarecido de forma voluntária. Os pacientes foram biopsiados e o diagnóstico histopatológico e molecular de LTA foi realizado.
As amostras de biópsia foram coletadas de 24 pacientes, e seus dados clínicos epidemiológicos foram coletados através de prontuários e amostras de biópsias de pele das lesões com suspeita de infecção por Leishmania registrados pelo setor de Dermatologia do HC/UFPE. As biópsias foram processadas e analisadas histopalogicamente no Laboratório do Serviço de Dermatologia do Hospital das Clínicas da UFPE e molecularmente no Laboratório de Doenças Transmissíveis do Departamento de Parasitologia do IAM, Fiocruz.
Coleta de Biópsia da pele
Todas as lesões cutâneas foram biopsiadas a partir da borda da lesão de cada paciente e armazenadas em tubos cheios de formalina hermeticamente fechados. As biópsias cutâneas foram retiradas por profissionais habilitados do setor de Dermatologia, com tamanho de 5 mm, através de punch e mantidas em blocos de parafina, onde uma parte foi cortada e corada por hematoxilina-eosina (HE) e Giemsa, e outra parte foi colocada em microtubos Eppendorf de 1,5 mL, acondicionadas em recipiente refrigerado e em seguida levadas ao IAM, Fiocruz, PE, ao Departamento de Parasitologia no Laboratório de Doenças Transmissíveis (LDT) para análise molecular.(9)
Teste histopatológico
Cortes histopatológicos dos pacientes foram parafinizados em blocos feitos na espessura de 5 µm, processados e corados pela coloração de hematoxilina-eosina.(9) A quantificação microscópica dos patógenos e a análise das características histopatológicas das doenças foi dada por meio da contagem de dez campos aleatórios no aumento de 40x e 100x,(9) com o objetivo de avaliar o grau histológico e a presença de grânulos metacromáticos.
Outros corantes também foram utilizados para identificar elementos teciduais específicos nos casos em que a suspeita de Leishmaniose foi descartada pelas provas histopatológica e molecular. Os corantes usados para corar os cortes das lesões dos pacientes quando descartada a possibilidade de Leishmaniose foram Ziel Nilsen (ZN), ácido periódico de Schiff (PAS), Sirius red (SR) e formalina.
Teste molecular
Extração de DNA em material de biópsia parafinada. Amostras de biópsia de pele parafinada foram extraídas com kit de extração da Promega ReliaPrep TM Total Nucleic Acid Purification Kit, (Promega, Brasil), seguindo as recomendações do fabricante com algumas adaptações.
O material de biópsia de pele parafinado de cada paciente do hospital das clínicas foi submetido à extração de DNA seguindo os seguintes passos: as lâminas parafinadas com cortes de biópsia foram aquecidas em bloco de aquecimento para o derretimento da parafina, em seguida o material de biópsia foi removido cuidadosamente para um tubo Eppendorf no qual foram adicionados 200 µL de tampão de lise e 20 µL de proteinase K (Cell Lusis Buffer – CLD), agitando-se brevemente em um vórtex por dez segundos e, em seguida, incubados a 55°C por três horas. Após esse tempo foram adicionados 250 µL de Binding Buffer (BBA) e agitados no vórtex por dez segundos. O conteúdo do tubo foi transferido para uma coluna do kit RealiaPrepTM Binding Column e centrifugados por um minuto a 14.000 rpm. Removendo o sobrenadante do tubo de coleta e colocando a coluna em um novo tubo, adicionaram-se 500 µL de tampão de lavagem (Column Wash Solution – CWD) na coluna e centrifugaram-se por três minutos a 14.000 rpm, repetindo esse último passo três vezes. Em seguida, a coluna foi transferida para um tubo de Eppendorf 1,5 mL. Adicionaram-se 50 µL-100 µL de água purificada (Nuclease-free Water) na coluna e centrífugaram-se por um minuto a 14.000 rpm. Descartou-se o ReliaPrepTM Binding Column e guardou-se o eluído a -20°C ou -80°C até o processamento.
Amplificação de DNA – PCR
A PCR foi realizada com o kit da Qiagen TopTaq Master Mix Kit de acordo com o fabricante. A amplificação do DNA da região espaçador interno transcrito 1 (ITS-1) foi realizada com os primers LITSR 5′-CTGGATCATTTCCGATG-3′ e L5.8S 5′-TGATACCACTTATCGCCACTT-3′. As condições de ciclagem foram uma desnaturação inicial de 95°C por três minutos e desnaturação de 95°C por quarenta segundos; o anelamento foi de 53°C a 45 segundos, extensão 72°C de um minuto e a extensão final foi de 72°C por seis minutos. Um controle positivo foi usado com cepa de Leishmania brasiliensis e, para o controle negativo, foram usados apenas os reagentes da PCR e água, sem adição do DNA.
O produto da amplificação foi submetido à eletroforese em gel de agarose a 2% e visualizado em espectrofotômetro e digitalizado através do software L.PIX Loccus Biothecnology (Thermofisher – USA), usando-se um marcador de peso molecular de 100 bp (Invitrogen). Os dados dos pacientes foram armazenados e analisados no banco de dados de Excel versão 2010, com os respectivos resultados para a comparação dos resultados imunológico e molecular.
Comitê de Ética
O estudo foi aprovado pelo Comitê de Ética em Pesquisas envolvendo Seres Humanos (CEP/CCS/UFPE): CAAE número 51426415.0.0000.5208
RESULTADOS
As lesões cutâneas de 24 pacientes com suspeita de LTA foram analisadas por métodos histopatológico e molecular. Dos pacientes estudados, 58,33% eram do sexo masculino e 41,66% do sexo feminino. A faixa etária predominante foi de 33 a 78 anos, com média de 50,2 anos.
Do total de amostras de pacientes com suspeita clínica para Leishmaniose, uma foi positiva pelo método histopatológico, evidenciando dermatite granulomatosa sem necrose com infiltrado inflamatório na derme profunda e fibrose cicatricial de úlcera crônica ativa (Figura 1). Porém, nenhuma das amostras estudadas apresentou o DNA Leishmania braziliensis pela técnica de PCR. Todas as amostras tiveram resultados negativos (Figura 2). Os dados obtidos na análise molecular foram correlacionados com o laudo histopatológico realizado nos referidos pacientes.
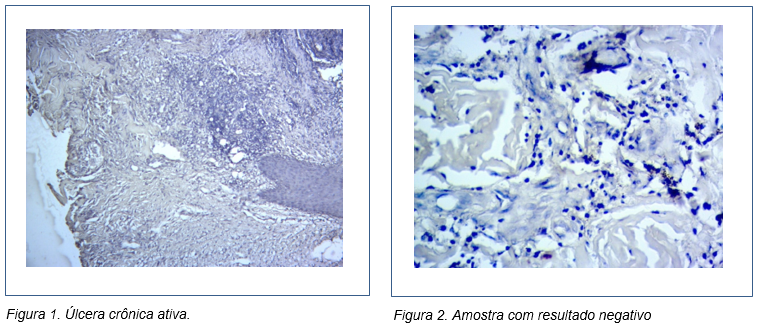
As características histopatológicas predominantes observadas nas lesões de LTA causadas por L. (V.) braziliensis foram; intensa reação inflamatória na derme com combinação de padrões de apresentação linfohistiocitária, linfoplasmocitária e granulomatosa e presença de úlceras, acantose, exocitose e espongiose na epiderme (Tabela 1).
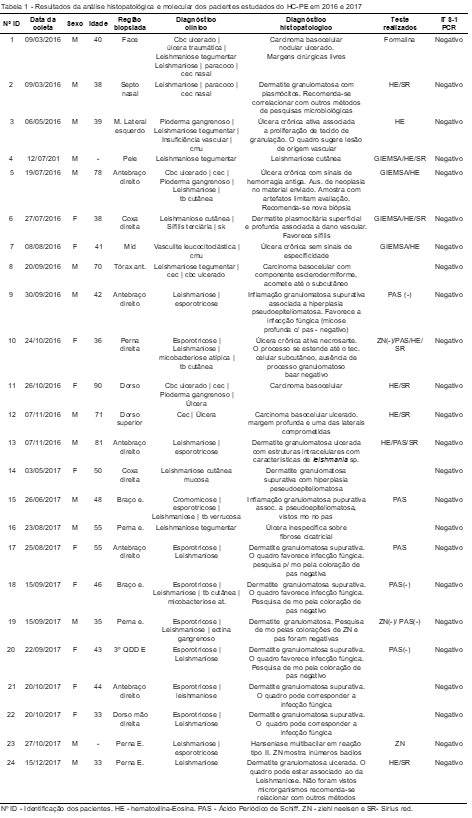
Alguns métodos de coloração não conseguiram evidenciar componentes teciduais pela técnica histológica usada no estudo.
Os cortes das lesões foram caracterizados microscopicamente com base nas alterações histológicas encontradas na epiderme e na derme. Foram avaliadas a intensidade e a distribuição das reações inflamatórias na derme, a presença de diferentes tipos celulares presentes no infiltrado, a formação de granuloma e a carga parasitária, entre outros aspectos morfológicos.
Foram evidenciados nos testes histopatológicos os seguintes achados: Dermatite granulomatosa 33,33%, úlcera crônica 20,83%, carcinoma basocelular 16,66%, Leishmaniose, Dermatite plasmocitária e Inflamação granulomatosa, 8,33% e Hanseníase 4,16%.
DISCUSSÃO
No presente estudo, dos 24 participantes com hipótese diagnóstica de LTA, 58,3% eram do sexo masculino e 41,6% do sexo feminino, corroborando com um estudo que teve predominância do sexo masculino.(5) A predominância do gênero masculino pode estar relacionada com atividades em locais de risco, como agricultura, pecuária, acampamentos e garimpo,(5-10) enquanto que as mulheres estão, em geral, menos expostas a regiões agrícolas e, na maior parte das vezes, ocupando ambientes domiciliares.(11)
A LTA no Brasil vem causando uma incidência significativa, especialmente nas áreas rurais. Isso ocorre por vários fatores como moradias próximas às bordas de florestas, ou até mesmo no seu interior. A sua gravidade aumenta devido muitas vezes à incapacidade diagnóstica, à falta de capacitação dos profissionais de saúde e ao acesso ao cuidado nas áreas rurais.(10)
Nesta pesquisa, constatou-se que a predominância da faixa etária estudada foi entre 33 a 78 anos, com mediana de idade de 76 anos, e a média de idade foi de 50,2 anos. Esses resultados diferem de outras pesquisas, nas quais foi verificada uma predominância entre as idades de 24 a 39 anos pelo pesquisador Rocha et al.,(10) e de 20 a 59 anos por Batista et al.(11)
Em relação à PCR realizada em lesões de 24 pacientes com suspeita diagnóstica de LTA, evidenciou-se que 24 amostras tiveram seus resultados negativos para LTA, e com o método histopatológico apenas uma amostra teve resultado positivo, assemelhando-se com o estudo de Tirelli et al.,(12) no Hospital Universitário, Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo (FMRP-USP), onde 437 pacientes atendidos entre 1980 e 2013 com suspeita de LTA participaram da pesquisa. Oitenta e seis (19,7%) casos com hipótese clínica inicial de LTA apresentaram um diagnóstico final diferente, revelando lesões cutâneas e mucosas. Foram solicitadas amostras de 58 (67,4%) casos para serem analisadas através do PCR, mas todas as amostras solicitadas foram negativas, não se identificando Leishmania nesses pacientes.(12)
Essa controversa entre hipótese diagnóstica e o diagnóstico final de LTA deve-se ao fato de que se trata de uma doença que apresenta lesões na pele e mucosa, podendo ser confundida com vários diagnósticos de doenças, apresentando sinais e sintomas semelhantes, especialmente doenças infecciosas e granulomatosas inflamatórias, bem como cânceres de pele não melanomas.(12)
Foram evidenciados nos testes histopatológicos Dermatite granulomatosa 33,33%, úlcera crônica 20,83%, carcinoma basocelular 16,66%, Leishmaniose, Dermatite plasmocitária e Inflamação granulomatosa 8,33% e Hanseníase 4,16%. Algumas dessas evidências estão presentes no estudo realizado por Tirelli e Roselino,(13) o qual evidenciou processos inflamatórios inespecíficos nasais (27%), etiologia neoplásica com 20% e, principalmente, carcinoma basocelular e espinocelular. Etiologia variada com 15%, incluindo úlceras.(12) Outro estudo realizado por Morgado et al.(13) evidenciou que a Hanseníase pode apresentar lesões mucosas nos pacientes com a forma clínica multibacilar da doença.(13)
Acredita-se que os números de casos notificados não traduzam a realidade de ocorrências de LTA, pois muitos pacientes demoram a procurar o sistema de saúde, sendo difícil o diagnóstico por parte do próprio sistema. Mesmo com essas falhas é evidente o aumento de casos novos e a sua intensidade ao acometer o homem.(4)
CONCLUSÃO
Leishmaniose Tegumentar Americana é uma doença que acomete o tecido do indivíduo. Diante disso, ela pode ser facilmente confundida com outras lesões de pele, especialmente doenças granulomatosas, inflamatórias e infecciosas, bem como tumores de pele. Portanto, vale salientar a importância de se diagnosticar criteriosamente cada lesão de pele, principalmente em áreas de risco para LTA, como no Nordeste do Brasil.
Apenas um caso foi positivo pelo diagnóstico histopatológico para LTA. Porém, a PCR não detectou DNA do parasito. Esse resultado divergente pode ter ocorrido devido à reação cruzada pelo método histopatológico. No entanto, a PCR é capaz de confirmar o diagnóstico de Leishmaniose Tegumentar com alto grau de sensibilidade e especificidade nos casos em que a histopatologia é compatível com o diagnóstico de Leishmaniose cutânea, não devendo ser excluído o exame histopatológico para o desfecho do diagnóstico.
Agradecimentos
Agradeço acima de tudo a Deus, à equipe do setor de Dermatologia do Hospital das Clínicas (HC-UFPE), ao Departamento de Parasitologia do IAM e a todos que contribuíram para a realização deste projeto.
Abstract
Objective: Accomplish a histopathological and molecular analysis in skin biopsy between the dermatitis lesions of patients with suspected American Cutaneous Leishmaniasis (ATL) at the Hospital of Reference of the State of Pernambuco between the period of 2016 and 2017. Methods: This is a descriptive, observational study in which all patients with clinically suggestive lesions for ATL included in the study were submitted to skin biopsy of the lesions and analyzed by the histopathological technique and PCR (Polymerase Chain Reaction). Results: Were analyzed 24 skin biopsy samples from patients with clinical suspicion of ATL, by histopathological tests and confirmation by PCR. Samples were characterized by the search of Leishmania braziliensis DNA through PCR. Of the 24 samples studied, no DNA of L. braziliensis was found. Only in one case was detected presence of Leishmania amastigotes by histopathological technique. Other microscopic findings were granulomatous dermatitis (33.33%), chronic ulcer (20.83%), basal cell carcinoma (16.66%), Leishmaniasis, plasmacytoma dermatitis and granulomatous inflammation (8.33%) and leprosy, 16%). Conclusion: The histopathological diagnosis detected a case of ATL, however, the PCR did not find DNA of the parasite. The histopathological analysis showed that the dermatotropic lesions of the patients come mainly from ulcers, skin tumors and leprosy.
Keywords
Leishmaniasis Cutaneous; Leishmania braziliensis; PCR
REFERÊNCIAS
- Furusawa GP, Magno E, Borges F. História da Medicina – colaboração para o conhecimento do histórico da leishmaniose tegumentar americana no Brasil: possíveis casos entre escravos na Vila de Vassouras-RJ, nos anos 1820 a1880. Rev Patol Trop, v. 43, n. 1, p. 7-25, 2014.
- Araújo ARD. Fatores de risco associados à leishmaniose tegumentar americana em área endêmica do estado de Pernambuco, 2014. Dissertação de Mestrado. [acesso em 19 de jun 2018] Disponível em https://repositorio.ufpe.br/handle/123456789/11467.
- De Dominicis CN, Ferreira FR, de Oliveira Rabay FM, Mandelbaum SH. Leishmaniose Tegumentar Americana: Uma Doença Polimorfa. Rev. Sociedade Portuguesa de Dermatologia e Venereologia, 2018;76(2):177-180. Acessível em; https://revista.spdv.com.pt/index. php/spdv/article/view/838
- Negrão GN, Ferreira MEMC. Considerações sobre a leishmaniose tegumentar americana e sua expansão no território brasileiro. Rev. Percurso, 2014;6(1):147-168.
- Leatte EP, Braga LDS, Rocha TN, Ciupa L, Skraba CM, Silveira TGV, Silva RCR. Aspectos epidemiológicos e laboratoriais da leishmaniose tegumentar americana em uma região endêmica do sul do brasil. Revista Uningá Review, 2014;19(1). Disponível em: <http://revista.uninga.br/index.php/uningareviews/article/view/1529.
- Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância das Doenças Transmissíveis. Manual de vigilância da leishmaniose tegumentar. Ministério da Saúde, 2017.
- Garbin CAS, de Melo Belila N, Precinoti IB, Miyada S, Garbin AJÍ, Martins RJ. Abordagem multiprofissional no diagnóstico de leishmaniose: um relato de caso. Archives of Health Investigation. 2017;6(8):359-362 . DOI: http://dx.doi.org/10.21270/archi.v6i8.2090.
- Vasconcelos PP, Rocha FJS, De Araújo NJ. Ocorrência e comportamento sociodemográfico de pacientes com leishmaniose tegumentar americana em Vicência, Pernambuco, no período de 2007 a 2014. Semina: Ciências Biológicas e da Saúde, 2017; 38 (1):105-114. DOI: 10.5433/1679-0367.2017v38n1p105.
- Gontijo B, Carvalho MLR. Leishmaniose tegumentar americana. Rev. Soc. Bras. Med. Trop. [Internet]. 2003 Jan;36(1):71-80. Acessível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid =S0037-86822003000100011&lng=en&nrm=iso
- Rocha TJM, Barbosa ACA, Santana EPC, Calheiros CML. Aspectos epidemiológicos de casos humanos confirmados de leishmaniosis tegumentaria americana en el Estado de Alagoas, Brasil. Rev Pan-Amaz Saude v.6 n.4 Ananindeua dez. 2015 [Internet]. 2015 Dez [citado 2018 Jun 20];6(4):49-54. Disponível em:< http://scielo.iec.gov.br/scielo.php?script=sci_arttext&pid=S2176-62232015000400007 &lng=pt.
- Batista FMA, Machado FFOA, Silva JMO, Mittmann J, Barja PR, Simioni AR. Leishmaniose: perfil epidemiológico dos casos notificados no estado do Piauí entre 2007 e 2011. Revista Univap. 2014;20(35):44-55. DOI: http://dx.doi.org/10.18066/revunivap. v20i35.180
- Tirelli F, Vernal S, Roselino AM. Final diagnosis of 86 cases included in differential diagnosis of American tegumentary leishmaniasis in a Brazilian sample: a retrospective cross-sectional study. An. Bras. Dermatol. [online], 2017;92(5):642-648. Acessível em: http://dx.doi.org/10.1590/abd1806-4841.20175794.
- Morgado de Abreu MA, Roselino AM, Enokihara M, Nonogaki S, Prestes-Carneiro LE, Weckx LL, et al. Mycobacterium leprae is identified in the oral mucosa from paucibacillary and multibacillary leprosy patients. Clin Microbiol Infect. 2014 Jan;20(1):59-64. doi: 10.1111/1469-0691.12190.
Correspondência
Maria Auzenir de Anastácio e Silva
Av. Prof. Moraes Rego, 1235 – Cidade Universitária
50670-901 – Recife-PE, Brasil
