Interferências laboratoriais: Principais fármacos que alteram o perfil glicêmico
Laboratory interferences: Main drugs that alter the glycemic profile
Carlena Sinara Martins da Silva1, Geane Borba Althaus2
1 Doutora em Biotecnologia/ Centro Universitário da Amazônia – UNAMA – (Docente). Santarém, PA, Brasil.
2 Bacharel em Biomedicina / Centro Universitário da Amazônia – UNAMA. Santarém, PA, Brasil.
Recebido em 04/07/2020
Aprovado em 15/03/2022
DOI: 10.21877/2448-3877.202202034
INTRODUÇÃO
O laboratório de análises clínicas tem por finalidade realizar exames laboratoriais, avaliando as condições fisiológicas do organismo de cada indivíduo, possibilitando definir a patologia mediante os resultados encontrados.(1) Os laboratórios seguem normas e/ou recomendações que visam diminuir erros ou mesmo evitá-los. Portanto, é necessário que o profissional da saúde tenha consciência desses procedimentos e evite possíveis erros para não influenciar diretamente no diagnóstico por meio de resultados falsos positivos e/ou falsos negativos.(2)
A orientação ao paciente minimiza esses erros, pois a coleta das amostras biológicas é o primeiro passo para um resultado de qualidade.(3) Esta fase, conhecida como pré-analítica, inicia com o cadastro dos pacientes onde são coletadas suas informações e repassadas orientações sobre procedimentos necessários para a realização da coleta, centrifugação e distribuição das amostras aos setores. Sendo assim, esta fase compreende todas as atividades feitas antes da realização do exame.(4)
Um fator importante na hora da coleta de dados do paciente é sobre o uso de fármacos, pois este aumenta a probabilidade de erros laboratoriais. A Sociedade Brasileira de Patologia Clínica/Medicina Laboratorial – SBPC(5) destaca que as interferências podem ocorrer por duas ações de medicamentos: interferências in vivo e in vitro. A primeira ocorre quando o medicamento é capaz de provocar uma alteração que se expressa na modificação do resultado e a outra interferência acontece quando o uso do fármaco é capaz de produzir alterações na amostra coletada, gerando resultados que não se correlacionam com a clínica do paciente.
Diante do fato, o presente estudo teve como objetivo investigar interferências laboratoriais de medicamentos que alteram o perfil glicêmico, visto que estes podem afetar os resultados dos exames laboratoriais, gerando diagnósticos equivocados.
MATERIAL E MÉTODOS
Trata-se de um estudo descritivo, quantitativo, usando informações retrospectivas, uma avaliação documental. O estudo foi realizado em um laboratório de análises clínicas no município de Santarém – PA. A técnica de coleta de dados foi a partir cadastros e histórico dos pacientes, através de sistema informatizado, tendo como base o mês de julho de 2018.
Foram avaliados 457 cadastros e os nomes dos pacientes foram mantidos em sigilo. A pesquisa contempla os preceitos éticos relacionados aos seres humanos, cujo Projeto está aprovado pelo Comitê de Ética em Pesquisa do Instituto Campinense de Ensino Superior – (CEP/ICES UNAMA Belém) nº 3.318.610.
RESULTADOS E DISCUSSÕES
Dentre os 457 cadastros, 355 foram excluídos por não apresentarem informações cadastrais completas, como a ausência da identificação dos fármacos em uso e ausência do uso de fármacos (Tabela 1).
Das 102 fichas analisadas que estavam aptas a continuarem na pesquisa, 38 eram do sexo masculino e 64 do sexo feminino (Tabela 2).
O resultado das alterações dos testes glicêmicos indicou que das 64 pacientes do sexo feminino, 37,5% apresentaram resultados alterados para glicemia. Enquanto os pacientes do sexo masculino apontaram igualdade quanto ao número de pacientes alterados e não alterados (Figura 1).
Tabela 1
Relação da porcentagem de pacientes em relação aos critérios de exclusão.
| Critério de exclusão | Quantidade | Porcentagem (%) |
| Uso de fármacos sem identificação | 60 | 16,90 |
| Sem fármacos | 295 | 83,10 |
| Total | 355 | 100 |
Tabela 2
Relação da porcentagem de pacientes em relação ao sexo.
| Gênero | Quantidade | Porcentagem (%) |
| Masculino | 38 | 37,25 |
| Feminino | 64 | 62,75 |
| Total | 102 | 100 |
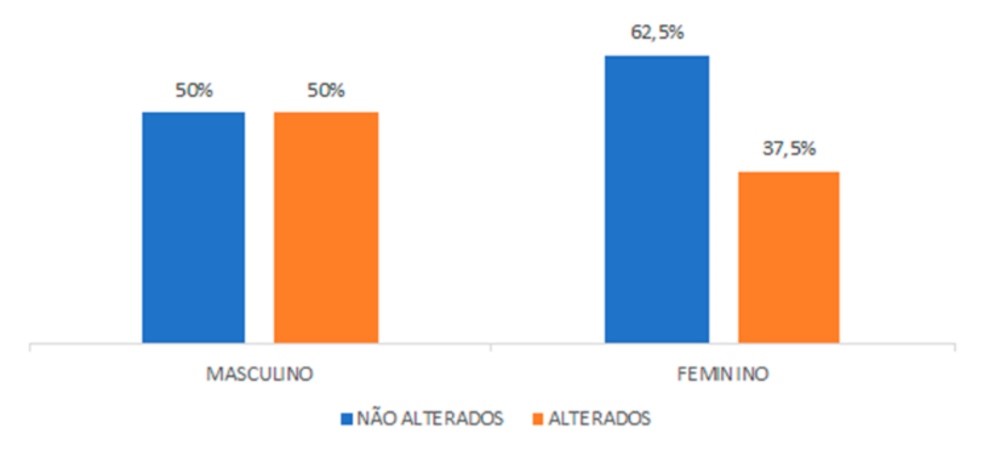
Figura 1
Alteração dos testes glicêmicos de acordo com o gênero.
A Tabela 3 mostra a distribuição das idades por faixa etária e a quantidade de fármacos utilizados por todos os pacientes, comprovando que a maioria dos pacientes faz uso de vários medicamentos. Entre as pessoas com diagnóstico de doenças crônicas, a terapia com mais de uma classe de fármacos foi necessária, ocasionando a polimedicação. Esta é definida como uso simultâneo de mais de cinco medicamentos utilizados por mais de três meses, ocorrendo em maior número nos idosos. […] sendo a população que mais consome medicamentos.(5)
Um total de 53 medicamentos diferentes foram identificados nos arquivos dos pacientes, sendo que alguns destes foram relatados por mais de um paciente ou foi relatado o uso de mais de um fármaco por paciente (Figura 2).
Dentre os 53 medicamentos utilizados pelos pacientes, foram selecionados os cinco mais utilizados e que possivelmente estão associados às alterações da glicemia, são eles: losartana, metformina, captopril, hidroclorotiazida e rosuvastatina. A Tabela 4 mostra a relação dos medicamentos com a quantidade de pacientes.
Foi observado que a maioria dos pacientes apresentava problemas relacionados à pressão arterial, justificando o uso de anti-hipertensivo, sendo os mais utilizados a losartana e o captopril. A losartana foi utilizada por 31,82% dos pacientes, um bloqueador do receptor de angiotensina II, um não-peptídico do receptor desta enzima para o tratamento de hipertensão.(7) Já o captopril, utilizado por 13,63% dos pacientes, um potente inibidor da enzima conversora de angiotensina (IECA) na qual impede a conversão de angiotensina I em angiotensina II, sendo o primeiro a ser introduzido no tratamento terapêutico.(8)
O uso da metformina, uma biguanida, disponibilizada pelo Sistema Único de Saúde (SUS), seguiu como segundo fármaco mais utilizado pelos pacientes (22,73%). O mecanismo de ação das biguanidas pode ocorrer por captação direta da glicose na musculatura esquelética, com a diminuição da gliconeogênese hepática e renal, a redução do nível de glicemia, de LDL e VLDL, redução de absorção de glicose pelo trato gastrointestinal, e ainda aumento da conversão da glicose em lactato pelos enterócitos e a diminuição nos níveis de glucagon.(9) A metformina pode fasear o aparecimento de cetona urinária, assim como reduzir as concentrações de colesterol e dos triglicerídeos em exames laboratoriais.(10)
Os diuréticos tiazídicos, como é o caso da hidroclorotiazida, utilizados por 18,18% dos pacientes, podem causar um aumento nas dosagens de glicose e cálcio no sangue provocado por efeito fisiológico, assim como a diminuição nos valores de potássio e sódio.(10)
A rosuvastatina, usada por 13,63% dos pacientes, pode inibir a enzima HMG-CoA redutase, que é importante na fabricação do colesterol pelo organismo reduzindo os níveis de lipídios no sangue, principalmente o colesterol e os triglicérides.(11)
Os medicamentos que ocasionaram alterações no perfil glicêmico dos pacientes foram a metformina (hipoglicemiante) e a hidroclorotiazida e rosuvastatina (aumento dos níveis glicêmicos).
Tabela 3
Distribuição das idades por faixa etária dos pacientes e quantidades de fármacos utilizados, com suas respectivas porcentagens.
| Faixa etária | Quantidade de paciente | Quantidade de fármacos | Média de medicamento por paciente |
| 21 a 30 | 7 | 8 | 1,14 |
| 31 a 40 | 21 | 31 | 1,48 |
| 41 a 50 | 24 | 40 | 1,67 |
| 51 a 60 | 24 | 56 | 2,33 |
| 61 a 70 | 16 | 31 | 1,94 |
| 71 a 80 | 10 | 24 | 2,40 |
| Total | 102 | 190 | 1,86 |
Tabela 4
Medicamentos mais utilizados pelos pacientes em relação a quantidade de pacientes.
| Medicamentos | Nº de pacientes | Porcentagem (%) |
| Losartana | 7 | 31,82 |
| Metformina | 5 | 22,73 |
| Hidroclorotiazida | 4 | 18,18 |
| Captopril | 3 | 13,63 |
| Rosuvastatina | 3 | 13,63 |
| Total | 22 | 100 |
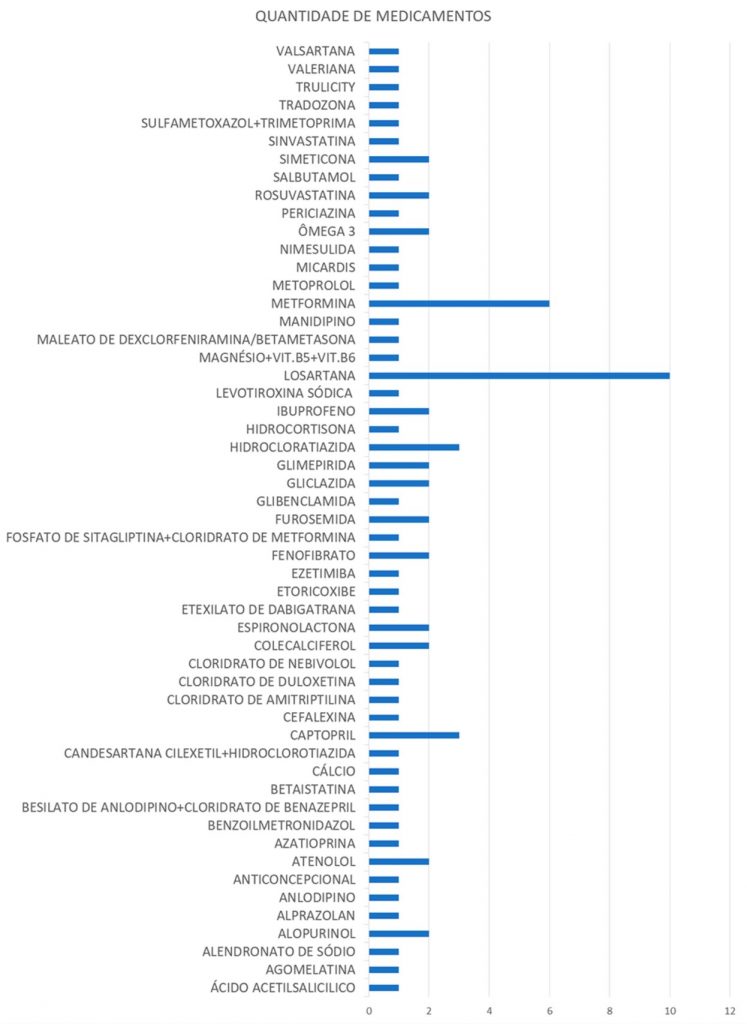
Figura 2
Medicamentos utilizados pelos pacientes
CONCLUSÃO
Neste estudo, observamos que três medicamentos interferiram no exame de glicemia. A disseminação de conhecimentos a respeito das interferências que os medicamentos causam em exames laboratoriais é essencial para auxiliar na conduta médica da escolha terapêutica e monitoramento do paciente. A fase pré-analítica incorreta pode ocasionar complicações futuras na saúde do paciente, provocando alterações em exames laboratoriais em decorrência de efeitos adversos. Dessa forma, este levantamento é de grande relevância por promover a divulgação de informações para os profissionais da área da saúde.
REFERÊNCIAS
- Souza ABS; Barbosa EC; Rocha TRF; Fernandes T da PB. Importância e vantagens do interfaceamento em laboratório de análises clínicas. Revista Multidisciplinar em Saúde, [S. l.], v. 1, n. 3, p. 26, 2020. Disponível em: https://editoraime.com.br/revistas/index.php/rems/article/view/370. Acesso em: 9 mar. 2023.
- Souza RKL.; Coan EW; Anghebem MI. Não conformidades na fase pré-analítica identificadas em um laboratório de saúde pública. Jornal Brasileiro de Patologia e Medicina Laboratorial, v. 56, 2020.
- Steckert C; Silva AP da. Aplicabilidade de ferramentas da qualidade no controle de falhas do laboratório clínico. Inova Saúde, v. 9, n. 1, p. 115-128, 2019.
- Teixeira JCC; Chicote SRM; Daneze ER. Não conformidades identificadas durante as fases pré-analítica, analítica e pós-analítica de um laboratório público de análises clínicas. Nucleus, v. 13, n. 1, p. 251-60, 2016.
- SOCIEDADE BRASILEIRA DE PATOLOGIA CLÍNICA/MEDICINA LABORATORIAL (SBPC/ML). Recomendações da Sociedade Brasileira de Patologia Clínica/Medicina Coleta e preparo da amostra biológica. São Paulo, 2013.
- Pereira KG et al. Polifarmácia em idosos: um estudo de base populacional. Revista Brasileira de Epidemiologia, v. 20, p. 335-344, 2017.
- Costa JJ de L; Abreu TP de. Efeitos da terapia combinada de losartana com hidroclorotiazida em pacientes do programa farmácia popular. Revista Ibero-Americana de Humanidades, Ciências e Educação, [S. l.], v. 7, n. 10, p. 1266–1275, 2021. DOI: 10.51891/rease.v7i10.2660. Disponível em: https://www.periodicorease.pro.br/rease/article/view/2660. Acesso em: 9 mar. 2023.
- Dias KGM et al. Viabilidade do captopril sublingual em crises hipertensivas. Revista Ensaios Pioneiros, v. 4, n. 1, p. 34-40, 2020.
- Lopes VP; Júnior MCS; Júnior AFS; Santana AIC. Farmacologia do diabetes mellitus tipo 2: antidiabéticos orais, insulina e inovações terapêuticas. Revista Eletrônica de Farmácia, v. 9, n. 4, p. 69-90, 2012
- Golan DE; Junior T; Armen H; Armstrong EJ; Armstrong AW. Princípios de Farmacologia: A base fisiopatológica da farmacoterapia. 3ª edição. Rio de Janeiro: Guanabara Koogan, 2014.
- Silva MF do N et al. Impacto do contraste farmacocinético dos inibidores da HMG-CoA redutase: comunicação breve. Revista de Casos e Consultoria, v. 11, n. 1, p. e11116-e11116, 2020.
Correspondência
Carlena Sinara Martins da Silva
E-mail: [email protected]
