Inclusões semelhantes aos corpúsculos de Russell em blastos mieloides
Inclusions similar to Russell bodies in myeloblasts
João Thomas Schmidt Mello1
Maria Carla Dania Barbosa2
Julia Poeta1
Carine Ghem3
1Biomédico (a). Centro Universitário Ritter dos Reis, Porto Alegre-RS, Brasil.
2Farmacêutica-Bioquímica. Serviço de Diagnóstico Laboratorial, Hospital de Clínicas de Porto Alegre (HCPA), Porto Alegre-RS, Brasil.
3Biomédica. Serviço de Diagnóstico Laboratorial, Hospital de Clínicas de Porto Alegre (HCPA), Porto Alegre-RS, Brasil.
Instituição: Serviço de Diagnóstico Laboratorial, Hospital de Clínicas de Porto Alegre (HCPA). UniRitter – Centro Universitário Ritter dos Reis, Porto Alegre-RS, Brasil.
Recebido em 09/09/2019
Artigo aprovado em 12/12/2019
DOI: 10.21877/2448-3877.201900909
INTRODUÇÃO
A leucemia mieloide aguda (LMA) é uma neoplasia hematológica caracterizada pela expansão clonal de células progenitoras hematopoiéticas, que têm como consequência a proliferação de células mieloides imaturas, com prejuízo da hematopoese normal, levando a infecções severas, anemia e hemorragia.(1)
A LMA pode ocorrer em qualquer faixa etária, sendo uma doença predominante em pessoas idosas, com média de idade ao diagnóstico de 68 anos.(2) A sua patogênese está associada a alterações genéticas e moleculares, sendo descritas diferentes translocações cromossômicas e mutações gênicas que estão envolvidas com alterações no mecanismo de proliferação celular, como é o caso das mutações incluindo os genes PML, RUNX1, CBFB, TET2, FLT3, dentre outros.(3)
A mutação do gene FLT3 (FMS-like tyrosina kinase) é uma das mais comuns alterações genômicas na LMA, identificada em aproximadamente 1/3 dos pacientes. O gene FLT3 está localizado no cromossomo 13q12, e codifica um receptor com atividade tirosina quinase altamente expresso em células progenitoras hematopoiéticas. Esse receptor está associado à sinalização nas vias de apoptose, proliferação celular e diferenciação das células na medula óssea, e o seu mau funcionamento provoca descontrole na produção hematopoiética e imaturidade celular.(4,5)
Alterações nos mecanismos celulares também podem ser evidenciadas pela presença dos corpúsculos de Russell, que são inclusões intracitoplasmática basofílicas. Estas inclusões ocorrem devido a uma indigestão celular de proteínas e podem ser observadas em diversas condições patológicas como: leucemias, mieloma múltiplo, linfoma de Burkitt e gastrite com corpúsculos de Russell, sendo mais raras de serem observadas nas leucemias mieloides agudas.(6) As possíveis causas destas alterações intracelulares são a falha na degradação de proteínas no retículo endoplasmático, mutação em uma imunoglobulina da classe G, que não pode ser degradada pelas proteases, ou falha no transporte para a degradação.(7)
Os corpúsculos de Russel representam morfologicamente a cisterna do retículo endoplasmático dilatado contendo imunoglobulinas condensadas, geralmente uma imunoglobulina mutada que não é secretada ou não é degradada. Originalmente foram descritos nas células plasmáticas, porém têm sido encontrados em diferentes tipos celulares.(7)
O presente estudo tem como objetivo relatar a presença de inclusões citoplasmáticas semelhantes aos corpúsculos de Russell em blastos de esfregaço de sangue periférico em uma paciente com LMA. Este estudo obteve aprovação no Comitê de Ética em Pesquisa do Hospital de Clínicas de Porto Alegre sob o número 2018-08-24, e a paciente assinou o termo de consentimento livre e esclarecido.
RELATO DE CASO
Paciente do sexo feminino, 51 anos de idade, com diagnóstico prévio de LMA, apresentou recaída medular da doença dois anos após o diagnóstico. No hemograma foram observados: eritrócitos: 2,55 milhões/uL; hemoglobina: 7,3 g/dL; hematócrito: 21,5%; VCM: 84,3fL; HCM: 28,6 pg e leucócitos totais: 19,38 x103/uL, com presença de 95% de blastos no esfregaço de sangue periférico. Na análise do esfregaço sanguíneo foram observados blastos com inclusões intracitoplasmáticas basofílicas, muito similares aos corpúsculos de Russell (Figura 1). A paciente apresentou cariótipo normal, com presença de mutação do gene FLT3.
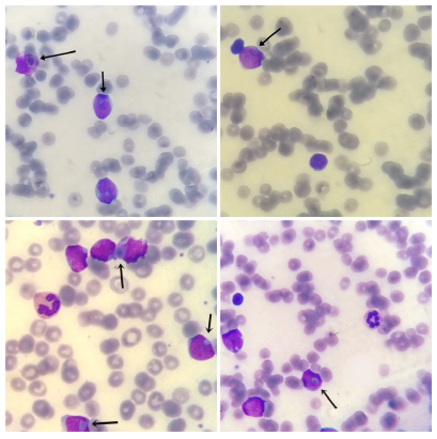 Fig.1. Blastos com inclusões citoplasmáticas semelhantes a corpúsculos de Russell.
Fig.1. Blastos com inclusões citoplasmáticas semelhantes a corpúsculos de Russell.
O estudo imunofenotípico da população total de células identificou 87% de células mieloides imaturas, positivas para cMPO fraco e heterogêneo, CD33 fraco e CD45 fraco, destas 25% expressam CD117 fraco. Ausência de CD35, HLA-DR e CD15, sendo esse imunofenótipo sugestivo de LMA.
O medulograma apresentou medula hipercelular com a hematopoiese normal substituída por infiltração de 90% de blastos com aspecto mieloide. A paciente iniciou protocolo quimioterápico e entrou em remissão morfológica. Não foi realizado o Transplante de Células-Tronco Hematopoiéticas devido ao alto risco de morte.
DISCUSSÃO
Os achados morfológicos no esfregaço de sangue periférico, mielograma e a imunofenotipagem por citometria de fluxo são utilizados em conjunto para confirmar o diagnóstico da LMA. A análise citogenética e o screening para mutações genéticas também auxiliam no diagnóstico e prognóstico do paciente, sendo que a mutação do gene FLT3 é um alvo importante para o desenvolvimento de terapias para o tratamento da LMA e outras formas de leucemia. Entender os mecanismos pelos quais cada mutação interage com os mecanismos celulares pode auxiliar no diagnóstico e prognóstico do paciente.
O presente relato demonstrou a presença de inclusões morfologicamente semelhantes aos corpúsculos de Russell em blastos de uma paciente com LMA. Acredita-se que a hiperestimulação antigênica na leucemia, provocada pelas inflamações ou pela invasão de agentes patológicos, possa resultar em disfunções de armazenamento de proteínas no retículo endoplasmático, não só em plasmócitos mas também em blastos.(8,9) No entanto, não foi evidenciada a presença de processo inflamatório ou infeccioso ativo nesta paciente, uma vez que estes quadros poderiam estar associados a depósitos intracelulares e, desta forma, contribuir para a formação das inclusões observadas.
Bunting & Lew demonstraram a presença de inclusões semelhantes aos corpúsculos de Russel em um caso de leucemia linfoblástica, porém os exames de imunohistoquímica foram negativos para IgM e cadeias leves Kappa e Lambda, demonstrando que o material condensado não era constituído por imunoglobulinas, como ocorre na formação dos corpúsculos de Russell. As inclusões eram compostas de material granular e fibrilar, demonstrando que distúrbios fisiológicos são capazes de causar disfunções de armazenamento intracelular em blastos.(10)
No presente relato de caso não foi possível a realização de exames de imunohistoquímica para avaliar a composição das inclusões observadas, e não está claro o papel desempenhado por esse achado incomum na morfologia dos blastos para o diagnóstico e prognóstico da LMA, bem como se existe uma associação da mutação do gene FLT3 com a presença dos corpúsculos de Russel, uma vez que essa mutação é a causa de alterações de mecanismos celulares. O conhecimento das características bioquímicas e consequências fisiológicas dos corpúsculos de Russell ainda permanecem obscuras, sendo necessários estudos adicionais para avaliar o seu real valor prognóstico.
Abstract
Changes in cell mechanisms result in the appearance of Russel bodies, which are basophilic intracytoplasmic inclusions. These inclusions occur due to cellular indigestion of proteins, and can be observed in several pathological conditions such as leukemias, multiple myeloma, Burkitt’s lymphoma, and gastritis with Russell bodies, but rarely observed in acute myeloid leukemias. The present study reports the presence of inclusions similar to Russell bodies in peripheral blood blasts in a 51-year-old female patient with acute myeloid leukemia.
Keywords
Myeloide Leukemia; hematology; inclusion bodies
REFERÊNCIAS
- Short NJ, Rytting ME, Cortes JE. Acute myeloid leukaemia. Lancet. 2018 Aug 18;392(10147):593-606. doi: 10.1016/S0140-6736 (18) 31041-9.
- McNerney ME, Godley LA, Le Beau MM. Therapy-related myeloid neoplasms: when genetics and environment collide. Nat Rev Cancer. 2017;17(9):513-27. doi: 10.1038/nrc.2017.60.
- Goldman SL, Hassan C, Khunte M, Soldatenko A, Jong Y, Afshinnekoo E, et al. Epigenetic Modifications in Acute Myeloid Leukemia: Prognosis, Treatment, and Heterogeneity. Front Genet. 2019;10:133. doi: 10.3389/fgene.2019.00133.
- Daver N, Schlenk RF, Russell NH, Levis MJ. Targeting FLT3 mutations in AML: review of current knowledge and evidence. Leukemia. 2019;33(2):299-312. doi: 10.1038/s41375-018-0357-9.
- Short NJ, Kantarjian H, Ravandi F, Daver N. Emerging treatment paradigms with FLT3 inhibitors in acute myeloid leukemia. Ther Adv Hematol. 2019;10:2040620719827310.
- Yorita K, Iwasaki T, Uchita K, Kuroda N, Kojima K, Iwamura S, et al. Russell body gastritis with Dutcher bodies evaluated using magnification endoscopy. World J Gastrointest Endosc. 2017; 9(8):417-24. doi: 10.4253/wjge.v9.i8.417.
- Kopito RR, Sitia R. Aggresomes and Russell bodies. Symptoms of cellular indigestion? EMBO Rep. 2000;1(3):225-31. DOI: 10.1093/embo-reports/kvd052.
- Mossuto MF, Ami D, Anelli T, Fagioli C, Doglia SM, Sitia R. Biochemical nature of Russell Bodies. Sci Rep. 2015;5:12585. https://doi.org/10.1038/srep12585
- Mattioli L, Anelli T, Fagioli C, Tacchetti C, Sitia R, Valetti C. ER storage diseases: a role for ERGIC-53 in controlling the formation and shape of Russell bodies. J Cell Sci. 2006;119(Pt 12):2532-41.
- Bunting ST, Lew G. “Russell-like” bodies in Philadelphia chromosome-positive B-lymphoblastic leukemia. Blood. 2014;123(16):2448. doi: 10.1182/blood-2014-01-547513.
Correspondência
João Thomas Schmidt Mello
Ramiro Barcelos 2350, Bairro Santa Cecília
Porto Alegre-RS, Brasil
