Evolução clínica de indivíduos com antígeno de superfície do vírus da hepatite B reagente, atendidos em um laboratório clínico de Caxias do Sul – RS, entre os anos de 2010 a 2015
Clinical course of individuals with B hepatitis surface antigen attended in a clinical laboratory in Caxias do Sul – RS between the years of 2010 to 2015
Giulia Vailatti1
Marina Ferri Pezzini1
Caroline Pietá2
Julia Poeta4
- Graduada em Biomedicina. Centro Universitário FSG, Caxias do Sul-RS, Brasil.
- Doutora em Ciências do Movimento Humano – Universidade Federal do Rio Grande do Sul (UFRGS), Laboratório de Pesquisa do Exercício – Porto Alegre-RS, Brasil.
- Mestre em Ciências Médicas – Universidade Federal do Rio Grande do Sul (UFRGS) e professora do Curso de Biomedicina do Centro Universitário Ritter dos Reis – Porto Alegre-RS, Brasil.
Instituição: Centro Universitário Ritter dos Reis – Porto Alegre-RS, Brasil.
Recebido em 10/07/2017
Artigo aprovado em 12/04/2018
DOI: 10.21877/2448-3877.201800595
Resumo
Objetivo: A hepatite B é uma doença infecciosa que atinge, aproximadamente, 2 bilhões de pessoas. Apresenta fase aguda que pode evoluir para a cura ou cronificar. O quadro da doença é avaliado por meio de enzimas hepáticas e marcadores sorológicos, que detectam anticorpos e antígenos produzidos pelo vírus. Esse trabalho teve como objetivo avaliar os diferentes marcadores da hepatite B através de exames laboratoriais de indivíduos infectados, correlacionando testes de função hepática com a evolução da doença. Métodos: Trata-se de estudo transversal retrospectivo realizado de 2010 a 2015, utilizando banco de dados de um laboratório de Caxias do Sul-RS. As variáveis estão apresentadas em média e desvio-padrão e foram comparadas utilizando o teste t Student para amostras dependentes e as variáveis entre os grupos pelo teste t Student para amostras pareadas. Resultados: Um total de noventa indivíduos foi incluído, com média de idade de 46,0±13,5 anos (51% homens). Quanto à evolução, 31% dos pacientes evoluíram para a cura e 69% para a crônica. Encontramos significância entre as enzimas ALT e GGT, no momento do diagnóstico, com as últimas dosadas pelo laboratório (p < 0,008 e p< 0,007, respectivamente). Entre os grupos, houve diferença entre ALT (inicial e final) do grupo cura (p = 0,012), o que não ocorreu no grupo que cronificou (p= 0,848). Conclusão: O estudo pôde revelar o comportamento das transaminases e GGT frente à contaminação pelo vírus da hepatite B, ficando evidente a importância do correto acompanhamento da hepatite B através desses exames laboratoriais para se conhecer a noção real do estado da patologia.
Palavras-chave
Hepatite B; Testes de função hepática; Testes sorológicos
INTRODUÇÃO
A hepatite B é uma doença infeciosa que atinge aproximadamente 6,5 a cada 100 mil brasileiros.(1) A transmissão ocorre através do contato com sangue, sêmen ou outros fluidos corporais infectados pelo vírus da hepatite B (HBV). A doença costuma se manifestar de forma aguda e pode evoluir para a cura ou cronificação.(2)
A Organização Mundial da Saúde (OMS) estima que mais de 2 bilhões de pessoas no mundo sejam portadoras do HBV e, destas, 360 milhões possuam hepatite B crônica.(3) Apesar de ser uma doença distribuída mundialmente, a maioria dos indivíduos infectados está localizada no Sudeste Asiático e na África Central.(4,5) No Brasil, pelo menos 15% da população já esteve em contato com o HBV e 1% apresenta doença crônica relacionada ao vírus.(6) Dados do boletim epidemiológico, do ano de 2012, informam que foram notificados 120.343 casos de hepatite B no Brasil entre os anos de 1999 a 2011, sendo o maior número de casos nas regiões Sudeste (36,3%) e Sul (31,6%).(1)
A forma aguda da hepatite B apresenta um período de incubação do vírus que dura em torno de 45 dias. Esta fase pode ser assintomática ou apresentar sintomas prodrômicos pouco significativos, como cansaço, falta de apetite, náuseas e febre. No início da infecção é comum encontrar um leve aumento das transaminases séricas, ALT (alanina aminotransferase) e AST (aspartato aminotransferase). Com a evolução do quadro agudo, os sintomas prodrômicos aumentam, o paciente pode apresentar icterícia e as transaminases elevam-se consideravelmente, podendo acompanhar essa elevação os níveis de bilirrubina, fosfatase alcalina e gamaglutamiltransferase (GGT). O quadro comum de hepatite B aguda costuma perdurar em torno de seis semanas, quando os sintomas desaparecem e as provas hepáticas normalizam.(5) A cura da doença é confirmada através dos marcadores sorológicos, que detectam anticorpos produzidos em resposta à infecção com a diminuição da produção de antígenos pelo DNA viral. Nestes casos, o paciente não apresenta mais índices de antígeno de superfície para o vírus da Hepatite B (HBsAg), mas apresenta anticorpos para o vírus (Anti-HBs) e continua apresentando anticorpos contra o antígeno central do HBV (Anti-HBc total).(7-9) A recuperação espontânea é comum, logo, não são prescritos antivirais, apenas medicamentos para reduzir os sintomas, até que desapareçam.(7,10)
A forma crônica da hepatite B, no entanto, se caracteriza pela permanência do vírus no organismo por mais de seis meses após o contato inicial, sendo o diagnóstico caracterizado pela permanência do HBsAg no soro do paciente.(11) Pacientes crônicos costumam apresentar níveis altos de transaminases ao longo de toda a vida. Com isso, o objetivo do tratamento, nessa fase, é diminuir a replicação do vírus e evitar a progressão da doença, impedindo, portanto, o surgimento de cirrose ou hepatocarcinoma.(12-14)
Estudos indicam que a infecção pelo HBV evolui para a cura em 90% a 95% dos casos e para o estado de portador crônico nos restantes 5% a 10%.(4,15,16)
O método mais eficaz de prevenção da hepatite B é a vacinação. A vacina é aplicada no Brasil desde 1989, e desde 1998 faz parte do calendário de vacinação para crianças menores de 1 ano, estando disponível pelo Sistema Único de Saúde (SUS). A vacina também é ofertada para todas as pessoas até 49 anos e para indivíduos pertencentes aos grupos de risco (usuários de drogas injetáveis, trabalhadores do sexo e trabalhadores da saúde). Estima-se que 75% da população menor de 29 anos seja vacinada.(17,18)
De acordo com os dados representativos do Sul do Brasil, buscou-se avaliar os diferentes marcadores solicitados para o HBV e correlacionar com os testes de função hepática e com a evolução da doença, por meio da pesquisa em banco de dados de um laboratório da cidade de Caxias do Sul/RS.
MATERIAL E MÉTODOS
Estudo transversal, retrospectivo, realizado no período de janeiro de 2010 a julho de 2015, utilizando banco de dados de um laboratório de referência na cidade de Caxias do Sul-RS.
Foram incluídos no estudo todos os pacientes com idade maior ou igual a 18 anos que foram diagnosticados com hepatite B através do marcador HBsAg reagente, e fizeram acompanhamento do quadro por meio dos demais marcadores sorológicos para o HBV, além de enzimas hepáticas, no mesmo laboratório. Como critério de exclusão, os prontuários cujos indivíduos não realizaram o acompanhamento completo, que já haviam sido diagnosticados anteriormente ou que o intervalo entre o primeiro e o último exame foi menor ou igual a seis meses.
Para expressar a evolução do paciente foram coletados dados dos exames realizados no momento do diagnóstico, indicando a fase aguda da doença e o último exame realizado até a data final da coleta dos dados. Após a análise dos dados, os pacientes foram divididos em dois grupos: grupo da cura, aqueles que não apresentavam mais HBsAg reagente e apresentavam anti-HBs reagente; e, como grupo crônico, os indivíduos que ainda apresentavam HBsAg reagentes por mais de seis meses. Os dados foram coletados por conveniência utilizando-se o programa de dados do próprio laboratório e armazenados no Microsoft Excel 2010.
As variáveis analisadas foram: idade, sexo, resultados dos marcadores sorológicos (HBsAg, HBeAg, Anti-HBc-total, Anti-HBe e Anti-HBs), resultados dos testes de função hepáticas (ALT, AST e GGT) e evolução clínica da patologia (estado crônico ou cura).
Os dados foram avaliados estatisticamente utilizando-se o software SPSS versão 20.0. As variáveis quantitativas contínuas com distribuição normal foram apresentadas descritivamente em média e desvio-padrão. As variáveis foram comparadas entre grupos utilizando-se o teste t de Student para amostras dependentes, e as diferenças entre as variáveis entre os grupos de evolução da doença foram analisadas pelo teste t de Student para amostras pareadas, com nível de significância p<0,05. A normalidade das variáveis foi avaliada pelo teste de Shapiro-Wilk.
O projeto foi aprovado pelo Comitê de Ética em Pesquisa da Faculdade da Serra Gaúcha (Parecer: 1.235.513).
RESULTADOS
Foram analisados 42.860 resultados de HBsAg entre os anos de 2010 a 2015. Destes, 850 apresentaram resultados reagentes: sete foram excluídos por se tratar de indivíduos com idade inferior a 18 anos, 348 resultados por falta de acompanhamento clínico e 225 por referir-se a pacientes com história prévia da doença, resultando em 270 resultados de HBsAg, correspondendo a 90 pacientes. A média de idade da população estudada foi de 46,0 ± 13,5 anos (IC: 18 a 78 anos) sendo 51% homens.
Quando analisados os marcadores realizados no momento do diagnóstico, observou-se que 15,6% dos pacientes apresentavam Anti-HBc total reagente, e, com o decorrer do acompanhamento clínico, esse valor aumentou para 32,2%. A porcentagem de pacientes que apresentavam HBeAg reagente no início do acompanhamento era de 5,6%, e, com o transcorrer do tempo, diminuiu para 2,2% (Tabela 1).

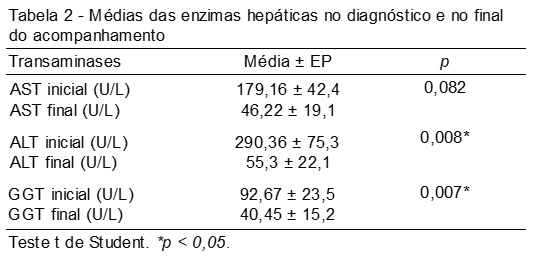
Encontramos significância estatística entre as enzimas hepáticas ALT e GGT, no momento do diagnóstico, com as últimas dosadas pelo laboratório, classificadas como “iniciais” e “finais” com p < 0,008 e p< 0,007, respectivamente. Não houve relação significativa entre as dosagens de AST (p = 0,082). As variáveis estão apresentadas na Tabela 2.
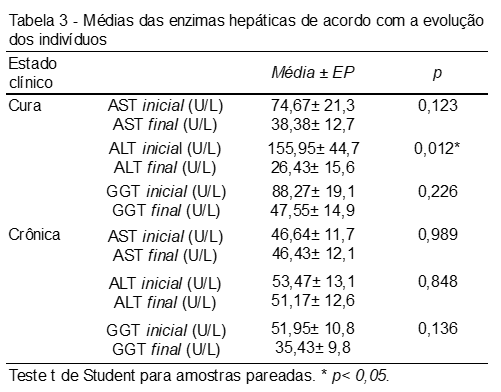
A Tabela 3 aponta a média das enzimas hepáticas relacionadas com a evolução da doença. Houve diferença estatística entre as ALT (inicial e final) do grupo de cura da doença (p = 0,012), o que não ocorreu, no entanto, no grupo da fase crônica (p =0,848). Na análise das demais enzimas, AST e GGT, não houve significância entre os grupos estudados.
Observou-se que 31% dos pacientes que fizeram o acompanhamento completo evoluíram para cura e, em contrapartida, 69% para a fase crônica da doença. Como o esperado, todos os pacientes que evoluíram para a cura apresentaram Anti-HBs reagente.
DISCUSSÃO
Pesquisas apontam que a maioria dos pacientes infectados pelo HBV evolui espontaneamente para a cura e em torno de 10% acabam desenvolvendo a forma crônica.(4,19) Entretanto, neste estudo, a maioria dos pacientes acompanhados (69%) desenvolveu a forma crônica. Acredita-se então que essa condição se deve em alguns casos, onde a hepatite B evolui através de sintomas pouco característicos e leves, não dando indícios suficientes para os pacientes procurarem ajuda médica especializada.(20)
Estudos realizados em São Paulo(21) e Santa Catarina(22) encontraram maior prevalência de hepatite B em homens com idade entre 30 a 39 anos, dados que estão de acordo com esta pesquisa, onde o limite superior de idade foi um pouco maior (59 anos). Estudos realizados na China(19) e em São Paulo(23) indicam uma diminuição no número de crianças e adolescentes infectados pelo HBV, resultante do fácil acesso a vacinação. Como a vacina é aplicada no Brasil desde 1989,(18) sua eficácia também pode ser demonstrada em nosso estudo, já que nossa população é formada principalmente por adultos acima de 30 anos.
Os resultados dos marcadores sorológicos utilizados estão compatíveis com a literatura.(24,25) O HBeAg é um marcador de replicação viral que costuma negativar quando a doença encontra-se em faze estacionária, elevando os níveis do seu anticorpo, o Anti-HBe. Nossos resultados demostram que houve uma diminuição de indivíduos HBeAg reagentes quando comparados com o início e com o final do acompanhamento, resultando na redução na taxa de replicação viral. Os valores de Anti-HBe não tiveram mudança significante quando comparados o início e o final do acompanhamento. Os dados do Anti-HBc total também estão correspondendo com as expectativas, este que é um marcador de contato com o HBV. Encontramos elevação nos níveis de Anti-HBc total em comparação com o início e o fim do acompanhamento, sugerindo o aparecimento desse marcador com o passar do tempo, já que o mesmo costuma ser detectado entre 4 a 10 semanas após o contato com o vírus. Conforme era previsto, todos os pacientes que evoluíram para a cura apresentaram Anti-HBs reagente já que este é um marcador de resposta imunológica à infecção.
Encontramos relação significativa entre ALT inicial e final e GGT inicial e final, quando comparados os resultados das médias das enzimas hepáticas do primeiro e do último exame realizado, contudo não foi encontrada significância entre os resultados de AST. Isso ocorre pelo fato da ALT ser hepatoespecífica, considerada a melhor enzima para determinação de lesões hepáticas, e a GGT estar presente nas vias biliares e fígado, enquanto a AST pode ser utilizada como marcador também para dados cardíacos ou musculares, não sendo específica do fígado.(26)
Quando comparadas às médias das enzimas hepáticas com a evolução clínica dos pacientes encontramos significância estatística ao relacionar ALT inicial e final do grupo da cura. Este dado está de acordo com a literatura, uma vez que ocorre um aumento significativo da enzima na fase aguda da doença e, consequentemente, uma diminuição quando o paciente está recuperado.(5) O mesmo não foi observado com ALT do grupo da fase crônica porque o valor da transaminase permaneceu dentro da mesma média, indicando estabilidade na atividade das enzimas, o que é esperado em pacientes crônicos para hepatite B. Apesar de não termos encontrado significância quando analisamos as médias de GGT, um estudo realizado em 2014(9) demonstrou que esta enzima pode ser utilizada para monitorar o dano hepático principalmente em pacientes com hepatite B, elevando sua atividade conforme o grau da lesão.
CONCLUSÃO
O estudo pôde revelar o comportamento das transaminases e GGT frente à contaminação pelo vírus da hepatite B. Os dados demonstraram que os pacientes acometidos pela infecção aguda, neste estudo representados pelo primeiro exame realizado, apresentaram grau de disfunção hepática considerável em relação aos pacientes que evoluíram para fase crônica. Apesar de a literatura indicar que a maioria dos pacientes evolui para a cura da hepatite B, isto não foi observado quando analisamos resultados da população de um laboratório clínico; dessa maneira, pode ser relacionado à falta de sintomas característicos da patologia. Por isso enfatiza-se a importância de testes para doenças sexualmente transmissíveis como parte da rotina normal de exames para auxiliar no diagnóstico precoce de hepatite B, além da realização da vacina como melhor forma de prevenção.
Os dados descritos são de prontuários de um laboratório da região; assim, necessita-se de uma ampliação da amostra estudada, além de outras causas de disfunção hepática e do acompanhamento médico para que se tenha uma verdadeira noção do quadro desses pacientes. Muito embora restritos, os dados apresentados têm grande relevância, pois ressaltam a importância do acompanhamento da evolução do HBV, utilizando todos os marcadores sorológicos juntamente com as provas de função hepática.
Abstract
Objective: B hepatitis is an infectious disease affects, proximally, 2 billion people. This disease has an acute phase that can progress to cure or chronic course. The clinical course of the disease is value by liver enzymes and biological markers that detect antibodies and antigens produced by virus. The aim of this study was evaluate different markers of hepatitis B through laboratory tests of infected individuals, correlating the liver function tests in order to make an analysis of the evolution of the disease. Methods: It is a retrospective transversal study conducted from 2010 to 2015 using the laboratory database of Caxias do Sul/RS. Variables presented as mean ± standard deviation were compared using Student’s t-distribution for dependent samples, and variables between groups were analyzed using Student’s t-distribution for paired samples. Results: Ninety individuals were included in the study, mean age 46.0 ± 13.5 years (51% men). For evolution, 31% of patients progressed to cure and 69% to chronic phase. We found significance between liver enzymes ALT and GGT when compared first and final results dosed by the laboratory (p< 0.008 and p< 0.007, respectively). Comparing groups showed difference between ALT (first and final) in the cure group (p = 0.012), which did not occurred with ALT in the group of chronic phase (p = 0.848). Conclusion: The study could reveal the behavior of transaminases and GGT front contamination with B hepatitis, evidencing the importance of proper monitoring this disease through laboratory tests to know the real state of the pathology.
Keywords
Biological markers; Liver function tests; Hepatitis B
REFERÊNCIAS
- Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde Departamento de DST, Aids e Hepatites Virais: Boletim Epidemiológico. 2012; 3 (01):19-32.
- World Health Organization [Internet]. Information sheet observed rate of vaccine reactions Hepatitis B vaccine [acesso em nov 2015]. Disponível em: http://www.who.int/vaccine_safety/initiative/tools/Hep_B_Vaccine_rates_information_ sheet.pdf?ua=1
- World Health Organization. Hepatitis B vaccines. Weekly epidemiological record. 2009;84(40):405-20.
- Ferreira MS. Diagnosis and treatment of hepatitis B. Rev Soc Bras Med Trop. 2000;33(4):389-400. [Article in Portuguese].
- Ferreira MS, Borges AS. Advances in the treatment of hepatitis B. Rev Soc Bras Med Trop. 2007;40(4):451-62. [Article in Portuguese].
- Cristina Targa Ferreira, Themis Reverbel da Silveira. Hepatites virais: aspectos da epidemiologia e da prevenção. Rev. Bras. Epidemiologia. 2004;7(4):473-87.
- Patiño -Massis J. Hepatitis B: Quadro clinico. Acta méd.costarric.50 (Suppl 3):9-11, 2008.
- Fonseca JC. Natural history of chronic hepatitis B. Rev Soc Bras Med Trop. 2007;40(6):672-7. [Article in Portuguese].
- Eminler AT, Irak K, Ayyildiz T, Keskin M, Kiyici M, Gurel S, et al. The relation between liver histopathology and GGT levels in viral hepatitis: more important in hepatitis B. Turk J Gastroenterol. 2014; 25(4):411-5.
- World Gastroenterology Organization. Management of acute viral hepatites. Practice Guidelines. 2003; 1 (1): 7-12.
- Hudson Ben, Collins Peter. Chronic hepatitis B: diagnosis, monitoring and management. Prescriber. 2014;25(21): 37-43.
- D’ Souza R, Foster GR. Diagnosis and treatment of chronic hepatitis B. J R Soc Med. 2004;97(7):318-21.
- Lok AS, McMahon BJ. Chronic Hepatitis B: Update 2009. Hepatology. 2009;50(3):661-2.
- Mikolajczyk AE, Aronsohn AI. Current Management of Chronic Hepatitis B and C in Chronic Kidney Disease. Adv Chronic Kidney Dis. 2015 Sep;22(5):352-60.
- Brasil. Ministério da Saúde [Internet]. Hepatite B. Departamento de DST, AIDS e Hepatites Virais [acesso em nov 15]. Disponível em: http://www.aids.gov.br/pagina/hepatite-b.
- World Heath Organization [Internet]. Hepatitis B. Fact sheet N°204 [acesso em nov 2015]. Disponível em: http:// www.who.int/mediacentre/factsheets/fs204/en/
- Souza LA, Mattos AA, Fiorini M, Ribeiro P, Tovo CV. Clinical outcome of a patient cohort with acute hepatitis B. Clinics (Sao Paulo). 2013;68(5):718-20.
- Brasil. Ministério da Saúde. Secretaria de vigilância em saúde departamento de vigilância das doenças transmissíveis. Ampliação da oferta da vacina da Hepatite B para faixa etária de 30 a 49 anos em 2013. 2013.
- Liang X, Bi S, Yang W, Wang L, Cui G, Cui F, et al. Epidemiological serosurvey of Hepatitis B in China – Declining HBV prevalence due to Hepatitis B vaccination.Vaccine. 2009;27(47):6550-7.
- Silva, Alessandro Lisboa da; Vitorino, Rodrigo Roger; Vanderson, Esperidião-Antonio, et al. Hepatites virais: B, C e D: atualização. Rev. Soc. Bras. Clín. Méd;10(3),2012.
- Cruz CRB, Shirassu MM, Martins WP. Comparação do perfil epidemiológico das hepatites B e C em um serviço público de São Paulo. Arq Gastroenterol. 2009;46(3):225-9.
- Chávez JH, Campana SG, Haas P. An overview of hepatitis B in Brazil and in the state of Santa Catarina. Rev Panam Salud Publica. 2003;14(2):91-6. [Article in Portuguese]
- Luna Expedito José de Albuquerque, Moraes José Cássio de, Silveira Lygia, Salinas Hilda Souza Neves. Eficácia e segurança da vacina brasileira contra hepatite B em recém-nascidos. Rev. Saúde Pública [Internet]. 2009;43(6):1014-20. Available from: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0034-89102009000600013&lng=en.
- Wallach Jacques M.D. Interpretação de Exames Laboratoriais. 7ed. Rio de Janeiro: Guanabara Koogan AS, 2003. p. 241-51.
- Lopes Taís Gardenia Santos Lemos, Schinoni Maria Isabel. Aspectos gerais da hepatite B. R. Cie. med. biol. 2011; 10(3):337-44.
- Motta VT. Bioquímica Clínica para o Laboratório: princípios e interpretações. 4ª ed. São Paulo: Robe, 2003.p. 117-9.
Correspondência
Julia Poeta
Rua Orfanotrófio, 555 – Alto Teresópolis
Porto Alegre-RS, Brasil
e-mail: [email protected]
