Diagnóstico parasitológico em amostras fecais no laboratório de análises clínicas: comparação de técnicas e custo de implantação
Parasitological diagnosis in fecal samples in the laboratory of clinical analyses: comparison of techniques and cost of implantation
Eduarda Peixoto Azevedo1
Elida Mateus de Almeida1
Juliana da Silva Matos1
Andreza Rodrigues Ramos1
Mayara Perlingeiro de Siqueira2
Ana Beatriz Monteiro Fonseca3
Alynne da Silva Barbosa 4
Otilio Machado Pereira Bastos5
Claudia Maria Antunes Uchôa6
Discente de Graduação do Curso de Biomedicina da Universidade Federal Fluminense (UFF) – Niterói-RJ, Brasil.
2Estudante de Mestrado do Pós-Graduação do Programa de Microbiologia e Parasitologia da Universidade Federal Fluminense (UFF) –
Niterói-RJ, Brasil.
3Docente do Laboratório de Estatística, Departamento de Estatística, Universidade Federal Fluminense (UFF) – Niterói-RJ, Brasil.
4Docente da Disciplina de Parasitologia do Departamento de Microbiologia e Parasitologia (MIP), Instituto Biomédico (CMB),
Universidade Federal Fluminense (UFF/RJ) e pós-doutoranda do Laboratório de Toxoplasmose, Instituto Oswaldo Cruz, Fundação
Oswaldo cruz – Rio de Janeiro-RJ, Brasil.
5Docente da Disciplina de Parasitologia do Departamento de Microbiologia e Parasitologia (MIP), Instituto Biomédico (CMB),
Universidade Federal Fluminense (UFF) – Niterói-RJ, Brasil.
6Doutor. Professor associado da Universidade Federal Fluminense (UFF) – Niterói-RJ, Brasil.
Instituição: Laboratório de Bioagentes Ambientais, Departamento de Microbiologia e Parasitologia (MIP), Instituto Biomédico (CMB), Universidade Federal Fluminense (UFF) – Niterói-RJ, Brasil.
Suporte Financeiro: Capes e Proppi – Proad UFF.
Artigo recebido em 01/06/2017
Artigo aprovado em 18/09/2017
DOI: 10.21877/2448-3877.201700586
Resumo
Objetivo: Esse estudo objetivou comparar as técnicas de Baermann-Moraes, Faust et al., Ritchie modificada, Lutz e Kato-Katz, para o diagnóstico de parasitoses intestinais e estimar o custo de implantação de cada uma dessas técnicas em um laboratório de análises clínicas. Métodos: Foram analisadas 374 amostras de fezes pelas cinco técnicas. Resultados: Das amostras estudadas, 292 foram analisadas pela técnica de Baermann & Moraes, sendo negativas. A positividade, considerando as demais técnicas, foi de 25,66%. Ritchie modificada detectou positividade em 20,1% das amostras com maior eficiência para Blastocystis sp., seguida por Lutz (15,8%), Faust et al. (12,8%) e Kato-Katz (1,1%). Os índices de concordância Kappa entre as técnicas utilizadas, excluindo Kato-Katz, foram moderados, e de Kato-Katz com as outras técnicas parasitológicas foi fraca. Foi evidenciada ausência de diferença significativa somente entre as técnicas de Faust et al. e Lutz. O Kato-Katz foi considerado uma técnica inadequada para o diagnóstico de parasitoses intestinais, frente ao declínio da frequência de geohelmintíase e permanência ou aumento das infecções determinadas por protozoários. A técnica de Lutz foi a que apresentou menor custo de implantação, seguida por Baermann & Moraes, Kato-Katz, Ritchie modificado e Faust et al., devendo ser a técnica de escolha quando o parâmetro for econômico. Conclusão: Considerando o parâmetro positividade preconiza-se a implantação de Ritchie modificada, embora a associação de técnicas gere resultados mais eficazes. A associação de técnicas com melhores resultados foi de Ritchie modificado e Lutz ou Ritchie modificado e Faust et al.
Palavras-chave
Testes diagnósticos de rotina; Custos e análise de custo; Análise parasitológica
INTRODUção
As parasitoses intestinais são doenças que refletem as condições sanitárias de uma população e ainda hoje preocupam devido à negligência com que têm sido tratadas e por ocorrerem, de forma heterogênea, em diversas regiões do país.(1)
A infecção pode ser favorecida por fatores associados ao hospedeiro, como idade, estado nutricional, genéticos, culturais, comportamentais e profissionais. Também são essenciais fatores relacionados ao parasito, como a resistência ao sistema imune do hospedeiro e os mecanismos de escape vinculados às transformações bioquímicas e imunológicas verificadas ao longo de seu ciclo de vida.(2)
Na rotina laboratorial, o diagnóstico das parasitoses intestinais ocorre, principalmente, mediante a utilização de técnicas parasitológicas em amostras fecais, pois apresentam custo baixo e procedimento técnico simples. A literatura disponibiliza várias técnicas com fundamentos diferentes, como as técnicas de sedimentação e flutuação, que permitem concentrar ovos, cistos, oocistos e larvas de diversas espécies de parasitos intestinais em uma amostra fecal (p. ex. ovos de Ascaris lumbricoides e Trichuris trichiura, cistos de Giardia duodenalis, Endolimax nana e Entamoeba coli), viabilizando determinar sua presença e sua identificação.(3)
O diagnóstico clínico das parasitoses intestinais é impreciso, pois baseia-se em manifestações clínicas, que, nesse caso, podem variar desde quadros assintomáticos a outros de sintomatologias inespecíficas, tais como diarreia, náuseas, desconforto abdominal, dentre outros.(4)
Portanto, o diagnóstico laboratorial desempenha um papel importante no diagnóstico das infecções/doenças parasitárias, sendo a chave para a seleção da conduta terapêutica adequada.(5)
Chaves et al.(6) apontaram que, apesar da existência de inúmeras técnicas, quantitativas e qualitativas, propostas para o exame parasitológico de fezes, todas têm sido objeto de críticas diversas. No laboratório de rotina preconiza-se uma combinação de técnicas com o objetivo de aumentar a acurácia diagnóstica e, consequentemente, diminuir os resultados falsos negativos, principalmente quando há baixa carga parasitária, uma vez que a utilização combinada de várias técnicas com fundamentos distintos é indicada para detectar infecções intestinais causadas por parasitos, tendo em vista sua variabilidade morfológica e biológica.(7)
A comparação de técnicas tem sido estudada por diversos autores (6,8-11) ao longo dos anos, objetivando avaliar sua eficiência no diagnóstico parasitológico.
Baseado nessa diversidade de técnicas para pesquisa de parasitos em amostras fecais, esse estudo comparou cinco diferentes técnicas coproparasitológicas, objetivando ampliar o arcabouço teórico sobre o tema, bem como estimar o custo de sua implantação em um laboratório de Análises Clínicas.
Material e Métodos
As amostras fecais utilizadas foram oriundas de estudantes e funcionários de sete escolas municipais de Niterói-RJ, sendo elas: Anísio Teixeira (A), Santos Dumont (B), Noronha Santos (C), Levi Carneiro (D), Dario de Souza Castello (E), André Trouche (F) e Antônio Coutinho (G). Foram envolvidos os estudantes do 1º ano do Ensino Fundamental I ao 7º ano do Ensino Fundamental II e funcionários. O aceite de participação ao projeto foi voluntário, sendo os escolares representados por seus pais e/ou responsáveis em caso de menores de 18 anos, mediante assinatura do termo de consentimento livre e esclarecido (TCLE).
Para a realização das técnicas parasitológicas foi entregue a cada participante um kit com três recipientes para coleta de amostras fecais, sendo dois com conservante (Railliet & Henry), e um sem conservante. O conservante foi escolhido por ser utilizado com excelentes resultados na rotina de coleta de amostras fecais do laboratório de Bioagentes Ambientais da UFF, tendo em sua composição solução salina, ácido acético e formol. A amostra fecal sem conservante foi processada segundo a técnica de Baermann & Moraes(12) para pesquisa de larvas de nematoides. As amostras coletadas com conservante foram submetidas às técnicas de Ritchie(13) modificado por Young et al.,(14) Faust et al.,(15) Lutz(16) e Kato-Katz.(17) As amostras foram processadas e analisadas na Universidade Federal Fluminense no Departamento de Microbiologia e Parasitologia (MIP). Os resultados obtidos foram analisados de forma descritiva, a concordância de positividade/negatividade por amostra entre as técnicas foi analisada pelo teste de McNemar com intervalo de confiança de 5% e a concordância geral por meio do índice de concordância (Kappa).(18)
Com relação ao custo de implantação utilizou-se a contabilidade de custo(19) como parâmetro para os cálculos da implantação das técnicas parasitológicas em laboratório de Análises Clínicas. Foi considerado como custo de implantação o levantamento de preços de materiais duráveis e materiais descartáveis para a realização de cada técnica, ou seja, o custo unitário do produto. No caso de materiais duráveis e descartáveis foi considerado o preço de menor valor, na análise de até três empresas. Foi pesquisada para materiais duráveis e equipamentos a taxa de depreciação para possibilitar avaliar o custo benefício na compra desses materiais e equipamentos.
Os cálculos utilizados foram: custo dos materiais duráveis, custo dos materiais degradáveis, custo unitário da análise, custo total, depreciação dos materiais duráveis e equipamentos, depreciação anual, cálculo relativo a um funcionário fictício e o custo unitário direto da mão de obra. No custo de materiais duráveis e no custo de materiais descartáveis considerou-se como material de uso geral uma pisseta (durável), um par de luvas (descartável) e cinco mililitros de álcool 70% por técnica (descartável). Para efeito de cálculo da técnica não se retiraram os equipamentos, embora esses possam determinar um aumento no custo dessa técnica, pois calculou-se o custo de implantação em um laboratório que estivesse sendo criado e não o custo de execução da técnica na rotina.
Ética
O estudo foi vinculado ao projeto da Universidade Federal Fluminense e Fundação Municipal de Educação de Niterói intitulado “Parasitoses intestinais em escolares de Niterói, RJ: frequência, conhecimentos e profilaxia” que obteve parecer favorável em 22 de abril de 2014 no Comitê de Ética em Pesquisa da Faculdade de Medicina/Hospital Universitário Antônio Pedro, possuindo registro de identificação no CEP, CMM/HUAP nº 621.193 e CAAE nº 25061913.0.0000.5243 tendo sido desenvolvido de agosto de 2014 a fevereiro de 2016.
Resultados
Foram analisadas amostras fecais de 374 indivíduos. Todas as amostras frescas (n= 292) entregues foram negativas pela técnica de Baermann & Moraes. Considerando as demais técnicas utilizadas, 96/374 (25,7%) foram positivas por uma ou mais técnicas. Houve maior frequência de protozoários que de helmintos.
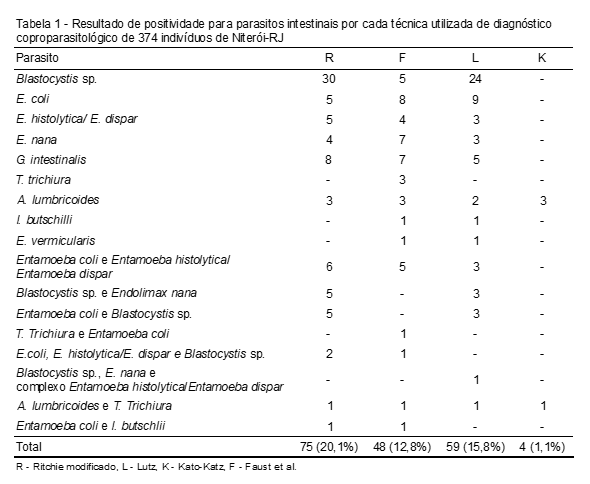
A técnica de Ritchie modificada detectou parasitos em 75 (20,1%) amostras, Lutz em 59 amostras (15,8%), Faust et al. em 48 (12,8%) e Kato-Katz em 4 amostras (1,1%) (Tabela 1). A análise quantitativa na técnica de Kato-Katz, para A. lumbricoides foi de 72, 58, 163 e 47 ovos e T. trichiura de 13 ovos, em associação com A. lumbricoides. Nas amostras positivas, Faust et al. e Lutz apresentaram resultados concordantes em 33 amostras (k=0,55), Ritchie e Faust et al. em 38 amostras (k=0,55), Ritchie e Lutz em 42 amostras (k=0,55), sendo a concordância moderada. As quatro técnicas foram capazes de detectar Ascaris lumbricoides em três amostras.
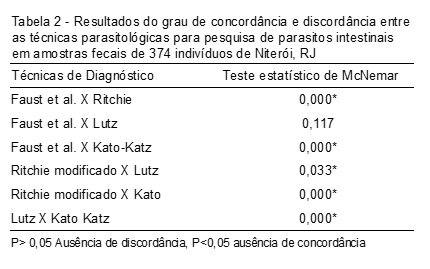
O grau de concordância entre a técnica de Kato-Katz e as técnicas de Ritchie modificado, Faust et al. e Lutz foram de k=0,057, k=0,137 e k=0,077, sendo todas fracas, respectivamente. Os resultados de significância obtidos pelo teste de McNemar estão apresentados na Tabela 2.
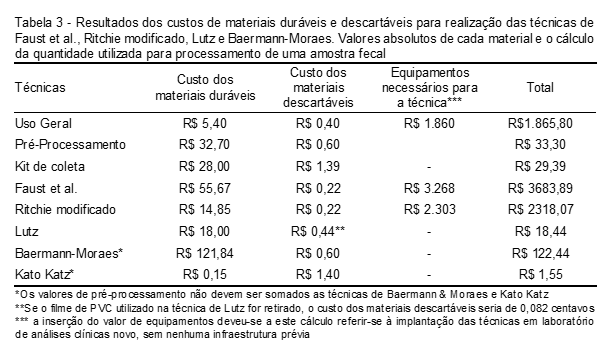
Os resultados dos custos de materiais duráveis e descartáveis para implantação das cinco técnicas de forma individualizada estão apresentados na Tabela 3. Considerando o custo da técnica, associado ao pré-processamento, uso geral e material de coleta, a técnica de Faust et al. foi a que apresentou maior valor (R$ 5.612,38) e a técnica de Kato-Katz a de menor valor (R$1.896,74).
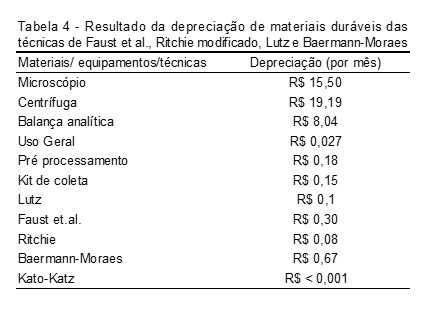
Na Tabela 4 demonstra-se o resultado do custo de depreciação dos materiais duráveis e equipamentos das técnicas de Faust et al., Ritchie modificado, Lutz e Baermann & Moraes.
O custo de implantação unitário de cada técnica está apresentado na Tabela 5.

A técnica de Lutz apresentou com equipamento custo de 19,60 resultante da soma de: 0,81 (mão de obra) + 0,1 (material durável ) + 0,35 (material durável geral) + 15,50 (microscópio) + 0,44 ( material descartável) + 0,40 + 0,60+1,39 (materiais descartáveis gerais). A retirada do custo com equipamento determinaria um custo bem menor (19,60 – 15,50 = 4,10).
Discussão
A positividade para parasitos intestinais, considerando positividade por pelo menos uma das técnicas utilizadas, foi de 25,7% (96/374), sendo superior à obtida nos estudos de Cavagnolli et al.,(20) Ngrenngarmlet et al.,(21) Castro et al.(22) e Ferreira et al.(23) Entretanto, Miotto et al.(24) apresentaram resultados com positividade similar (24,56%). A diferença entre as positividades, nesses diferentes estudos, pode ser associada a diversos fatores, como técnicas empregadas, localidade do estudo, condições socioeconômicas e faixa etária do grupo estudado.
Não foi encontrada nenhuma amostra positiva por meio da técnica de Baermann & Moraes, concordando com os resultados de Carvalho et al.,(9) que justificaram essa negatividade pela inexistência ou baixa frequência de Strongyloides stercoralis no local onde viviam os sujeitos do estudo. Sugere-se que a negatividade também pode ter sido influenciada pela não entrega da amostra sem conservante por 82 participantes, impossibilitando a realização da técnica.
A técnica que demonstrou maior eficiência no diagnóstico foi a de Ritchie modificada (20,1%). Carvalho et al.(9) observaram que o Coprotest®, que usa como fundamento a técnica de Ritchie modificada por Young et al., apresentou melhor resultado como técnica única, bem como no diagnóstico de Blastocystis sp. Nesse estudo, Ritchie modificada também obteve melhores resultados para detecção de Blastocystis sp.
A segunda técnica de maior detecção parasitária foi a de Lutz apresentando positividade em 15,8% das amostras. A espécie mais detectada também foi Blastocystis sp., embora com resultados inferiores à Ritchie modificada. Por ambas serem técnicas de concentração por sedimentação, a quantidade de detritos na lâmina foi grande, o que tornou a leitura mais cansativa. Carvalho et al.,(25) na comparação entre TFT® e Lutz, sugeriram que a centrifugação adicional do TFT®, que também existe em Ritchie modificada, pode ter favorecido a maior concentração de formas evolutivas de parasitos. Sugere-se que o encontro de Blastocystis sp., nessa técnica, contrariando os resultados de Alarcón et al.,(26) deve-se ao uso de conservante na coleta de duas das três amostras, o que pode ter favorecido ao não rompimento do protozoário nas etapas subsequentes do processamento técnico.
Nesse estudo, a técnica de Faust et al. apresentou positividade em 12,8% das amostras, diagnosticando todos os parasitos que foram encontrados, incluindo protozoários e helmintos. Observaram-se resultados, em número absoluto, superiores ou iguais quando se comparou a detecção da maioria dos protozoários por Faust et al. e Ritchie modificada, embora tenha sido evidenciada diferença significativa entre as técnicas. Alyani et al.,(11) comparando Faust et al. e Ritchie, verificaram maior eficiência de Ritchie na detecção de protozoários intestinais, o que difere desse estudo. No presente estudo, a técnica de Faust et al. mostrou importância na detecção não só de protozoários como também na de Trichuris trichiura, sendo 4/5 amostras positivas para esse helminto detectadas somente por meio dessa técnica.
A técnica de Kato-Katz apresentou menor capacidade de detecção entre as técnicas analisadas. Com relação aos helmintos foram encontrados por Kato-Katz, Ascaris lumbricoides e Trichuris trichiura. Essas amostras também foram positivas por pelo menos uma das demais técnicas utilizadas. No caso de T. trichiura, Kato-Katz só detectou o parasito em uma amostra, gerando resultados falso-negativos nas outras quatro. Tal fato pode ter sido devido à leitura de uma única lâmina nessa técnica. Tarafder et al.,(10) Mendes et al.(7) e Nunez-Fernandez et al.(27) apontaram a técnica de Kato-Katz como melhor opção para o diagnóstico de geohelmintos, como Ascaris lumbricoides e Trichuris trichiura, o que está em desacordo com os resultados desse estudo. Pensa-se que a técnica de Kato-Katz, apesar de sua fácil execução, não seria adequada para o diagnóstico de parasitos intestinais, pois a quantidade de amostra utilizada é pequena e, portanto, pouco representativa do que realmente está sendo eliminado no conteúdo fecal do hospedeiro, como proposto por Brandelli et al.(28) para justificar as diferenças de resultados obtidos na comparação entre as técnicas de sedimentação espontânea e Paratest®. Outro fator que contribuiria para sua baixa eficiência seria a distribuição irregular de formas evolutivas de parasitos nas fezes, como apontado por Krauth et al.(29) Sugere-se que o próprio movimento intestinal, em especial do intestino grosso, favoreça a concentração de formas evolutivas de parasitos na superfície do material fecal, o que pode interferir no resultado obtido, dependendo da porção da amostra utilizada no processamento da técnica. Não se discute aqui a eficiência de Kato-Katz para o diagnóstico de S. mansoni, uma vez que o parasito não foi encontrado nas amostras estudadas.
Além desses fatores, cabe lembrar que tem sido observado por vários autores(30,31) uma manutenção ou aumento da frequência de protozoários com redução de frequência de helmintos, o que também reforça a não adequação do uso do Kato-Katz como técnica única na rotina do diagnóstico de parasitos intestinais, ainda que em pesquisa de campo e reforçado pelo índice de concordância baixo com as demais técnicas.
Com relação aos custos de implantação, a técnica que apresentou menor custo foi a de Lutz, incluindo todos os parâmetros analisados. Apesar disso, todas as técnicas parasitológicas avaliadas nesse estudo apresentaram valor mínimo de R$ 19,60 e máximo de R$ 47,58, o que permite sua realização em laboratórios de análises clínicas, mesmo sem grande aporte financeiro. Os kits comerciais, como o Coprotest®, quando cotados em janeiro de 2016, apresentaram o valor de R$ 1.685,00, totalizando 360 unidades. Dessa forma, cada exame teria o custo de R$ 4,68, sendo o descartável. Cerqueira(8) afirmou que o kit Coprotest® apresenta como vantagens alto enriquecimento, detectando tanto protozoários quanto helmintos. Além disso, elimina o mau odor da amostra, simplifica o manuseio pelo técnico e requer pouco espaço. Se for levada em consideração a possível perda dos materiais duráveis e a possibilidade de acidentes nas etapas de processamento e lavagem de vidraria, os kits comerciais representam boas alternativas na rotina laboratorial. Mesmo com esse custo inicial, se for feito o cálculo do custo de implantação da técnica, essa técnica manteve-se dentro dos valores já apresentados (R$ 41,04, esse valor foi calculado segundo a fórmula de valor unitário).
A balança, o microscópio, a centrífuga e o funcionário fictício podem ser considerados como investimentos para o laboratório, pois serão usados por outros setores, não só no setor de Parasitologia. Por isso, o custeio das técnicas se torna mais acessível e baixo. Cabe lembrar que, na rotina, o custo das técnicas será inferior ao de implantação.
Considerando a questão custo de implantação versus capacidade de diagnóstico observou-se variação dentre as técnicas analisadas, sendo a técnica de Lutz a mais indicada, pela simplicidade de procedimentos técnicos, baixo custo e amplo espectro de diagnóstico. A desvantagem dessa técnica estaria relacionada a maior necessidade de espaço para guarda das amostras até a leitura e necessidade de maior tempo para emissão do laudo.
A técnica de Ritchie modificada foi a que apresentou melhores resultados em relação à positividade, porém, a de Faust et al. foi a que detectou maior diversidade de espécies ou gêneros de parasitos. Ambas têm custo próximo e procedimentos técnicos mais complexos, que demandam maior treinamento do profissional. Faust et al. tem como desvantagem o maior tempo de execução, devido às múltiplas lavagens e a possibilidade de deformação de formas evolutivas pela exposição da amostra em solução de sulfato de zinco por tempo excessivo.
Conclusão
A escolha de técnicas para serem implementadas na rotina laboratorial no setor de Parasitologia envolve vários fatores. Cabe lembrar que, para garantir melhor resultado, a associação de técnicas resulta sempre em maior confiabilidade, principalmente quando se utilizam técnicas de fundamentos diferentes. Seguindo essa proposta, as técnicas mais indicadas seriam, objetivando maior positividade, Ritchie modificado e Lutz, seguido pela associação de Ritchie modificado e Faust et al.
Agradecimentos
Ao Núcleo de Ações Integradas da Fundação Municipal de Educação de Niterói, às Escolas Municipais de Niterói representados por seu corpo docente, discentes e responsáveis pela participação na coleta de amostras.
Abstract
Objective: This study aimed to compare the techniques of Baermann-Moraes, Faust et al., modified Ritchie, Lutz and Kato-Katz for the diagnosis of intestinal parasitosis and to estimate the cost of implantation of each of these techniques in a clinical analysis laboratory. Methods: A total of 374 faecal samples were analyzed by the five techniques. Results: Of the samples studied, 292 were analyzed by the Baermann-Moraes technique and were negative. Positivity, considering the other techniques, was 25.66%. Modified Ritchie detected positivity in 20.1% of the samples with greater efficiency for Blastocystis sp., Followed by Lutz (15.8%), Faust et al. (12.8%) and Kato-Katz (1.1%). The Kappa agreement indexes between the techniques used excluding Kato-Katz were moderate and Kato-Katz with the other parasitological techniques was weak. It was evidenced absence of significant difference only between the techniques of Faust et al. and Lutz. Kato-Katz was considered an inadequate technique for the diagnosis of intestinal parasitosis, in the face of the decline in the frequency of geohelminthiasis and the permanence or increase of the infections determined by protozoa. Lutz presented the lowest implantation cost, followed by Baermann-Moraes, Kato-Katz, modified Ritchie and Faust et al., and should be the technique of choice when the parameter is economical. Conclusion: Considering the positivity parameter, the implementation of modified Ritchie is recommended, although the association of techniques yields more effective results. The association of best-performing techniques was between modified Ritchie and Lutz or modified Ritchie and Faust et al.
Keywords
Diagnostic tests, Routine; Costs and cost analysis; Parasitological analysis
REFERÊNCIAS
- Cruz PFF, Rezende DV, Penatti MPA, Guimarães EC, Pedroso RS; LIMA SC. Ações educativas com ênfase à prevenção de parasitoses intestinais em uma localidade rural no município de Uberlândia, MG. REBES. 2014;4(2):8-15.
- Chieffi PP, Amato Neto V. Vermes, verminoses e a saúde pública. Cienc. Cult. 2003;55:41-3.
- De Carli GA. Parasitologia clínica: seleção de métodos e técnicas de laboratório para o diagnóstico das parasitoses humanas. São Paulo, Editora Atheneu p.58, 2007.
- Oriehl TC, Ash LR, Ramachandran CP, Ottesen E. Medios Auxiliares para el Diagnóstico de las Parasitosis Intestinales. Geneva: Organización Mundial de la Salud, 1997.
5 . Machado ER, Santos DS, Costa-Cruz JM. Enteroparasites and commensals among children in four peripheral districts of Uberlândia, State of Minas Gerais. Rev Soc Bras Med Trop. 2008; 41(6):581-5.
- Chaves A, Alcantara OSD, Carvalho ODS, Santos JSD. Estudo comparativo dos métodos coprológicos de Lutz, Kato-Katz e Faust modificado. Rev Saúde Públ. 1979;13:348-52.
- Mendes CR, Teixeira ATLS, Pereira RAT, Dias LCDS. Estudo comparativo de técnicas parasitológicas: Kato-Katz e Coprotest®. Rev Soc Bras Med Trop. 2005;38(2):178-80.
- Cerqueira FL. Coprotest: Metodologia confiável para o exame parasitológico de fezes. LAES/HAES. 1988;9(51):5-9.
- Carvalho FM, Falção AO, Albuquerque MC, Silva P, Bastos OMP, Uchôa CMA. Diagnóstico coproparasitológico: estudo comparativo entre os métodos de Faust e cols.; Lutz, Baermann e Moraes e Coprotest®. Rev bras anal clin. 2002;36:145-6.
- Tarafder MR, Carabin H, Joseph L, Balalong E, Olveda R, McGarvey ST. Estimating the sensitivity and specificity of Kato-Katz stool examination technique for detection of hookworms, Ascaris lumbricoides and Trichuris trichiura infections in humans in the absence of a ‘gold standard’. Int. j. parasitol. 2010;40(4):399-404.
- Alyani D, Murhandarwati EH, Sumarni S, Ernaningsih E. Comparing the Sensitivity and Specificity of Zinc Sulphate Flotation Method to Formol Ether Sedimentation Method in Identifying Intestinal Protozoa’s Cysts. Trop Med J. 2015; 3(2):176-83.
- Baermann G. Eine einfache methode zur auffindung von ankylostomum (Nematoden) larven in erdproben. Geneeskunding Tijdschrift voor Nederlandsch-Indië. 1917; 7:131-7.
- Ritchie LS. An ether sedimentation technique for routine stool examinations. The Bulletin of the U.S. Army Medical Department. 1948, 8:4.
- Young KH, Bullock SL, Melvin DM, Spruill CL. Ethyl acetate as a substitute for diethyl ether the formalin-ether sedimentation technique. J Clin Microbiol. 1979;10(6):852-3.
- Faust EC, D’Antoni JS, Odon V, Miller MJ, Perez C, Sawitz W, Thomen LF, Tobie J, Walker JH. A critical study of clinical laboratory technics of the diagnosis of protozoan cysts and helminth eggs in feces.I – Preliminary communication. Am J Trop Med. 1938;18:169-83.
- Lutz A. O Schistosomum mansoni and Schistosomatosis observed in Brazil. Mem. Inst. Oswaldo Cruz. 1919;11(1):121-55 Available from: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0074-02761919000100006&lng=en
- Katz N, Chaves A, Pellegrino J. A simple device for quantitative stool thick-smear technique in schistosomiasis mansoni. Rev Inst Med Trop. São Paulo, v. 14, p. 397-400, 1972.
- Landis JR, Koch GG. The measurement of observer agrément for categorical data. Biometrics. 1977;33:159-74.
- Fapan. Faculdade de Paraíso do Norte. Apostila de Contabilidade de Custos I. Disponível em: <www.fapanpr.edu.br/ site/docente/arquivos/Apostila%20Custos%20%20Auxiliar.pdf>. Acesso em: 02/12/2015.
- Cavagnolli NI, Camello JT, Tesser S, Poeta J, Rodrigues AD. Prevalência de enteroparasitoses e análise socioeconômica de escolares em Flores da Cunha- RS. Rev patol. trop. 2015; 44(3):312-22.
- Ngrenngarmlert W, Lamon MC, Pasaralertsakul S, Yaicharoen R, Wongjindanon N, Sripochang S, Kiatfuengfoo R. Intestinal parasitic infections among school children in Thailand. Trop. Biomed. 2007; 24(2):83-8.
- Castro AZ, Viana JD, Penedo AA, Donatele DM. Levantamento das parasitoses intestinais em escolares da rede pública na cidade de Cachoeiro de Itapemirim-ES. Newslab. 2004;64(13):140-4.
- Ferreira MU, Ferreira CDS, Monteiro CA. Tendência secular das parasitoses intestinais na infância na cidade de São Paulo (1984-1996). Rev. Saúde Pública. 2000;34(6 Supl):73-82.
- Miotto JE, Caro DSA, Barros MF, Rego BEF, Santos FC, Macagnan R, Santos IS. Diagnóstico laboratorial de enteroparasitoses e anemia e sua possível associação com eosinofilia em crianças em idade escolar em Ubiratã-PR. Biosaúde. 2016;16(2):52-62.
- Carvalho GL, Moreira LE, Pena JL, Marinho CC, Bahia MT, Machado-Coelho GL. A comparative study of the TF-Test®, Kato-Katz, Hoffman-Pons-Janer, Willis and Baermann-Moraes coprologic methods for the detection of human parasitosis. Mem Inst Oswaldo Cruz. 2012;107(1):80-4.
- Alarcón R, Amato-Neto V, Gakiya E, Bezerra R. Observações sobre Blastocystis hominis e Cyclospora cayetanensis em exames parasitológicos efetuados rotineiramente. Rev Soc Bras Med Trop, 2007;40(2): 253-5.
- Núñez-Fernández FA, Sanjurjo Gonzalez E, Finlay Villalvilla CM. Comparison of several coproparasitological techniques for the diagnosis of soil-transmitted intestinal helminthiasis. Rev Inst Med Trop Sao Paulo. 1991;33(5):403-6. [Article in Spanish]
- Brandelli CL, Cargnin ST, Willers DM, Oliveira KR, Tasca T.. Comparison between spontaneous sedimentation method and Paratest® for the diagnosis of intestinal parasitic infections. Trans R Soc Trop Med Hyg. 2011;105(10):604-6.
- Krauth SJ, Coulibaly JT, Knopp S, Traoré M, N’Goran EK, Utzinger J. An in-depth analysis of a piece of shit: distribution of Schistosoma mansoni and hookworm eggs in human stool. PLoS Negl Trop Dis, 2012;6(12):e1969.
- Belo VS, Oliveira RB, Fernandes PC, Nascimento BWL, Vitorino F, Fernandes CLF, Silva ES. Fatores associados à ocorrência de parasitoses intestinais em uma população de crianças e adolescentes. Rev Paul Pediatr. 2012;30(2):195-201.
- Melo EV, Costa WD, Conceição MJ, Coura JR. A comparative cross-sectional study on the prevalence and morbidity of schistosomiasis in a community in northeastern Brazil (1979-2010). Mem Inst Oswaldo Cruz. 2014;109(3):340-4.
Correspondência
Claudia Maria Antunes Uchôa
Rua Prof. Hernani Pires de Melo, n° 101,
24210 -130, – Niterói-RJ, Brasil
tel: (21) 2629-2426.
