Controle da qualidade laboratorial: implementação de valores de referência próprios determinados no controle interno
Quality control laboratory: implementation of proper reference valeus determinated by internal control
Evandro Brandelero1, Flavia Debiasi Tessari2
1 Mestre/Unoesc – Universidade do Oeste de Santa Catarina – campus Videira. Videira, SC, Brasil.
2 Auxiliar de Laboratório/Unoesc – Universidade do Oeste de Santa Catarina – campus Videira. Videira, SC, Brasil.
Recebido em 05/07/2021
Aprovado em 17/03/2022
DOI: 10.21877/2448-3877.202202163
INTRODUÇÃO
O controle da qualidade é um sistema ativo e complexo, envolvendo todos os setores de uma empresa, com o propósito de aperfeiçoar e garantir a qualidade final do serviço prestado.(1) Nas análises clínicas, o controle da qualidade é imprescindível, tendo em vista a necessidade de um resultado seguro e confiável para um diagnóstico médico preciso, visto que algumas tomadas de decisões são cruciais, urgentes e irreversíveis. Desta maneira, os laboratórios clínicos vêm aprimorando seu sistema interno da qualidade com o uso de métodos alternativos adequados às normas técnicas, reduzindo ao mínimo as falhas e interferências.(2,3)
No laboratório de análises clínicas, o controle de qualidade deve envolver todas as etapas do processo, sendo elas a pré-analítica, analítica e pós-analítica.(4) A etapa pré-analítica engloba o requerimento da análise, a coleta da amostra e a triagem inicial da análise. A etapa analítica reúne todos os procedimentos necessários para execução da análise e, em seguida, a etapa pós-analítica, do alcance do resultado até a dispensa do laudo.(5) Qualquer laboratório de análises clínicas deve dispor de manuais de procedimentos operacionais padrão (POPs) abrangendo orientações e dados inerentes à rotina laboratorial.(6) Os POPs devem retratar minunciosamente as práticas laboratoriais, desde a fase pré-analítica até a pós-analítica, contendo explicações sobre o manejo correto com os equipamentos, precauções de biossegurança e detalhes dos processos técnicos. Esse procedimento tem como objetivo a padronização das técnicas por parte de todos os envolvidos, assegurando a qualidade final do serviço prestado. Sendo assim, o uso adequado desses procedimentos diminui os erros e faz com que as ações arriscadas não se tornem rotineiras.(7)
A área da saúde deve sempre se basear em evidências científicas, englobando parâmetros próprios para os ensaios bioquímicos. O valor de referência dos controles é um dos segmentos mais relevantes na análise laboratorial, visto que auxilia os profissionais na liberação de um resultado coerente, futuro diagnóstico e tratamento do paciente. Todavia, a origem desses valores raramente é determinada pelos laboratórios, e frequentemente são usados controles comerciais sem considerar as individualidades, como aparelho e reagentes utilizados, por exemplo.(8)
As amostras utilizadas como controle dispõem de valores preestabelecidos e sua supervisão é efetuada através de ensaios estatísticos, considerando valor de média, desvio padrão e coeficiente de variação. Para tanto, utilizam-se os gráficos de Levey-Jennings e as regras múltiplas de Westgard para interpretação, técnicas empregadas mundialmente na análise dos controles internos de qualidade.(9) Em 1950 Levey-Jennings introduziu os gráficos no laboratório de análises clínicas e em 1952 Henry e Segalove simplificaram e popularizaram os gráficos para utilização em amostras de controle.(3) O gráfico de Levey-Jennings permite que os resultados obtidos de controle interno sejam inseridos e confrontados com os “Limites Aceitáveis de Erro (LAE)” para cada analito, que é de dois desvios padrão. No momento em que o valor do controle obtido fica fora do LAE, ou seja, excede a média de mais ou menos dois desvios padrão, demonstra a possibilidade de falha no processo, indicativo de que esse analito não está reproduzindo da forma esperada.(10)
Com os valores próprios de referência dos controles sendo introduzidos, supervisionados diariamente no gráfico de Levey-Jennings e interpretados pelas regras múltiplas criadas por Westgard, procedimento utilizado para avaliar a aceitação ou rejeição de uma corrida analítica,(11) o acompanhamento das amostras controle é simplificado, pois são fáceis de serem visualizadas as tendências e os erros aleatórios e/ou sistemáticos. Esse trabalho é um desafio constante para o laboratório clínico, mas esse processo pode minimizar custos, diminuir erros e imprecisões, gerando resultados mais exatos e precisos.(3)
Interpretação pelas regras múltiplas de Westgard
As regras ajudam no entendimento dos resultados de controle, verificando de forma íntegra os dois níveis de cada analito. A utilização das regras auxilia na identificação de todas as situações possíveis, facilitando a detecção de perda de estabilidade de algum analito e, quando violadas, devem ser verificados e encontrados os possíveis causadores do problema e tomadas ações preventivas e/ou corretivas, dependendo do caso. Para tanto, os resultados dos controles foram alimentados no gráfico e aplicando-se as regras.
A regra: 1³s é quando um dos níveis do controle excedem o limite de ±3DP. Os resultados desse analito não podem ser liberados, pois indicam um aumento do erro aleatório ou um erro sistemático. A regra 1²s é quando um dos controles excede o limite de ±2DP, e nesse caso os resultados também não devem ser liberados, pois estão acima do estipulado pelo laboratório. Quando houve a quebra dessas duas regras, os controles foram repassados, certificando-se da qualidade da preparação dos mesmos e correta homogeneização. Quando a segunda passagem dos controles se apresentava dentro dos ±2DP o resultado era aceito, indicando uma não conformidade com a alíquota controle. Quando repetido e os valores ainda estavam superiores a ±2DP, os testes precisavam ser calibrados e repetidos mais uma vez. A regra 2²s é quando os dois níveis do controle excedem o limite ±2DP, indicando um erro sistemático, e então os resultados não devem ser liberados. A regra 4s é quando a diferença entre os dois controles excede 4DP, representando um erro aleatório. A regra 4¹s é quando quatro valores consecutivos de um controle excedem ±1DP, indicando um erro sistemático. A regra 7x é quando os valores permanecem do mesmo lado da média por 7 dias consecutivos, mesmo dentro de ±1DP. A regra 7t é quando os valores estão decrescendo ou crescendo por 7 dias consecutivos, não sendo necessário ultrapassar ±1DP. Significa um erro de tendência sistemático. A regra 10x é quando os valores estão no mesmo lado da média em 10 dias consecutivos, não sendo necessário ultrapassar ±1DP, indicando um erro de tendência sistemático.(12)
Um resultado analítico depende diretamente da qualidade da água utilizada e dos equipamentos. Elementos analíticos como esses precisam ser monitorados e otimizados, pois o mau uso pode acarretar falha nos resultados. A água em um laboratório clínico é o reagente mais utilizado, visto as diversas funções que exerce, como diluições das amostras, reconstituição dos controles e calibradores, preparação das soluções de limpeza e enxague, alimentação dos equipamentos, lavagem de vidrarias, entre outras. É também facilmente contaminável, por isso é necessário passar pelo tratamento adequado e um rígido controle de qualidade antes do seu uso. A Resolução da Diretoria Colegiada (RDC) 302:2005 recomenda que os laboratórios de análises clínicas durante a fase analítica utilizem como controle de qualidade a aferição do grau de pureza da água utilizada.(13)
Somente através da implantação de um controle de qualidade eficaz em todos os pontos, podem-se obter resultados mais exatos, ou seja, resultados que tenham o valor verdadeiro do analito e resultados mais precisos, gerando valores iguais quando uma amostra for repetida várias vezes.(14) Na área da saúde, mais do que corresponder aos interesses dos seus clientes, procura-se constantemente aprimorar as metodologias, com o intuito de minorar as ameaças à vida do paciente, conduta essa demonstrada na entrega de informações diagnósticas coesas e fiéis, no momento em que ela for vital. Para isso, é necessário controlar de forma efetiva todos os métodos utilizados, reconhecendo prováveis erros, assim que eles se apresentarem, e manter-se apto para agir instantaneamente sobre ela.(14)
MATERIAL E MÉTODOS
Foi realizada uma pesquisa laboratorial de caráter qualitativo descritivo em um laboratório de análises clínicas na cidade de Videira, em Santa Catarina, com objetivo de criar os valores próprios de referência para os controles de qualidade internos das bioquímicas, implementação e acompanhamento dos dados gerados nos gráficos de Levey-Jennings, interpretados pelas regras múltiplas de Westgard.
O laboratório faz uso de amostras controles comerciais em dois níveis (normais e patológicos) da marca Labtest e o aparelho utilizado para as análises é o modelo Labmax 240, também da marca Labtest. O controle interno realizado pelo laboratório era inicialmente baseado nos dados disponibilizados em bula, usando como critério de aceitação e rejeição ±2DP. Para realização do presente estudo, foram acompanhadas as rotinas analíticas, a preparação das alíquotas de controle interno e as condições gerais do equipamento.
Implantação dos próprios valores de referência dos controles de qualidade interna
Para a implantação dos valores próprios de referência dos controles, inicialmente foram avaliadas a exatidão, a precisão e a repetição do controle. Para isso, foram realizadas 20 corridas analíticas, sendo uma corrida por dia, por 20 dias consecutivos, nas mesmas condições em que se dosam as amostras de pacientes, utilizando os controles comerciais dos dois níveis, para cada analito. A partir dos resultados obtidos, foi determinada a média, o desvio padrão e o coeficiente de variação de cada analito, nos dois níveis, para determinar os novos valores (próprios) de referência do controle interno.
Implantação dos gráficos de Levey-Jennings
Depois de obtidos os resultados, foram estimados a média e o desvio padrão através do programa Excel. A partir dos dados, foram gerados dois gráficos, um para cada nível de controle.
No eixo X, horizontal, foi acomodada a escala de dias corridos, de 1 a 31, e foi nomeado como “dia da corrida analítica”. No eixo Y, vertical, apresentam-se os valores encontrados nos controles e o gráfico foi regulado para acondicionar o menor e o maior valor esperado(15). Por isso, os gráficos foram criados baseados em ±4DP. Para incluir os valores nas linhas, foi necessário então seguir a seguinte ordem, de cima para baixo do gráfico: na primeira linha média + 4DP, na segunda linha média +3DP, na terceira linha média +2DP, na quarta linha média +1DP, na quinta linha o valor da média, na sexta linha média -1DP, na sétima linha média -2DP, na oitava linha média -3DP, na nona linha média -4DP. Esse eixo foi titulado como “valores dos controles internos”.
Os valores encontrados para cada analito foram introduzidos nos gráficos e cada valor encontrado deve permanecer dentro do limite estipulado de ±2DP, comumente utilizado pelos laboratórios. O esperado é que se mantenham aproximadamente a metade de cada lado da média.(3)
RESULTADOS
A implantação dos valores próprios de referência dos controles internos obteve os resultados esperados, de fácil observação e entendimento, deixando os analitos visualmente estáveis e facilitando o trabalho dos profissionais. O analito glicose, conforme bula do controle Qualitrol nível 1, possui um intervalo proposto de 78 a 106, com valor de média 92. E conforme bula do controle Qualitrol nível 2, com intervalo proposto de 213 a 288, com valor de média 255.
A partir das 20 corridas analíticas e determinação dos valores próprios de referência dos controles, foi obtido para o nível 1, um intervalo de 84 a 102, com valor de média 93,50. A amplitude de variação dos resultados obtidos foi 83 a 101 (Figura 1), um desvio padrão de 4,33 (Figura 2) e um coeficiente de variação de 4,64.
Na Figura 3 são apresentados os valores individuais das medições da glicose, nível 1 (valores normais), transcorridas durante o mês, após a implantação dos valores próprios de referência do controle interno de qualidade (CQI). É possível verificar que o analito se manteve estável e reproduzindo de acordo com o esperado. Não houve quebra de nenhuma regra e todos os pontos se mantiveram dentro dos dois desvios padrão, intercalando-se com frequência acima e abaixo da média.
Para o nível 2, foi obtido um intervalo de 236,73 a 281,87, com valor de média 259,30. A amplitude de variação dos resultados obtidos foi de 245 a 279 (Figura 4), um desvio padrão de 11,29 (Figura 5) e um coeficiente de variação de 4,35.
Na Figura 6 são apresentados os valores individuais das medições da glicose, nível 2 (valores patológicos), transcorridas durante o mês, após a implantação dos valores próprios de referência do controle interno de qualidade (CQI). É possível verificar que nesse caso o analito também se manteve estável e reproduzindo de acordo com o esperado. Não houve quebra de nenhuma regra e todos os pontos se mantiveram dentro dos dois desvios padrão, intercalando-se com frequência acima e abaixo da média.
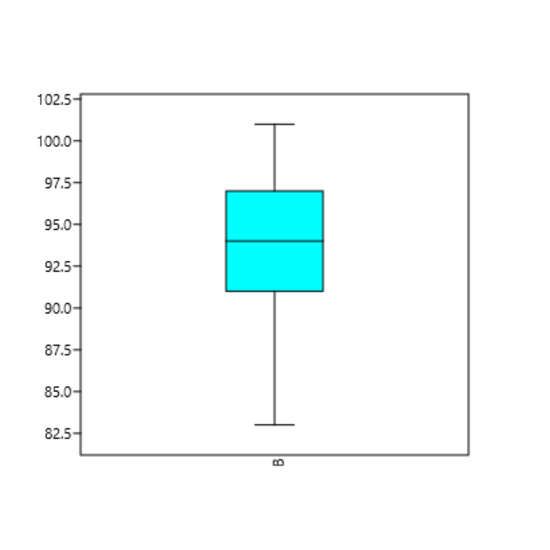
Figura 1
Amplitude de variação dos resultados obtidos do Qualitrol nível 1.
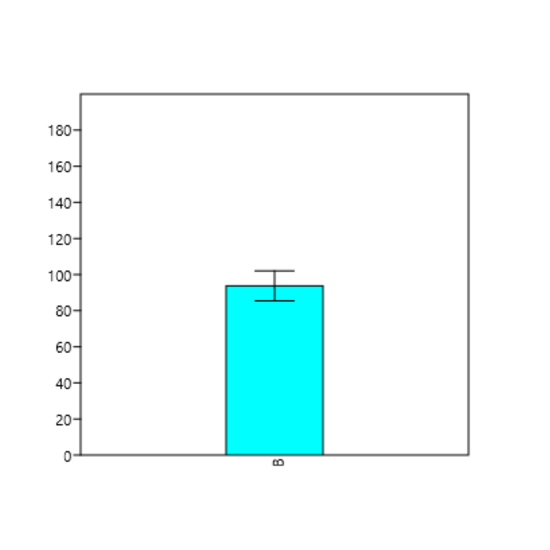
Figura 2
Valor de média e desvio padrão.
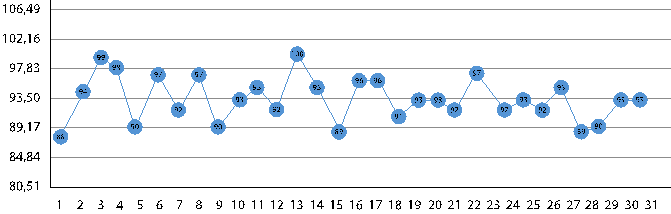
Figura 3
Valores da glicose obtidos com os próprios valores de referência do CQI nível 1.
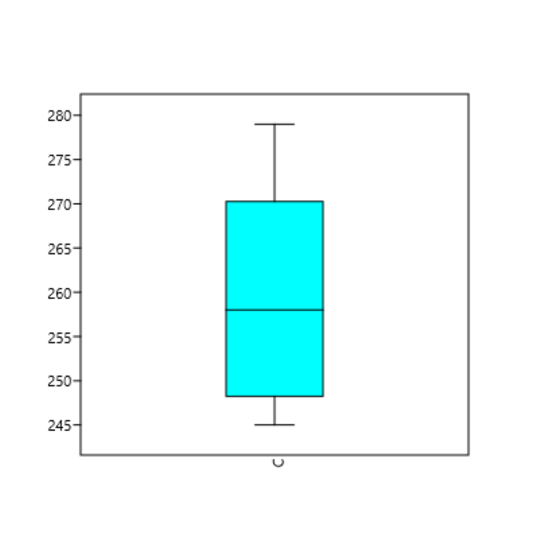
Figura 4
Amplitude de variação dos resultados obtidos do Qualitrol nível 2.
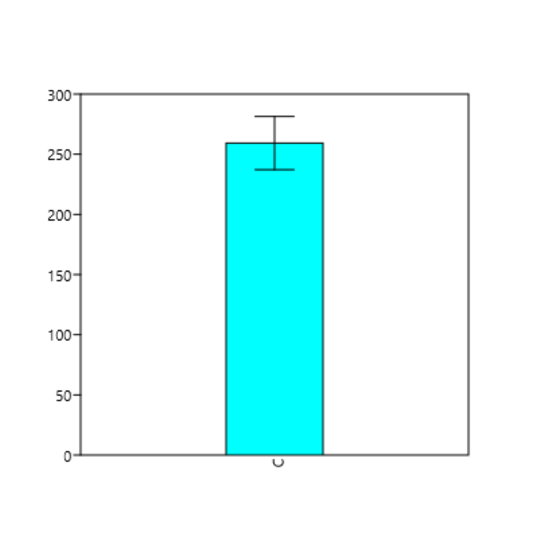
Figura 5
Desvio padrão obtido da glicose no Qualitrol nível 2.
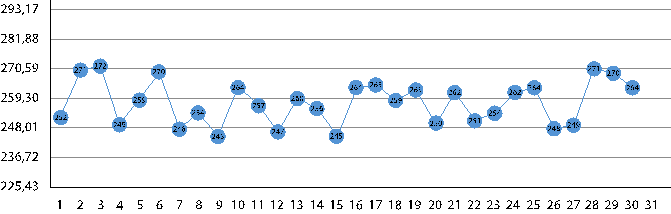
Figura 6
Valores da glicose obtidos com os próprios valores de referência do CQI nível 2.
DISCUSSÃO
A melhoria contínua da qualidade dentro dos processos de qualquer organização se faz necessária para garantir serviços e produtos excelentes, que atendam a todas as necessidades do cliente, entregando não somente o que lhes foi solicitado, mas superando suas expectativas. Na área da saúde, a prioridade fundamental é minimizar os erros, visto que estes podem colocar em risco a vida dos pacientes. Desta forma, nota-se a relevante importância de todos os processos que norteiam a qualidade interna do laboratório clínico, garantindo a liberação de um resultado confiável e extremamente fidedigno à situação do paciente. Para tanto, os usos de ferramentas de garantia de qualidade auxiliam em cada etapa do processo, permitindo a identificação e correção de falhas antes da liberação do resultado.
Com o presente estudo foi possível implantar uma ferramenta utilizada mundialmente como controle de qualidade, para aprimorar o controle interno das bioquímicas. Observou-se que inúmeras variantes podem interferir na análise clínica de um analito, gerando perdas de exatidão, precisão e tendências. Entre eles pode-se citar:
A qualidade da água utilizada, a forma de armazenamento das alíquotas controle, que depois de reconstituídas devem ficar na temperatura de -8°C a -30°C e protegidas da luz, sendo que alguns analitos como as bilirrubinas, são fotossensíveis.
A temperatura do banho-maria utilizada para reconstituição das alíquotas, que devem estar a até 37°C, a homogeneização da alíquota antes da introdução no aparelho, o lote do controle utilizado, pois para cada lote do controle comercial, deve-se refazer as 20 corridas analíticas e recalcular, obtendo os seus próprios valores de referência.
Condições de armazenamento dos reagentes usados, validade e preparação dos mesmos. Limpeza e condição dos materiais utilizados, falhas na operação do equipamento, defeitos no aparelho, sujeira e/ ou formação de fibrina na agulha, cubetas sujas ou riscadas, vida útil da lâmpada do aparelho, falta de homogeneização dos reagentes, formação de bolhas nos reagentes ou na alíquota controle, deterioração dos reagentes, principalmente os enzimáticos, que são menos estáveis.
Todos esses pontos devem estar registrados nos Procedimentos Operacionais Padrão (POPs), e quando seguidos à risca por todos os integrantes da equipe é possível reduzir as falhas e obter os resultados desejados. Em alguns casos, para deixar o controle dentro dos ±2DP esperados, foi necessário descartar o reagente e preparar um novo, descartar as alíquotas controles e preparar novas, pois por algum motivo perderam a estabilidade. Refazer o controle interno da água reagente, realizar a calibração de alguns analitos, trocar a lâmpada e as cubetas do aparelho, treinar os envolvidos para as manutenções preventivas e corretivas dos equipamentos, como a limpeza diária da agulha e lavagem das cubetas.
Mediante essas ações preventivas e corretivas que transcorreram durante o período do estudo, a implantação dos próprios valores e aplicação das regras no gráfico, obtivemos resultados com um excelente desempenho, apresentando uma baixa amplitude de variação entre os dias testados. Os resultados dos controles próprios de qualidade interna, quando dosada a glicose, reproduziram muito bem nos dois níveis. Foram testados outros 23 analitos e foi possível constatar o mesmo desempenho em todos.
CONCLUSÃO
Foi possível constatar que implementando os próprios valores de referência dos controles de qualidade interna, monitorando os mesmos pelo gráfico de Levey-Jennings e interpretando-o pelas regras múltiplas de Westgard, os analitos apresentaram-se minunciosamente mais estáveis, sendo possível observar a formação de tendências, evitando a quebra das regras, resultando em exames seguros e confiáveis, com a liberação de um laudo coeso, facilitando o diagnóstico e tratamento desse paciente.
REFERÊNCIAS
- Paladini EP. Qualidade total na prática. Implantação e avaliação dos sistemas de qualidade total. São Paulo: Atlas; 1997.
- Agência Nacional de Vigilância Sanitária (Brasil). Resolução RDC nº 302, de 13 de outubro de 2005. Regulamento Técnico para funcionamento de Laboratórios Clínicos. [portaria na Internet]. Diário Oficial da União 13 out 2005 [acesso em 23 abr 2021]. Disponível em: https://pncq.org.br/wp-content/uploads/2020/05/RDC-302-2005.pdf.
- Motta VT. Bioquímica clínica para o laboratório: Princípios e interpretações. Caxias do Sul: EDUCS; 2003.
- Chaves CD. Controle de qualidade no laboratório de análises clínicas. Jornal Brasileiro de Patologia e Medicina Laboratorial. 2010; 46(5).
- Garcia LS, Bruckner DA. Diagnostic Medical Parasitology. 3 ed., Washington: ASM Press, 1997.
- Souza RF, Amor ALM. Controle de qualidade de técnicas realizadas nos laboratórios de parasitologia da Secretaria Municipal de Saúde do Município de Salvador, Bahia. RBAC 2010; 42(2): 101-6.
- Agência Nacional de Vigilância Sanitária [homepage na Internet]. Segurança e controle de qualidade no laboratório de microbiologia clínica. [acesso em 03 abr 2021]. Disponível em: http://www.anvisa.gov.br
- Rosenfeld LG, Silva Júnior JB. Valores de referência para exames laboratoriais de hemograma da população adulta brasileira: pesquisa nacional de saúde. Revista Brasileira de Epidemiologia [periódico na Internet]. 2019 Fev [acesso em 25 abr 2021]; 22(2). Disponível em: https://www.scielo.br/j/rbepid/a/79JFJqJnBqcpgFL4CHVGdxS/?lang=pt
- Teodoro FR, Rabelo MS. Aplicação e adequação dos controles internos e externos de qualidade nos laboratórios de análises clínicas de Uruaçu, Goiás. Uruaçu. Monografia [Especialização em Gestão da Qualidade para Laboratório de Análises Clínicas] – Universidade Cruzeiro do Sul; 2013 [acesso em 23 abr 2021]. Disponível em: https://ceafi.edu.br/site/wp-content/uploads/2019/05/aplicao-e-adequao-dos-controles-internos-e-externos-de-qualidade-nos-laboratrios-de-anlises-clnicas-de-uruau-gois.pdf
- Lopes HJJ. Garantia e Controle da Qualidade no Laboratório Clínico Gold Analisa Diagnóstica [periódico na Internet]. 2003 [acesso em 25 abr 2021]. Disponível em: http://www.goldanalisa.com.br/arquivos/%7B8530AFBA-AE96-4413-90EE-9C929C896B39%7D_Garantia_e_Controle_da_Qualidade_no_Laboratorio_Clinico[1].pdf
- Westgard JO. Regras Múltiplas e “Regras de Westgard”: O que são? Controllab. [periódico na internet]. 2003 [acesso em 20 abr 2021]. Disponível em: https://so.controllab.com/pdf/westgard_o_que_sao.pdf
- Qualichart [homepage na Internet]. Regras múltiplas: As regras de Westgard no Controle da Qualidade dos Laboratórios Clínicos [acesso em 27 abr 2021]. Disponível em: https://www.qualichart.com.br/lp/regras-de-westgard-regras-multiplas.html
- Mendes ME, Fagundes CC, Porto CC, Bento LC, Costa TGR, Santos RA, et al. A importância da qualidade da água reagente no laboratório clínico. Jornal Brasileiro de Patologia e Medicina Laboratorial [periódico na Internet]. 2011 Jun [acesso em 03 mai 2021]; 47(3). Disponível em: https://www.scielo.br/j/jbpml/a/8sgJW4hxRbjp5QCqyY9Q4hx/?format=pdf&lang=pt
- Berlitz FA. Controle da qualidade no laboratório clínico: alinhando melhoria de processos, confiabilidade e segurança do paciente. Jornal Brasileiro de Patologia e Medicina Laboratorial [periódico na Internet]. 2010 Out [acesso em 03 mai 2021]; 46(5). Disponível em: https://www.scielo.br/j/jbpml/a/4WDGyv4yhv8fWnKXLVGnZRD/?format=pdf&lang=pt
- Corrêa JA. Garantia da qualidade no laboratório clínico. 3° edição. Rio de Janeiro: PNCQ; 2011.
Correspondência
Flavia Debiasi Tessari
Unoesc – Universidade do Oeste de Santa Catarina – campus Videira
Rua Helia Maria Braga Ferlin, 119
E-mail: [email protected]
