Coilocitose
Koilocytosis
Melissa Freire Zimmer1
Camila Tonet1
Lisiane Cervieri Mezzomo2
1Curso de Pós-Graduação em Citopatologia Diagnóstica – Universidade Feevale. Novo Hamburgo-RS, Brasil.
2Farmacêutica-Bioquímica/Citopatologista/Citologista. Doutorado em Patologia – Universidade Federal de Ciências da Saúde de Porto Alegre (UFCSPA). Porto Alegre -RS, Brasil.
Instituição: Universidade Feevale – Curso de Pós-graduação em Citopatologia Diagnóstica. Novo Hamburgo-RS, Brasil.
Conflito de interesses: não há conflito de interesse.
Recebido em 28/08/2019
Aprovado em 29/04/2020
DOI: 10.21877/2448-3877.202000897
INTRODUÇÃO
O Papiloma Vírus Humano (HPV) é um vírus de DNA. Já foram descritos mais de duzentos tipos e, destes, aproximadamente 45 infectam o epitélio do trato anogenital masculino e feminino.(1) Os subtipos virais do HPV podem ser classificados de acordo com a capacidade de causar infecção, podendo ser de baixo e alto risco oncogênico. Os HPVs considerados de baixo risco são principalmente os tipos 6, 11, 40, 42, 43, 54, 61, 70, 72, 81. Os considerados de alto risco, frequentemente associados às lesões de alto grau e às neoplasias invasoras, são representados principalmente pelos tipos 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73 e 82.(2) Os tipos 16 e 18 são considerados os mais prevalentes nos casos de câncer cervical invasivo, compreendendo 70% do total dessas neoplasias,(3) sendo que o subtipo HPV 16 é responsável por aproximadamente metade de todos os cânceres cervicais.(4-6)
O risco oncogênico está diretamente relacionado ao comportamento do genoma do vírus no núcleo da célula hospedeira. Os HPVs de baixo risco oncogênico tendem a manter o seu DNA íntegro, circular e epissomal, e a replicação do genoma viral é extracromossômica, diferente dos HPVs de alto risco oncogênico, cujas fitas de DNA circular se abrem, sofrem deleções e se integram ao genoma da célula hospedeira.(7,8)
Assim, nas lesões malignas, o DNA viral encontra-se integrado aos cromossomos da célula hospedeira e não acontece replicação viral. Há inativação da expressão da proteína E2 (controle trascricional/ replicação viral), que funciona como regulador negativo da expressão dos oncogenes E6 e E7 (oncoproteínas). Essa integração do DNA do HPV promove a imortalização celular, pois desregula a expressão dos E6 e E7, que interagem com genes supressores tumorais p53 e proteínas RB (proteína do retinoblastoma), respectivamente. Este processo prejudica a função do gene oncossupressor, com reparação do DNA, diminuição de apoptose e eventual morte celular. As mutações cromossômicas causam modificações funcionais como perda de heterozigose e proto-oncogene e ativação de mecanismos que permitem a indução da carcinogênese cervical.(9-11)
Assim, quando o indivíduo é infectado pelo HPV, as células do epitélio sofrem maturação e multiplicação acelerada, induzidas pelas oncoproteínas do vírus (E1 a E7, L1, L2 e LCR), gerando um processo que, se não detectado, pode evoluir para um processo neoplásico maligno.(12) Essa progressão é variável, dependendo da resposta do indivíduo, podendo variar até vinte anos, facilitando a detecção das lesões pré-neoplásicas precocemente no exame citopatológico de Papanicolaou.(13)
O vírus do HPV infecta apenas os seres humanos, homens e mulheres independentemente da idade, mas principalmente em idade reprodutiva.(14-16) A infecção viral ocorre quando há microlesões nas células basais do epitélio escamoso no colo do útero, onde o vírus penetra, liberando seu DNA, replicando-se e podendo permanecer em estado latente por vários anos, sem provocar manifestações clínicas ou subclínicas.(17)
Em algumas pessoas, a infeção por HPV é persistente e causa verrugas ou lesões pré-malignas e, em alguns casos, a lesão pode regredir naturalmente.(18) A infecção por HPV pode não induzir imunidade natural e, além disso, pode ocorrer contato com outro tipo viral.(15) Estudos epidemiológicos comprovam que apenas a presença do HPV por si só não é responsável pela carcinogênese cervical, mas, sim, sua persistência associada a fatores de risco, como início precoce da vida sexual, múltiplos parceiros sexuais, resposta imunológica do hospedeiro, uso de contraceptivos orais, tabagismo e a presença de doenças sexualmente transmissíveis.(19)
Coilocitose
Característica patognomônica (característica de uma doença específica), reconhecida na infecção pelo HPV, é identificada pelo aparecimento de células com grande halo perinuclear ou coilocitóticas, nas camadas diferenciadas do epitélio escamoso.(20) Caracterizadas por serem indicadores chave da infecção subclínica pelo HPV, as alterações morfológicas associadas à infecção pelo vírus podem ser usadas como parte da triagem do exame de Papanicolaou para o câncer do colo do útero.(21) O coilócito é específico da infecção pelo HPV, embora nem sempre esteja presente nos esfregaços citológicos.(21)
O coilócito é uma célula escamosa madura (intermediária ou superficial), que exibe uma cavitação perinuclear bem demarcada (halo perinuclear) com condensação periférica do citoplasma. Esse aro citoplasmático condensado que circunda frequentemente a cavitação perinuclear, dá à célula a aparência desbotada (ou de halo) em torno do núcleo displásico.(22) No entanto, a gênese do vacúolo citoplasmático permanece incerta, particularmente porque tanto a replicação do DNA do HPV como a montagem do virion ocorrem exclusivamente no núcleo.(22)
O núcleo dessa célula é displásico, geralmente aumentado de volume e hipercromático, similar àqueles das células da displasia leve. Pode haver binucleação ou multinucleação, embora esta última seja mais rara. As demais alterações nucleares incluem aumento do tamanho, núcleo excêntrico e hipercromático, cromatina grosseira e membranas nucleares irregulares, que podem estar comumente presentes na neoplasia intraepitelial cervical (LSIL).(23,24)
A coilocitose é observada em infecções por HPV de baixo e alto risco. E apenas nas camadas superiores e bem diferenciadas do epitélio escamoso estratificado, e é nessas camadas (e especificamente nos coilócitos) que as proteínas do capsídeo viral são expressas e agrupadas em vírions infecciosos.(25)
A morfologia coilocítica resulta da proteína E4 do vírus, que atua para romper o citoesqueleto da célula escamosa. Krawczyk et al. sugerem que as proteínas do HPV E5 e E6 trabalham juntas para promover a formação e fusão de cavitações perinucleares. Essa fusão provavelmente cria a grande cavitação que distingue as células infectadas pelo HPV, dando-lhes sua aparência desmarcada.(25)
As proteínas E5 e E6 de ambos os HPVs de baixo e alto risco cooperam para induzir a formação de coilócitos em células cervicais humanas in vitro. Importante, a E5 está presente nessas membranas de vacúolos, e seu terminal C é necessário para a formação de vacúolos.(25)
Embora a presença de coilócitos em esfregaços cervicais e amostras de biópsia seja característica da infecção por HPV, o papel biológico da coilocitose é incerto. A vacuolização do citoplasma perinuclear pode levar ao aumento da fragilidade celular, aumentando assim a saída viral e a infecção. Foi sugerido anteriormente que a proteína E4 do HPV possa promover a liberação viral na camada superior do epitélio, alterando a montagem do envelope cornificado e do citoesqueleto de queratina, e é possível que as proteínas E4 e E5 possam cooperar na potencialização do vírus.(16)
Embora os métodos moleculares estejam disponíveis para a detecção de infecções por HPV no trato genital feminino, a presença de coilócitos em exames de Papanicolaou e biópsias cervicais continuam sendo fundamentais para o diagnóstico patológico.(25) A gênese viral dos coilócitos é um pouco enigmática porque a maioria das proteínas do HPV está localizada no núcleo onde ocorre replicação e montagem viral.(22)
Lesões pré-cancerosas
São lesões que se desenvolvem na região cervical e podem ser classificadas como:
- Lesão intraepitelial escamosa de baixo grau (LSIL), ou NIC I (Neoplasia intraepitelial cervical Grau I), nas quais as alterações citológicas limitam-se ao terço do epitélio de revestimento da cérvice e quase sempre se encontra efeito citopático compatível com HPV;
- Lesão intraepitelial escamosa de alto grau (HSIL), também chamada de NIC II (Neoplasia intraepitelial cervical grau II) ou NIC III (Neoplasia intraepitelial cervical grau II), que atinge acima de 50% do epitélio pavimentoso de revestimento do colo uterino;
- Carcinoma in situ (NIC III), que abrange toda a espessura epitelial;
- Adenocarcinoma in situ (AIS), que são alterações semelhantes à NIC III, só que em células glandulares da cérvice; e
- Carcinoma invasor, compreendendo células escamosas com grande variação de forma, núcleo e tamanho.(15)
As alterações citológicas provocadas por esse vírus são descritas, de acordo com a Classificação de Bethesda, como lesão intraepitelial escamosa de baixo grau – LSIL.(26) Entre os efeitos citopáticos associados à infecção pelo vírus está a coilocitose.
Considerando a escassez de trabalhos no meio científico que expliquem com maior profundidade os mecanismos responsáveis pelas características citológicas conhecidas como coilocitose, o presente trabalho visa aprofundar o entendimento em relação às características citológicas decorrentes da infecção pelo HPV, por meio da produção de um atlas e a descrição dos mecanismos moleculares e celulares responsáveis por essa caracterização citológica. O seu uso poderá ser empregado no apoio ao diagnóstico, estudo e também na educação continuada, facilitando o entendimento desse assunto tão complexo e ao mesmo tempo comum no campo da citologia.
MATERIAL E MÉTODO
Trata-se de uma pesquisa exploratória, que visa proporcionar maior familiaridade com as características citológicas e o entendimento da transformação celular pelo vírus do HPV.
Inicialmente realizou-se uma pesquisa bibliográfica, utilizando as bases de dados National Center for Biotechnology Information, U.S. National Library of Medicine (PubMed – NCBI), Medical Literature Analysis and Retrieval System on-line (Medline) e Scientific Electronic Library Online (SciELO). Para a seleção da amostra, foram utilizados como critérios de inclusão os artigos publicados em Português e Inglês, indexados nas referidas bases de dados.
Concomitantemente ao levantamento de dados, foram geradas imagens microscópicas fotografadas a partir da objetiva do microscópio de óptico. As lâminas incluídas foram provenientes do arquivo de lâminas dos professores do curso de Pós-Graduação em Citopatologia Diagnóstica da Universidade Feevale.
Das questões éticas implicadas na pesquisa, a confidencialidade dos dados dos pacientes foi preservada, bem como a identidade dos mesmos. Como se trata de arquivo de lâminas de propriedade dos laboratórios, não é necessário TCLE (Termo de consentimento livre e esclarecido).
Figuras.
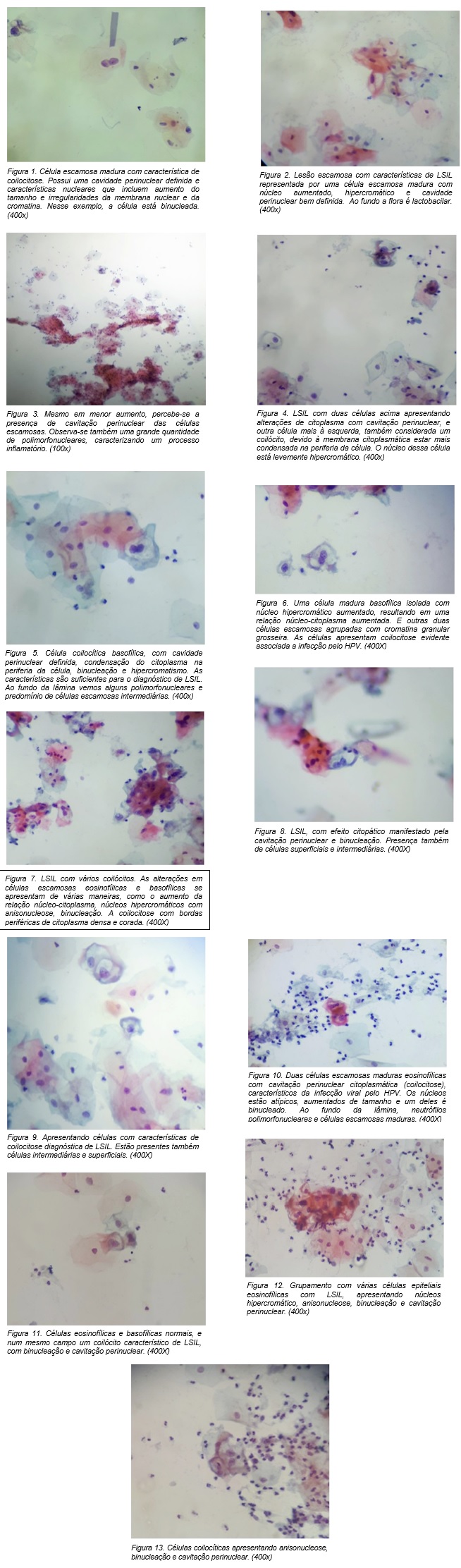
RESULTADOS
Os casos incluídos foram coletados por meio da técnica de citologia convencional corados pela Técnica de Papanicolaou.
CONCLUSÃO
O uso desse atlas virtual busca demonstrar a realidade na rotina em citopatologia. As imagens capturadas através da objetiva de um microscópio visam aproximar o leitor da realidade, no momento em que transmitem as imagens praticamente sem edição. Portanto, as imagens capturadas retratando os diferentes tipos de coilócitos, auxiliam e complementam os estudos de imagens, fornecendo um maior embasamento e olhar crítico para a definição de diagnóstico.
Abstract
Introduction: Koilocytosis is a descriptive term derived from the Greek adjective koilos, which means hollow. It is pathognomonic, for the diagnosis of low grade squamous intraepithelial lesion (LSIL), a lesion related to human papillomavirus (HPV) infection. Objectives: This study aims to describe the elaboration of a virtual atlas that addresses the different morphologies attributed to HPV pathognomonic cells to koilocytosis. Methods: The study is based on the capture of microscopic images of pre-neoplastic and cervico-vaginal neoplastic lesions and also a review of the literature on the subject, performed by searching scientific articles in the bibliographic database. The images were captured with the aid of a smartphone camera attached to the optical microscope objective. Conclusion: The captured images portray the different types of koilocytes present in pre-neoplastic and neoplastic lesions of the cervix, help and complement the imaging studies, providing a greater background and critical eye for the definition of diagnosis.
Keywords
Uterine cervix; neoplasms; HPV
REFERÊNCIAS
- Fedrizzi EN. Epidemiologia da infecção genital pelo HPV. Rev Bras Pat Trato GenInf 2011;1(1):3-8.
- Munoz N, Bosch FX, de Sanjosé S, et al. Epidemiologic classification of human papiloma vírus types associated with cervical cancer. N Engl J Med. 2003 fev;348(6):518-27. doi: 10.1056 / NEJMoa021641.
- Zampirolo JA, Merlin JC, Menezes ME. Prevalência de HPV de baixo e alto risco pela técnica de biologia molecular (Captura Hibrida II®) em Santa Catarina. Rev. bras anal clin. 2007;39(4): 265-8.
- Zur Hausen H, de Villiers EM. Papilomavírus humanos. Annu Rev Microbiol. 1994; 48: 427-447.
- Bosch FX, de Sanjosé S. Capítulo 1: papilomavírus humano e câncer do colo do útero – carga e avaliação de causalidade. J Natl Cancer Inst Monogr. 2003; 31: 3-13.
- Baseman JG, Koutsky LA. A epidemiologia das infecções por papilomavírus humano. J Clin Virol. 2005; 32 (Suppl 1): 16-24.
- Munoz N, Castellsagué X, de González AB, Gissmann L. HPV in the etiology of human cancer. Vaccine. 2006 agost; 24:1-10. doi: https://doi.org/10.1016/j.vaccine.2006.05.115.
- Scheurer ME, Tortolero-Luna G, Adler-Storthz K. Human papillomavirus infection: biology, epidemiology and prevention. Int J Gynecol Cancer. 2005;15:727-46.
- Münger K, Howley PM. Human papillomavirus immortalization and transformation functions. Virus Res 2002;89(2):213-28.
- Doorbar J. The papillomaviruses life cycle. J Clin Virol. 2005;32:(1 Suppl):S7-15. Doi: 10.1016 / j.jcv.2004.12.006.
- Tyring SK. Human papillomavirus infections: epidemiology, pathogenesis, and host immune response. J Am Acad Dermatol. 2000;43:S18-26. Doi:10.1067 / mjd.2000.107807.
- Ferraz LC, Santos ABR, Discacciati MG. Ciclo celular, HPV e evolução da neoplasia intraepitelial cervical: seleção de marcadores biológicos. J Health Sci Inst. 2012;30(2): 107-11.
- Brigel APV, Rodrigues MPF, Vidal ECF. Análise dos laudos de Papanicolau realizados em uma unidade básica de saúde. Rev Cogitare Enferm. 2012;17:745-51. Doi: http://dx.doi.org/10.5380/ce.v17i4.30385.
- Milner, Danny A. (2015). Diagnostic Pathology: Infectious Diseases (em inglês). [S.l.]: Elsevier Health Sciences. p. 40.I
- Instituto Nacional de Câncer. Coordenação Geral de Ações Estratégicas. Divisão de Apoio à Rede de Atenção Oncológica. Diretrizes brasileiras para o rastreamento do câncer do colo do útero – Rio de Janeiro: INCA, 2011. Rio de Janeiro, 2011 [acesso em 17 de mar 2013].
- Hamborsky J, Kroger A, Wolfe S. Centros de Controle e Prevenção de Doenças. Epidemiologia e Prevenção de Doenças Preveníveis por Vacinas. 13ª ed. Fundação de saúde pública de Washington DC, 2015. [Acesso em 20 de agost 2019]. Disponível em: < https://www.cdc.gov/vaccines/pubs/pinkbook/index.html>.
- Souza DRA, Catão RMR. Importância do conhecimento sobre Papilomavírus Humano: Considerações gerais. Rev Bio Far, vol. 8, n. 2, 2011.
- Zur Hausen H. Papilloma viruses causing cancer: evasion from host-cell control in early events in carcinogenesis. J Natl Cancer Inst. 2000;92 (9):690-8. Doi: 10.1093 / jnci / 92.9.690.
- Coser J, Fontoura S, Belmonte C, Vargas VRA. Relação entre fatores de risco e lesão precursora do câncer do colo do útero em mulheres com e sem ectopia cervical. Rev. bras anal clin. 2012; 44(1):50-4.
- Reid R, Stanhope CR, Herschman BR, Booth E, Phibbs GD, Smith JP. Genital warts and cervical cancer. I. Evidence of an association between subclinical papillomavirus infection and cervical malignancy. Cancer. 1982 jul;50(2):377-87. Doi: 10.1002 / 1097-0142 (19820715) 50: 2 <377: aid-cncr2820500236> 3.0.co; 2-a
- Abadi MA, Ho GY, Burk RD, Romney SL, Kadish AS. Stringent criteria for histological diagnosis of koilocytosis fail to eliminate overdiagnosis of human papillomavirus infection and cervical intraepithelial neoplasia grade 1. Hum Pathol. 1998 Jan;29(1):54-59. Doi: 10.1016 / s0046-8177 (98) 90390-2
- Krawczyk E, Suprynowicz FA, Liu X, Y Dai, Hartmann DP, Hannover J, Schlegel R. Koilocytosis: uma interação cooperativa entre o oncoproteínas de papilomavírus humano E5 e E6. Sou. J. Pathol. 2008 set; 173(3):682-8.
- Ayre JE. The link between koilocytosis and human papillomaviruses Ann Clin Lab Sci 195136485-487. Cancer cytology of the uterus. Grune Stratton, New York, 1951 quoted by Hajdu SI.
- Koss LG, Durfee GR. Unusual patterns of squamous epithelium of the uterine cervix: cytologic and pathologic study of koilocytic atypia. Ann NY Acad Sci. 1956; 63:1245-1261.
- Yamamoto LS, Alves VA, Maeda, Longatto-Filho A, Utagawa ML, Eluf Neto J. Protocolo morfológico e lista-guia de citologia do colo uterino associada à infecção pelo papilomavírus. Rev Inst Med Trop São Paulo. 2004;46:189-193.
- Nayar R, Wilbur DC. Sistema Bethesda para relato de Citologia: definições, critérios e notas explicativas. 3aEdição, 2018; 611: 134.3(81).
Correspondência
Lisiane Cervieri Mezzomo
Universidade Federal de Ciências da Saúde de
Porto Alegre (UFCSPA)
- Sarmento Leite, 245 – Centro Histórico
90050-170 – Porto Alegre-RS, Brasil
