Avaliação dos métodos de controle interno da qualidade no Laboratório Clínico da Pontifícia Universidade Católica de Goiás
Alternative method Evaluation of internal quality control in the Clinical Laboratory of Pontifical Catholic University of Goiás
Fernando de Almeida Dias1
Kassya Lopes Epaminondas Martins2
Sérgio Henrique Nascente Costa3
- Acadêmico do curso de Biomedicina da Pontifícia Universidade Católica de Goiás (PUC Goiás) – Goiânia-GO, Brasil.
- Mestre em Biologia da Relação Parasito-Hospedeiro, Biomédica do LAC PUC Goiás – Goiânia-GO, Brasil.
- Doutor em Ciências da Saúde, Professor da Pontifícia Universidade Católica de Goiás – Goiânia-GO, Brasil.
Instituição: Pontifícia Universidade Católica de Goiás (PUC Goiás) – Goiânia-GO, Brasil.
Recebido em 26/06/2017
Artigo aprovado em 13/04/2018
DOI: 10.21877/2448-3877.201800590
Resumo
Objetivo: Analisar a confiabilidade e a eficácia dos métodos alternativos de controle interno de qualidade utilizados no Laboratório Clínico da PUC Goiás, entre setembro de 2016 a janeiro de 2017. Métodos: Foi realizada a avaliação dos métodos de dupla leitura através da estatística de Kappa, tabela de Rümke e teste T de Student, nas seções de parasitologia, hematologia e uranálise respectivamente. Para análise interlaboratorial se utilizou o teste de tipagem sanguínea e fator Rh. Avaliou-se ainda a eficácia do Algoritmo de Bull na seção de hematologia. Resultados: Na seção de parasitologia foi obtido um grau bom de concordância (0,79) entre ambos os leitores, já na hematologia foi encontrado um percentual de conformidade de (99,88%), enquanto que na uranálise a contagem de hemácias apresentou variância de (0,20578), leucócitos (0,92104), células epiteliais (0,85467), não caracterizando diferença significativa (p> 0,05). Durante a avaliação do Algoritmo de Bull foi detectada, em dois dias, valores que ultrapassaram o limite superior de erro (c±2dp) em relação ao parâmetro número de eritrócitos (RBC). Não foi observada discordância na avaliação de processos interlaboratoriais. Conclusão: A análise dos resultados revelou que os métodos alternativos avaliados apresentaram alto índice de confiabilidade, podendo ser utilizados na rotina laboratorial como auxílio na qualidade do processo analítico.
Palavras-chave
Controle de qualidade; Laboratório clínico; Avaliação de processos
INTRODUÇÃO
O histórico da qualidade está fortemente ligado à revolução industrial da década de 1920, com ênfase nas indústrias bélicas, que, em decorrência da Primeira Guerra Mundial, aumentaram a produção de armamentos. Desse modo, surgiu então a necessidade de avaliar a qualidade do produto final, com o intuito de evitar a comercialização do mesmo de forma defeituosa, constituindo, assim, a primeira fase de evolução da qualidade. Em um segundo momento passa a existir a preocupação em todos os procedimentos da produção, tendo-se o entendimento de que fatores, como matéria-prima e profissional responsável pela operação, bem como equipamentos utilizados no processo, podem afetar direta ou indiretamente na variabilidade do produto.(1)
O conceito de qualidade na área da saúde tem alcançado um nível maior de interesse, sobretudo no âmbito laboratorial, graças ao notável crescimento tecnológico, aos avanços em pesquisas, à solicitação frequente de testes laboratoriais mais complexos e específicos, à alta competitividade no mercado de trabalho e um crescente nível de exigências por parte de usuários dos serviços laboratoriais.(2)
Nas áreas da saúde e industrial, a qualidade apresenta características semelhantes nas quais diversos estabelecimentos de saúde têm se adequado aos anseios dos clientes, bem como às exigências relacionadas à qualidade, que são consideradas como obrigatoriedade para a sobrevivência do laboratório clínico no mercado, tendo como prioridade o bem-estar e o contentamento do paciente e médico assistente.(1,3)
Em consequência, o controle de qualidade (CQ) é definido como o conjunto de metodologias e procedimentos operacionais que têm como finalidade monitorar o cumprimento dos requisitos específicos da qualidade, sendo dividido em Controle Externo de Qualidade (CEQ) e Controle Interno de Qualidade (CIQ). Assim, o CEQ envolve a verificação do correto desempenho dos sistemas analíticos em que se faz o uso de ensaios de proficiência e comparações interlaboratoriais. Por outro lado, o CIQ é feito em conjunto com as amostras dos pacientes e tem como objetivo avaliar se o sistema analítico apresenta resultados dentro dos intervalos pré-estabelecidos.(4)
De tal modo, para a realização do CIQ são utilizados materiais que podem ou não apresentar valores conhecidos, com a finalidade de verificar se a variabilidade das análises está dentro de limites aceitáveis e, também, identificar inconformidades para garantir a melhoria das atividades realizadas no laboratório clínico.(4,5)
Para padronizar as diversas ações no Laboratório Clínico, em 2005 foi elaborada e instituída a Resolução da Diretoria Colegiada de 2005 (RDC 302/2005), que foi parte fundamental na adesão do controle interno de qualidade por parte dos laboratórios clínicos brasileiros, que, durante cerca de 30 anos, utilizavam o CIQ como ferramenta alternativa de controle de qualidade. Com a criação da referida resolução, o uso do CIQ se tornou obrigatório para o funcionamento do laboratório.(2,4)
Na implementação de um CIQ com eficácia é necessária a escolha de um controle ideal para utilização em que geralmente são usados controles comerciais em concordância com a determinação da RDC 302/2005. A resolução exige que todos os laboratórios clínicos devem empregar preferencialmente controles comerciais e que, na ausência destes, poderão ser utilizadas metodologias alternativas de controle de qualidade que possibilitem analisar os parâmetros de precisão e exatidão dos sistemas analíticos nas diversas seções técnicas do laboratório clínico.(4)
Uma das estratégias que podem ser utilizadas é o controle alternativo de qualidade, que vem sendo empregado nas seções técnicas de bioquímica e imunologia, como, por exemplo, o uso de pool de soro e os chamados soros positivos e negativos. Na hematologia se observa o uso do algoritmo de Bull, repetição de amostras com base em parâmetros globais e a dupla leitura microscópica na avaliação diferencial de células, a utilização da estatística de Kappa na parasitologia e o teste T de Student na uranálise.(6,7)
Em situações onde não há a reprodutibilidade dos resultados laboratoriais, entende-se que podem ter ocorrido anormalidades no processo analítico, que poderiam resultar em erros nos exames. Tais erros podem ser considerados aleatórios quando ocorrem uma vez na rotina, ou sistemáticos quando é observado o mesmo padrão de erro em rotinas subsequentes.(8)
Desta forma, considerando a importância do controle interno de qualidade no laboratório clínico e a dificuldade na obtenção de controles comerciais para alguns exames, o presente estudo teve o objetivo de avaliar a eficácia dos métodos alternativos de controle interno de qualidade no Laboratório Clínico da Pontifícia Universidade Católica de Goiás – PUC Goiás (LAC PUCGO).
MATERIAL E MÉTODOS
O presente estudo foi realizado no Laboratório Clínico da PUC Goiás durante o período de setembro de 2016 a janeiro de 2017, tendo como objetivo analisar os métodos alternativos de controle interno de qualidade a fim de avaliar sua funcionalidade, confiabilidade e a facilidade de utilização.
Tipos de controle alternativos avaliados.
Controle Interlaboratorial
A avaliação do método alternativo de controle interlaboratorial ocorreu por meio da análise comparativa de testes de tipagem sanguínea e fator Rh entre o LAC PUC GO e um segundo laboratório. Amostras aleatórias foram selecionadas de acordo com a demanda semanal do exame e enviadas ao laboratório comparativo, que, após a análise da amostra, enviou o laudo ao LAC PUC GO para comparação de resultados.
Algoritmo de Bull
O Algoritmo de Bull(9) ou Controle X-bar é uma ferramenta auxiliar encontrada nos analisadores mais modernos, que se baseia na avaliação da média dos pacientes ao longo de um tempo, com o desígnio de auxiliar o laboratório na avaliação do perfil de pacientes de sua rotina.(15)
O método foi avaliado durante o período de cinco meses. As médias consistiram exclusivamente a partir de amostras de vinte pacientes da rotina e não foram incluídos controles comerciais ou de autocalibração. Os pacientes que apresentaram resultados muitos discrepantes (outliers) foram excluídos e considerados fora dos limites de aceitação. As médias calculadas foram incorporadas ao gráfico X-bar e posteriormente analisadas no software ExcelÒ2016 para construção dos gráficos.
Dupla Leitura
Para a avaliação do método de dupla leitura foram escolhidas e analisadas, semanalmente, lâminas aleatórias das seções de hematologia, parasitologia e uranálise. Após a leitura realizada pelo primeiro observador, também, posteriormente, foram observadas por um segundo microscopista, devidamente habilitado e que não possuía conhecimento prévio a respeito dos resultados das análises selecionadas. Para a avaliação de conformidade da leitura das lâminas hematológicas foi utilizada a tabela construída por C.L Rümke.(10) Já na detecção de variação entre os dois observadores, a seção de uranálise foi realizada pelo teste T de Student, enquanto que as lâminas parasitológicas foram avaliadas pelo índice de Kappa de Cohen.(11)
RESULTADOS
Durante a análise do controle interlaboratorial foram analisadas 15 amostras de tipagem sanguínea e fator Rh, não sendo observada variação entre os resultados do laboratório avaliado e o segundo laboratório em que foi realizado o controle interlaboratorial.
A dupla leitura na seção de hematologia se constituiu durante quatro semanas, fazendo-se a análise de quatro lâminas aleatórias semanais, desta forma, totalizando 16 lâminas mensais. A partir da análise, com a tabela de Rümke, foi observada uma concordância de (99,88%) entre os dois observadores, ou seja, o percentual de discordância foi de apenas (0,12%). Assim detectando a não concordância na contagem de linfócitos da semana dois, na lâmina 2, e nos valores contados de monócitos na semana quatro, na lâmina 1. Durante a análise da primeira e terceira semana não foram observadas discordâncias que fugissem aos valores da tabela de Rümke. (Tabela 1).
Na seção de parasitologia foram analisadas 19 amostras de fezes. A concordância observada foi de 0,79, enquanto a concordância esperada foi 0,60. Conforme o valor de Kappa houve um grau de concordância classificado como “bom”, pois se situou entre o intervalo de 0,60 – 0,79.
Na seção de uranálise ocorreu a leitura de 20 amostras de urinas aleatórias da rotina laboratorial. Assim, a contagem de hemácias apresentou variância de (0,20578), leucócitos (0,92104), células epiteliais (0,85467), ou seja, não apresentaram diferença significativa (p> 0,05).
Durante o período de avaliação do Algoritmo de Bull foi observada discreta ultrapassagem do limite superior pelo índice (Células Vermelhas do Sangue) RBC, retornando para os valores normais após um intervalo de dois dias consecutivos. Em continuidade, os demais padrões hematológicos não apresentaram valores que ultrapassassem a Média de ± 2 DP, conforme a observação das Figuras 1, 2, 3, 4, 5 e 6.
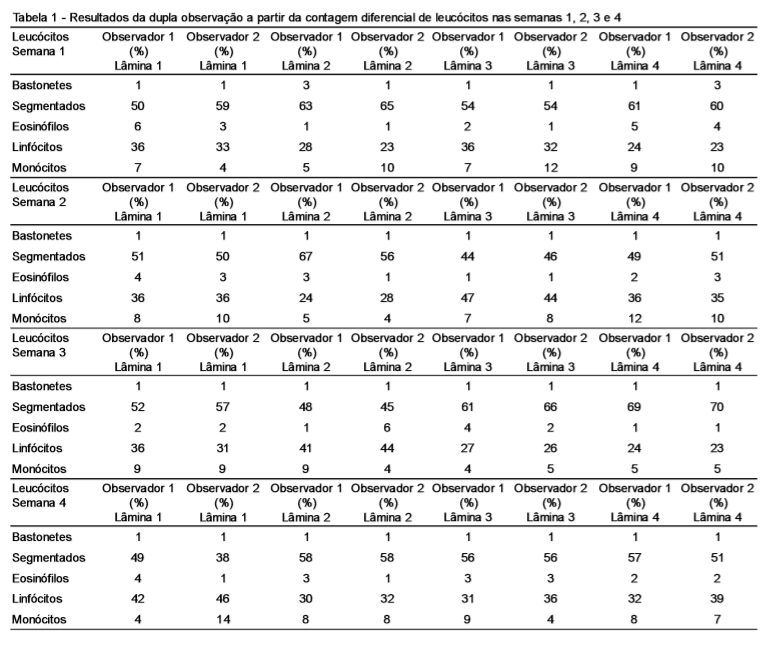
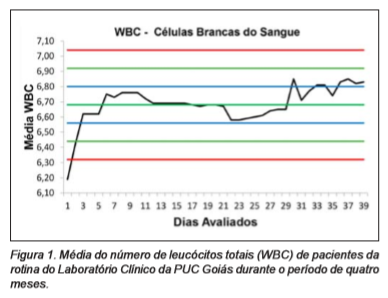
Figura 1. Média do número de leucócitos totais (WBC) de pacientes da rotina do Laboratório Clínico da PUC Goiás durante o período de quatro meses.
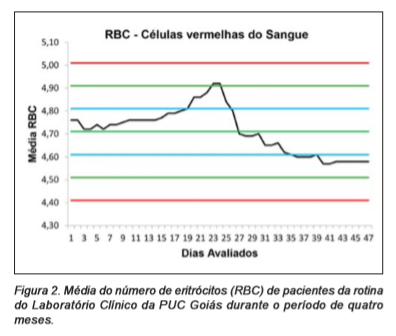
Figura 2. Média do número de eritrócitos (RBC) de pacientes da rotina do Laboratório Clínico da PUC Goiás durante o período de quatro meses.
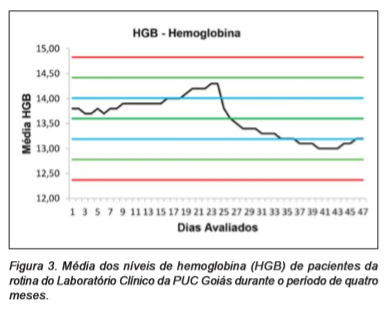
Figura 3. Média dos níveis de hemoglobina (HGB) de pacientes da rotina do Laboratório Clínico da PUC Goiás durante o período de quatro meses.
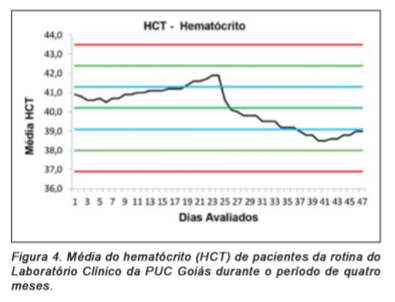
Figura 4. Média do hematócrito (HCT) de pacientes da rotina do Laboratório Clínico da PUC Goiás durante o período de quatro meses.
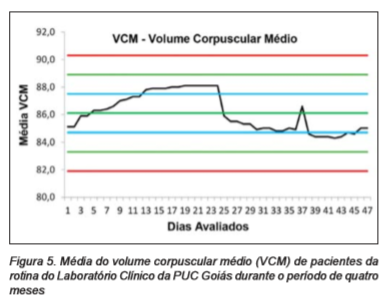
Figura 5. Média do volume corpuscular médio (VCM) de pacientes da rotina do Laboratório Clínico da PUC Goiás durante o período de quatro meses
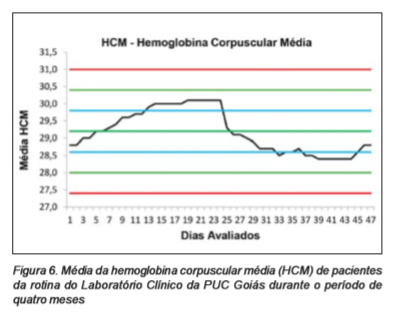
Figura 6. Média da hemoglobina corpuscular média (HCM) de pacientes da rotina do Laboratório Clínico da PUC Goiás durante o período de quatro meses
DISCUSSÃO
A RDC 302 de 2005 estabelece o uso obrigatório do CIQ na rotina laboratorial com o desígnio de avaliar a qualidade do sistema analítico, por conseguinte, fazendo o uso de amostras conhecidas. Os critérios de aceitação variam de acordo com o tipo de material analisado e a metodologia utilizada, uma vez que os controles utilizados podem ser de origem comercial ou poderão ser usadas formas alternativas de controle descritas na literatura.(4,6)
Na seção de hematologia, no que se refere à análise morfológica, foi utilizada a tabela de Rümke, que é uma estatística para avaliar a contagem diferencial de leucócitos em distensões sanguíneas que permite a contagem de 100, 200, 500 e 1.000 leucócitos, apresentando assim um intervalo de confiança de 95% para leucócitos em diferentes concentrações. A variação da contagem dependerá do total de células contadas, à vista que quanto maior o (n), menor será o índice permitido de variâncias entre as contagens.(12) Neste estudo, no decorrer de quatro semanas, foi realizada a contagem diferencial de leucócitos em distensões sanguíneos e posteriormente o método de dupla leitura se baseando nos valores da tabela Rümke.
Assim, dois valores excederam a referência preconizada por Rümke. Na semana 2, o primeiro microscopista observou 24% de linfócitos, enquanto que o segundo encontrou 38%, ou seja, ultrapassou o limite estabelecido pela tabela de Rümke, pois a mesma estipula que, em contagens de 20 a 25 células, a variação aceitável para um segundo observador é de 12,7 a 29,2. Na semana 4, o microscopista 1 obteve a contagem de 4% de monócitos em total de 100, enquanto que o segundo microscopista realizou a contagem de 14% de células monocíticas, sendo que a variação em contagens de quatro células é de 1,1 a 9,9. Nas demais semanas não foram observadas variações significativas entre os dois microscopistas. As variações observadas nas leituras das lâminas podem ser justificadas como sendo possíveis erros aleatórios, tendo em vista que não ocorreram com grande frequência,(2,8) assim como possível subjetividade na avaliação morfológica pelos microscopistas ou provável erro no processo de confecção das lâminas microscópicas.
Como método alternativo para a seção de parasitologia, utilizou-se o coeficiente de Kappa, empregado geralmente para dados de caráter nominal com a função de fornecer o grau de concordância entre dois observadores que realizaram uma mesma análise.(12) Os valores observados nas leituras das lâminas de parasitologia foram considerados bons (0,79) em uma escala Kappa de 0,60-0,79, todavia cabe ao laboratório clínico definir os critérios de aceitação.
Na seção de uranálise, de acordo com o teste T de Student, não foram observadas variações significativas entre os dois microscopistas nas lâminas analisadas durante o período do presente estudo. Logo, esse resultado demonstra a eficácia do método de dupla leitura, assim como o desempenho dos microscopistas frente à rotina do laboratório em estudo.
Métodos para padronização da análise microscópica são de extrema importância para a garantia da qualidade dos resultados gerados pelo laboratório clínico. Existe uma série de variáveis envolvidas, desde a coleta do material biológico, a confecção das lâminas, a capacitação do pessoal envolvido, findando-se, portanto, na liberação do laudo.(13,14)
O resultado da avaliação do controle interlaboratorial apresentou 100% de concordância entre o laboratório avaliado e o segundo laboratório utilizado para a comparação; assim, são excluídas, portanto, possíveis falhas no sistema analítico e nas fases pré-analítica e pós-analítica nestas análises.
O algoritmo de Bull utiliza exclusivamente pacientes da rotina laboratorial excluindo aqueles que apresentam valores alterados em alguns dos padrões hematológicos avaliados, pois, para a obtenção da média alvo do algoritmo, deve-se fazer a seleção de resultados normais ou que apresentam leve alteração e fazer a exclusão de valores discrepantes utilizando-se uma média e até ± 2 desvios-padrões. Este controle tem como função avaliar quesitos técnicos do contador hematológico, tais como a deterioração do reagente, a sensibilidade dos flag, assim como o perfil da comunidade atendida pelo laboratório clínico. Tem sua aplicação restrita a índices que não apresentam grandes variações no indivíduo, apresenta baixa sensibilidade em casos de erros aleatórios e parâmetros que apresentam alta variação.(15) No presente estudo avaliou-se a metodologia do algoritmo de Bull como controle interno em hematologia, durante o período de estudo, utilizando-se vinte pacientes como estipula o método.
A discreta ultrapassagem dos índices de RBC no limite superior ocorreu durante dois dias consecutivos e logo após os valores retornaram para a normalidade. Esta observação é aceitável, uma vez que a literatura afirma que, durante a implantação do Algoritmo de Bull, na seção de hematologia, são aceitos valores normais e discretamente alterados, excluindo-se apenas aqueles que apresentam resultados com grande discrepância (outliers).(15)
O resultado da média móvel dentro dos limites superior e inferior estabelecido, apresentando apenas ligeira ultrapassagem em um dos padrões, pode ser justificado pelo perfil de pacientes atendidos no laboratório clínico em estudo, que presta serviço ambulatorial. Nas rotinas que atendem pronto-socorro e UTI podem ser detectados frequentemente valores que ultrapassam os limites de tolerância aceitáveis. Fato esse justificado pelo estado patológico desses indivíduos.
CONCLUSÃO
Com base nos resultados obtidos nesse estudo, pode-se afirmar que os métodos alternativos de controle interno de qualidade aqui avaliados apresentam grande confiabilidade, desde que os profissionais envolvidos nos processos estejam em constante atualização de seus conhecimentos, como é notório na dupla leitura.
A normativa que regulamenta o funcionamento dos laboratórios clínicos fornece prioridade ao uso de amostras comerciais para serem utilizadas em controle interno. No entanto, nas seções ou exames em que não são disponibilizadas amostras comerciais, torna-se fundamental e necessário o emprego de métodos alternativos, os quais demonstraram ser eficientes no presente estudo.
Abstract
Objective: To analyze the reliability and effectiveness of alternative methods of internal quality control used at the Clinical Laboratory of PUC Goiás from September 2016 to January 2017. Methods: The evaluation of double reading methods was performed using the Kappa statistic, Rümke’s table and Student’s T-test, in the parasitology, hematology and uranalysis sections, respectively. For the interlaboratory analysis, blood typing and Rh factor were used. The effectiveness of the Bull Algorithm in the hematology section was also evaluated. Results: In the parasitology section, a good degree of concordance (0.79) was obtained between both readers, whereas in hematology a percentage of compliance was found (99.88%), while in uranalysis the red cell count presented a variance of (0.20578), leukocytes (0.92104), epithelial cells (0.85467), not characterizing significant difference (p> 0.05). During the evaluation of the Bull Algorithm, values that exceeded the upper limit of error (c ± 2dp) in relation to the number of erythrocytes (RBC) were detected in two days. There was no disagreement in the interlaboratory evaluation. Conclusion: The analysis of the results showed that the alternative methods evaluated had a high reliability index and can be used in the laboratory routine as an aid in the quality of the analytical process.
Keywords
Quality control; Clinical laboratory; Process assessment
REFERÊNCIAS
- Vieira KF, Shitara ES, Mendes ME, Sumita NM. A utilidade dos indicadores da qualidade no gerenciamento. J Bras Patol Med Lab. 2011;47(3):201-10. Available from: http://www.scielo.br/scielo. php?script=sci_arttext&pid=S1676-24442011000300002&lng=en. http://dx
- Control Lab. Gestão da fase analítica do laboratório: Como assegurar a qualidade na prática. 1sted. Rio de Janeiro: Control Lab Controle de Qualidade para Laboratórios LTDA; 2011.
- Mendes ME. Avaliação da Implantação de um Sistema da Qualidade em um Laboratório Clínico Público [tese]. São Paulo: Faculdade de Medicina. 1998.
- Brasil. Agência Nacional de Vigilância Sanitária. Resolução da Diretoria Colegiada No 302 de 13 de outubro de 2005. Dispões sobre regulamento técnico para funcionamento de laboratórios clínicos Brasíli, DF: Diário Oficial da República Federativa do Brasil, Poder Executivo; 3 out 2005.
- Stempliuk VdA. Controle interno da qualidade para testes de sensibilidade a antimicrobianos: OPAS/ANVISA/SVS; 2006.
- Schons CD, Tavares RG. Proposta do uso de pool de sangue total como controle. J. Bras. Patol. Med. Lab. 2010;46(3):181-186. Available from: http://www.scielo.br/scielo.php? script=sci_ arttext&pid=S1676-24442010000300005&lng=en.http://dx
- Burtis CA, Ashwood ER. Tietz: Fundamentos de química clínica Rio de Janeiro: Guanabara Koogan; 1998.
- Nunes, Araújo MR Ed. Relatório da Avaliação do Controle Interno da Qualidade – CQI dos Laboratórios de Microbiologia da Rede Nacional de Monitoramento da Resistência Microbiana em Serviços de Saúde – Rede RM; 2008.
- Bull BS, Ellasroff R, Heilbron D. A study of various estimators for the derivation of quality control procedures from erythrocytes indices. Am J Clin Pathol. 1974;61(4):473-81.
- Rümkecl C. Variability of results in differential cell counts on blood smears. Triangle. 1960;4:154-8..
- Landis JR, Koch GG. The measurement of observer agreement for categorical data. Biometrics. 1977;33(1):159-74.
- Munhoz MAG, Junior M. Comparação intralaboratorial em microscopia. In Lab C. Gestão da fase analítica do laboratório como assegurar a qualidade. Rio de Janeiro: ControlLab Controle de Qualidade para Laboratórios LTDA; 2010. p. 95-116.
- Weyer K. Tuberculosis: part II Microscopy Quality Control: SA HealthInfo; 2006.
- Institute CCALS. Body analysis for cellular compositions; Approved Guideline – H56-A. 26(26); 2006.
- Control Lab. Controle de processo em hematologia. In Junior N, Munhoz MAG. Gestão da Fase Analítica do Laboratório: como assegurar a qualidade na prática.: ControlLab Controle de Qualidade para Laboratórios LTDA; 2012. p. 47-69.
Correspondência
Sérgio Henrique Nascente Costa
Av. Universitária 1.440, Setor Universitário
74605-010 – Goiânia-GO, Brasil
