Índice de recoletas em um laboratório privado de Salvador-BA no ano de 2019
Recollection index in a private laboratory of Salvador-BA in the year 2019
Beneli Santos Miranda¹
Marissandra Santana Santos²
Vanessa da Silva Brito3
1,2 Biomédica, Escola Bahiana de Medicina e Saúde Pública, discente do curso de Especialização em Análises Clínicas e Gestão Laboratorial. Salvador, Bahia, Brasil.
3 Professor Adjunto – Escola Bahiana de Medicina e Saúde Pública, curso de Especialização em Análises Clínicas e Gestão Laboratorial. Salvador, Bahia, Brasil.
Recebido em 25/06/2021
Aprovado em 01/12/2021
DOI: 10.21877/2448-3877.202102158
INTRODUÇÃO
Os exames laboratoriais são fundamentais no auxílio às decisões diagnósticas e terapêuticas. Os laboratórios clínicos vêm passando por constantes modificações na última década, com auxílio das evoluções tecnológicas objetivando garantir atendimento eficiente e seguro no menor tempo possível. Assim, conceitos administrativos foram incorporados à visão técnica para minimizar erros e melhorar a qualidade do serviço prestado.(1)
A fase pré-analítica envolve muitas etapas desde a requisição do exame e cadastro do exame na recepção do laboratório até a chegada da amostra biológica ao setor analítico. Essas etapas incluem: orientação ao paciente pelo requisitante; preparo do paciente e orientações quanto à coleta da amostra a ser realizada; cadastro dos exames na recepção do laboratório; verificação das etiquetas e material que será usado na coleta das amostras; registro de informação sobre data e hora da coleta da amostra biológica; recolher informações sobre interferentes analíticos, como uso de medicamentos, ingestão de bebida alcoólica, atividade física nas últimas horas, dentre outras; verificação da etiquetagem para identificação correta das amostras recebidas ou coletadas possibilitando rastreabilidade; procedimento de coleta de amostra biológica realizado corretamente; transporte e armazenamento até a etapa analítica.(2,3,4)
Por incluir tantas etapas e muitos participantes, a fase pré-analítica concentra a maior frequência de erros associados a exames laboratoriais. Esta fase vem sendo apontada por diversos estudos como a grande responsável pelos erros laboratoriais, por possuir processos menos automatizados. Estes problemas estão associados a variáveis pré-analíticas, pois essas variáveis podem ser fisiológicas (sexo, idade, raça, exercício físico e jejum), variáveis de coleta e variáveis endógenas.(5,2)
Apesar do gradativo processo de automatização laboratorial, não há como substituir a figura dos coletadores (flebotomistas) em larga escala do processo de coleta do material biológico. É importante que os profissionais envolvidos nesse processo entendam que esta fase é crucial para um exame de qualidade.(6,7)
A ocorrência dos erros em qualquer uma das fases pode inferir de forma negativa no diagnóstico dos pacientes e na tomada de decisão terapêutica, sendo necessária a implantação de metodologias sistematizadas e mais rigorosas para rastreabilidade, detecção, classificação e redução destes erros, implementando indicadores laboratoriais que permitam avaliar a eficácia e eficiência do serviço. Dentre os indicadores mais comumente citados na literatura está o índice de recoletas, pois a classificação dos erros e da frequência em que ocorrem é uma medida valiosa para identificar prioridades para tomada de ações corretivas e preventivas.(8,9)
Os indicadores de recoletas são informações de natureza quantitativa ou qualitativa associada a um evento, possibilitando avaliações nas mudanças e tomadas de decisões. Além disso, o uso dos indicadores mostra falhas ou erros de um processo em relação ao número total, tendo como objetivo indicar problemas que precisam de ações preventivas e corretivas que ajudam a identificar os pontos fortes e fracos e oportunidades de melhoria e crescimento. O desempenho de um processo é satisfatório quando os indicadores estão dentro de um limite estabelecido pela organização.(10)
A busca de melhoria contínua nos serviços laboratoriais tem avançado, levando os laboratórios a participarem dos programas de Acreditação, que tem como objetivo a padronização de seus indicadores bem como a comparabilidade entre os laboratórios clínicos.(11) Tendo em vista esses aspectos, este estudo tem como objetivos descrever os índices de recoletas no período de um ano em um laboratório privado de análises clínicas, na cidade de Salvador – BA, identificando principais erros na fase pré-analítica e sua frequência.
MATERIAL E MÉTODOS
Trata-se de um estudo descritivo exploratório retrospectivo, no qual foram utilizados dados existentes nos arquivos de solicitação de recoleta do laboratório de análises clínicas, no qual foi realizado um levantamento de dados sobre interferentes laboratoriais e dados de recoletas em um laboratório clínico.
Para a realização do estudo foram considerados apenas os atendimentos das unidades ambulatoriais; os dados referentes aos atendimentos hospitalares não foram considerados nas análises estatísticas do presente estudo.
Obtenção dos dados
Os números de recoletas do período de janeiro a dezembro de 2019 e seus respectivos motivos foram extraídos através de relatório gerado pelo sistema SmartLab – v20.8 do laboratório, com prévia autorização através de carta de anuência dos responsáveis.
Análise dos dados
Após aquisição dos dados de recoletas foi realizada a tabulação através do software Microsoft Office Excel e, a partir disso, gráficos foram gerados e realizada a análise estatística descritiva através do software GraphPad Prism v.5.0 (Estados Unidos). Os números estão expressos em número absoluto (N), frequência (%), e suas respectivas medidas de tendências centrais, como em média e desvio padrão (Me±DP) e mediana e valores mínimos e máximos [Md (mín-máx)].
Considerações éticas
Neste estudo foram utilizados dados secundários coletados de registro em sistema da ferramenta de gestão da qualidade laboratorial, no qual não constam informações individuais ou pessoais das amostras dos pacientes, não sendo necessária a submissão do projeto a um Comitê de Ética em Pesquisa, conforme a Resolução nº 466/12 do Conselho Nacional de Saúde. Não há conflito de interesse entre os autores do artigo e o laboratório em questão.
RESULTADOS E DISCUSSÃO
No período de janeiro a dezembro de 2019 foram atendidos 567.214 pacientes, sendo estes divididos em 428.921 (75,6%) atendimentos ambulatoriais, 138.293 atendimentos hospitalares (24,4%) (Gráfico 1). Foram considerados para o presente estudo apenas os atendimentos ambulatoriais, sendo os meses de maio, julho e agosto com os maiores números de atendimentos (39.062, 39.437 e 39.545, respectivamente) e junho e dezembro os meses com menor número de atendimentos (29.676 e 28.632 respectivamente) (Tabela 1).
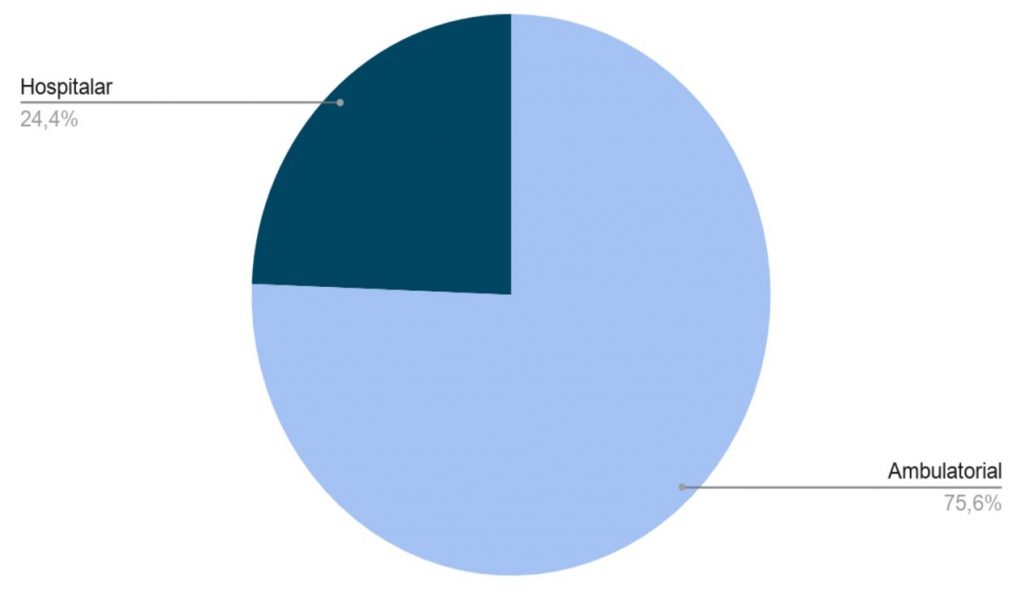
Gráfico 1. Distribuição da porcentagem anual dos atendimentos (ano 2019)
Tabela 1 – Número de atendimentos e solicitações de recoleta de amostra biológica por mês no ano de 2019
| Mês/2019 | N Abs. de atendimentos | N relativo de atendimentos (%) | N Abs. de recoletas | N relativo de recoletas (%) |
| Janeiro | 37.741 | 8,8 | 67 | 0,18 |
| Fevereiro | 35.386 | 8,3 | 48 | 0,14 |
| Março | 32.640 | 7,6 | 45 | 0,14 |
| Abril | 37.132 | 8,7 | 77 | 0,21 |
| Maio | 39.062 | 9,1 | 81 | 0,21 |
| Junho | 29.676 | 6,9 | 58 | 0,20 |
| Julho | 39.437 | 9,2 | 63 | 0,16 |
| Agosto | 39.545 | 9,2 | 89 | 0,23 |
| Setembro | 36.305 | 8,5 | 66 | 0,18 |
| Outubro | 37.777 | 8,8 | 89 | 0,24 |
| Novembro | 35.588 | 8,3 | 119 | 0,33 |
| Dezembro | 28.632 | 6,7 | 54 | 0,19 |
| TOTAL | 428.921 | 100 | 856 | 2,387 |
| Medidas de dispersão | ||||
| Me±DP | 35.743 ± 3651 | 8,3±0,8 | 71±21 | 0,20±0,05 |
| Md (mín-máx) | 36.720 (28.632 – 39.545) | 8,6 (6,7 – 9,2) | 66 (45 – 119) | 0,19 (0,14 – 0,33) |
Me±DP: média e desvio padrão; Md (mín-máx): mediana e valores mínimo e máximo; N Abs de atendimentos: número absoluto de pacientes atendidos a cada mês; N relativo de atendimentos: número relativo de pacientes atendidos a cada mês; N Abs de recoletas: número absoluto de recoletas solicitadas a cada mês; N relativo de recoletas (%): número relativo de recoletas solicitadas em cada mês.
No que se refere aos índices de recoleta, do total de pacientes atendidos em ambulatório (428.921) no ano de 2019, 0,2% dos pacientes em atendimento ambulatorial tiveram alguma solicitação de recoleta baseado nos indicadores de recoleta adotado pelo laboratório. Ao longo do ano de 2019 foram solicitadas em média 72±21 solicitações de recoletas de amostras biológicas. O mês de novembro foi o que apresentou maior taxa de recoleta e os meses de fevereiro e março as menores taxas.
Os indicadores identificados de recoleta a cada mês são observados os valores absolutos na Tabela 2 e valores relativos no Gráfico 3, sendo falha no procedimento da coleta o indicador mais frequente (19,2 ± 8,8), seguido pela presença de coágulo na amostra (17,4 ± 5,8) e falhas na área técnica e/ou no laboratório de apoio (13,5 ± 8,8), respectivamente. O indicador com menor frequência foi falha na etiqueta (0,08 ± 0,2), seguido por falha da recepção (1,7 ± 1,4) e urina derramada (1,9 ± 2,1), respectivamente (Gráfico 2).
Tabela 2 – Número absoluto de recoletas por indicador a cada mês no ano de 2019
| Mês/2019 | Hemólise | Triagem | Material Insuf. | Urina Derramada | Falha na recepção | Falha Apoio | Falha Coleta | Coágulo | Etiqueta | Total | |
| Janeiro | 0 | 4 | 2 | 2 | 3 | 12 | 17 | 27 | 0 | 67 | |
| Fevereiro | 7 | 3 | 2 | 2 | 2 | 9 | 11 | 11 | 1 | 48 | |
| Março | 4 | 3 | 1 | 1 | 1 | 4 | 20 | 11 | 0 | 45 | |
| Abril | 13 | 8 | 7 | 2 | 2 | 9 | 13 | 23 | 0 | 77 | |
| Maio | 10 | 10 | 7 | 5 | 0 | 13 | 20 | 16 | 0 | 81 | |
| Junho | 14 | 4 | 3 | 0 | 1 | 14 | 8 | 14 | 0 | 58 | |
| Julho | 7 | 4 | 2 | 1 | 1 | 15 | 21 | 12 | 0 | 63 | |
| Agosto | 10 | 7 | 5 | 0 | 2 | 21 | 19 | 25 | 0 | 89 | |
| Setembro | 7 | 6 | 9 | 0 | 1 | 16 | 13 | 15 | 0 | 67 | |
| Outubro | 6 | 3 | 6 | 7 | 3 | 6 | 33 | 24 | 0 | 88 | |
| Novembro | 12 | 4 | 2 | 2 | 5 | 37 | 39 | 18 | 0 | 119 | |
| Dezembro | 5 | 6 | 6 | 1 | 0 | 6 | 17 | 13 | 0 | 54 | |
| TOTAL | 95 | 62 | 52 | 23 | 21 | 162 | 231 | 209 | 1 | 856 | |
| Medidas de dispersão | |||||||||||
| Me±DP | 7,9 ± 4,0 | 5,2 ± 2,2 | 4,3 ± 2,6 | 1,9 ± 2,1 | 1,7 ± 1,4 | 13,5 ± 8,8 | 19,2 ± 8,8 | 17,4 ± 5,8 | 0,08 ± 0,2 | 71,3 ± 20,9 | |
| Md (mín-máx) | 7 (0 – 14) | 4 (3 – 10) | 4 (1 – 9) | 1,5 (0 – 7) | 1,5 (0 – 5) | 12,5 (4 – 37) | 18 (8 – 39) | 15,5 (11 – 27) | 0 (0 – 1) | 86,2 (45 – 119) | |
Me±DP: média e desvio padrão; Md (mín-máx): mediana e valores mínimo e máximo
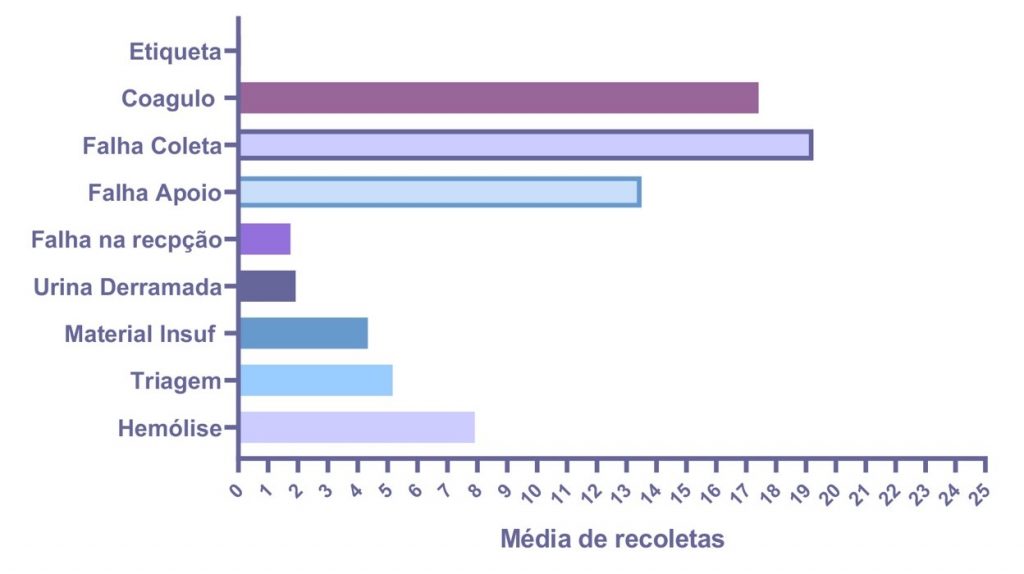
Gráfico 2. Média dos valores absolutos dos indicadores para recoletas no ano de 2019
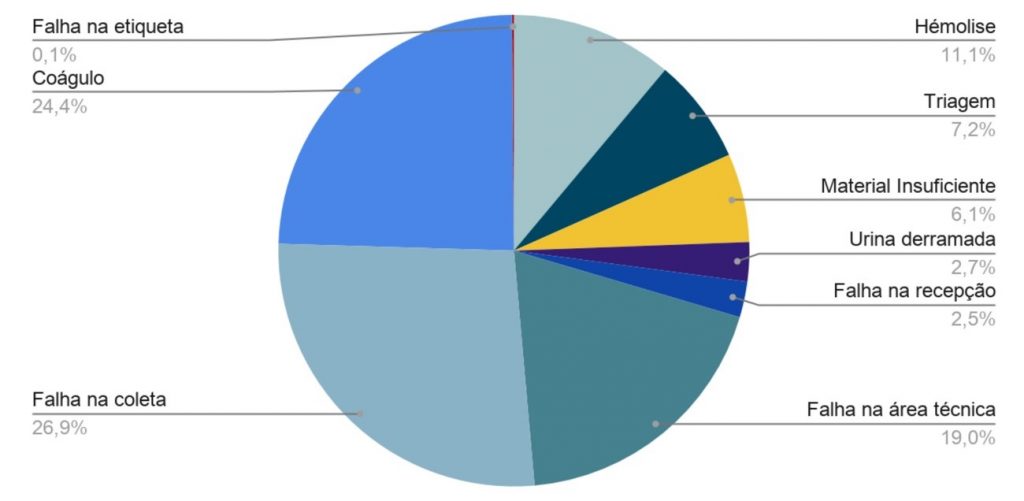
Gráfico 3. Distribuição da porcentagem dos indicadores de recoletas no ano 2019
A utilização desses indicadores no laboratório clínico permite ao gestor conhecer o desempenho das suas análises mensalmente, visando melhoria contínua da gestão da qualidade ao longo do tempo. Esses indicadores sinalizam para um bom desempenho de um processo quando confrontados com metas estabelecidas.(12)
O indicador laboratorial hemólise ocorre devido a uma série de fatores, como escolha da agulha de calibre pequeno, aspiração muito rápida (coleta com seringa), perda da veia durante a coleta, homogeneização brusca. Proporcionalmente à intensidade da hemólise, há alterações, como diminuição da contagem de eritrócitos, redução do hematócrito e da hemoglobina, interferindo nesses parâmetros da série vermelha. Além da hemoglobina, as hemácias contêm várias proteínas, enzimas, lipídios e carboidratos que podem interagir ou competir com reagentes de ensaio, ou elevar a quantidade do analito dosado em soro ou plasma. Há interferência da hemólise para alguns exames bioquímicos como: Aspartato aminotransferase (AST), alanina aminotransferase (ALT), Fosfatase alcalina (ALKP), Gama-glutamiltransferase (GGT), bilirrubinas, lactato desidrogenase (LDH), magnésio, creatinoquinase (CK), troponinas e os eletrólitos.(6,13-15)
A triagem é o local de manuseio e preparação para o transporte de amostras, sendo crucial para a identificação dos interferentes laboratoriais, desse modo, é importante certificar-se de que os tubos estejam corretamente encaixados na caçamba da centrífuga para evitar acidentes com material biológico e perda de materiais.(16-18)
Os materiais denominados como insuficientes são aqueles com baixo volume e/ou qualidade para realização do exame no laboratório clínico, sendo assim as amostras biológicas, sejam elas sangue total, soro, plasma, urina, fezes ou líquor, devem conter material suficiente para a realização da análise.(19,20)
Urina derramada acontece no ato do recebimento ou no processo de triagem, e portanto deve-se certificar que o coletor com urina esteja fechado adequadamente. O frasco de coleta e o saco coletor bem vedado podem evitar quedas acidentais, saída da tampa, e consequente perda do material.(20,21,7,22)
Falha da recepção ocorre durante o cadastro do paciente e registros dos exames solicitados na guia médica. É importante confirmar dados pessoais como: endereço, telefone, idade, sexo, gestação, utilização de medicamentos e jejum. Além das informações sobre dados clínicos do paciente, a quimioterapia, a radioterapia e as doenças crônicas também fazem parte do cadastro. O preenchimento inadequado no cadastro leva a repetições de exames desnecessárias.(23,5)
Falhas na área técnica ou no laboratório de apoio estão relacionadas com processo de conservação das amostras, coletor ou tubo inadequado, envio indevido, acidente com material biológico, identificação inadequada e volume de amostra impróprio.(24)
A falha na coleta está relacionada com o flebotomista, que tem papel importante nessa fase e deve respeitar os protocolos para a obtenção do material biológico. É preciso seguir a sequência dos tubos que serão utilizados, verificar o volume de sangue apropriado para cada tubo e realizar a homogeneização correta. Os recipientes com materiais de coletas deverão ser identificados durante o procedimento técnico.(25,26)
O coágulo ocorre devido a homogeneização insuficiente após a coleta e em situações de coleta difícil. Essas amostras são desprezadas, já que a formação do coágulo afeta os parâmetros avaliados no hemograma.(27)
Falha na etiqueta acontece durante impressão e posicionamento incorreto, levando à necessidade de reimpressão que ocasiona retrabalho na triagem de amostras, podendo gerar recoleta. O uso de código de barras para identificar amostras no ato da coleta garante a rastreabilidade de todo o processo técnico.(28,29)
As etapas de um procedimento pré-analitico
A fase pré-analítica do processo laboratorial envolve os procedimentos de preparo e coleta das amostras. Esses processos precisam ser realizados de acordo com os manuais de coleta para que os resultados não sejam comprometidos. Essa fase exige uma série de atividades interligadas e sistematizadas, e divide-se em: extralaboratorial e intralaboratorial.(9)
Na fase extralaboratorial inicia-se com solicitação de exames, avaliação do paciente e orientações de preparo do paciente para coleta. Os requisitos de cadastro do paciente seguem as recomendações da PALC e RDC 302.(5,7)
Desse modo, no consultório médico o profissional irá fornecer ao paciente as primeiras orientações e informações sobre os exames solicitados. Na recepção do laboratório inicia-se o processo de cadastro e orientações específicas de cada exame, como horário pré-definido, jejum, ingestão de bebidas alcoólica nas últimas 72 horas, a realização de exercício físico e outros. Além de informar ao paciente essas particularidades é importante ressaltar que para evitar erros as orientações devem ser entregues por escrito.(7,26)
No cadastro do paciente deve conter o número de registro de identificação gerado pelo laboratório, nome, idade e sexo do paciente, telefone, endereço, médico solicitante, horário do atendimento, exames e tipo de amostra. Em casos de menor de idade, contato do responsável. Dados importantes como medicação, tabagismo, etilismo e condições cronobiológicas devem ser fornecidos pelo paciente e são de extrema importância para análise técnica.(5)
Na fase intralaboratorial é realizada uma nova inspeção, confrontando-se a identificação do paciente, preparo para os exames solicitados e identificação do material coletado. O flebotomista irá identificar o paciente e verificar os exames para proceder com a coleta. Na coleta de sangue venoso deve-se respeitar a ordem dos tubos para que não haja contaminação e consequente interferente na análise dos exames. O Manual clinical and Laboratory Standards Institute (CLSI) padroniza tubo em escala distinguindo por cor.(30,31)
Após localizar o melhor local de acesso para perfusão, o profissional de coleta deverá realizar a lavagem das mãos, calçar as luvas e preparar o material na presença do paciente. Os materiais perfurocortantes devem ser desencapados somente no processo de punção, evitando assim acidentes. Agulha ou escalpe devem ser posicionados de forma que o bisel fique com face para cima e a posição em um ângulo de 45°C. Ao concluir a punção, a agulha é retirada acionando dispositivo de segurança e posterior descarte em local apropriado. O bloodstop é aplicado e o paciente é orientado a pressionar o local, com o objetivo de tamponar e não causar hematomas.(26)
Na triagem técnica as amostras coletadas são conferidas, preparadas e segregadas para o encaminhamento à central de análises e processamentos. O transporte das amostras biológicas deve ser realizado em recipientes isotérmicos, higienizáveis e impermeáveis, com o devido controle de temperatura e identificado com a simbologia de risco biológico.(32,33)
Embora os motivos de recoletas sejam indicadores de qualidade importantes para o laboratório clínico, indicando problemas que precisam de ações preventivas, não há consenso de limites determinado para a aceitabilidade. A meta estabelecida pela gestão do laboratório pesquisado é de no máximo 0,23% de recoletas mensais. Portando, os resultados da pesquisa demonstraram que a frequência de recoletas obtidas durante o período de um ano esteve dentro da meta prevista pela empresa.
CONSIDERAÇÕES FINAIS
No ano de 2019 houve um índice de solicitação de recoleta de amostra biológica excelente, com menos de 0,5% do total de pacientes atendidos em determinado laboratório de análises clínicas na cidade de Salvador-BA. O motivo de solicitação de recoleta mais frequente foi relacionado a erros no procedimento de coleta da amostra biológica e o menos frequente foi erro relacionado à etiqueta de identificação da amostra, indicando a necessidade de treinamentos e aprimoramentos dos profissionais que orientam ou executam a coleta de amostra biológica, e avaliação da qualidade e adequabilidade dos instrumentos e equipamentos utilizados nesta etapa.
Diversos fatores estão envolvidos nos erros pré-analíticos, por ser a fase menos automatizada no laboratório. Dada a importância da fase pré-analítica para obtenção de resultados e útil à prática médica, todos os segmentos de normas e precauções são essenciais para que erros sejam evitados. Deve haver especial atenção a todos os procedimentos dessa fase, para garantir a viabilidade das amostras a serem analisadas.
Apesar da crescente utilização de novas tecnologias, como automação e robótica, algumas atividades da coleta influenciam decisivamente no erro total e, consequentemente, no resultado analítico que o laboratório irá liberar. A padronização dos processos e a educação continuada são ferramentas imprescindíveis para essa finalidade.
As recoletas causam ao paciente incômodo por necessitar de retorno ao laboratório para uma nova coleta, além de gerar custos para a empresa e afetar a credibilidade do laboratório, deixando o paciente às vezes insatisfeito. A gestão da qualidade dos laboratórios clínicos é imprescindível para a garantia da qualidade e confiabilidade dos exames oferecidos por ele.
REFERÊNCIAS
- Horvath, A. R. From evidence to best practice in laboratory medicine. Clin. Biochem. Rev. 34, 47–60 (2013).
- Costa, V. G. Da & Moreli, M. L. Principais parâmetros biológicos avaliados em erros na fase pré-analítica de laboratórios clínicos: revisão sistemática. J. Bras. Patol. e Med. Lab. 48, 163–168 (2012).
- Fonseca, K. M. N. de L. Coleta de exames de rotina de urina. Recom. da Soc. Bras. Patol. Clínica/ Med. Lab. Fatores pré-analíticos e Interf. em ensaios Lab. 330 (2019).
- Corrêa, J. A. Garantia da Qualidade no Laboratório Clínico. (2019).
- BRASIL. MS– ANVISA. RDC 302. in RDC 302 (2005).
- Ialongo, C. & Bernardini, S. Phlebotomy, a bridge between laboratory and patient. Biochem. Medica 26, 17–33 (2016).
- Andriolo, Adagmar; Sumita, N. M. W. S. G. A. C. F. V. B. C. A. M. A. G. F. de O. C. E. dos S. F. C. A. de O. G. M. E. M. Recomendações da sociedade brasileira de patologia clínica/medicina laboratorial (SBPC/ML) : fatores pré-analíticos e interferentes em ensaios laboratoriais. (2018).
- SANTOS, P. R., Silva, C. L., Gall, M. C., Allyne, ; & Grando, C. Impacto nos custos por erros pré-analíticos em laboratório de análises clínicas Impact of pre-analytical errors on costs of clinical analysis laboratory. J Bras Patol Med Lab 57, 1–4 (2021).
- Corrêa, J. A. Garantia da Qualidade no Laboratório Clínico. (2019).
- Coriolano, N. L., Silva, I. C. R. & Lamounier, T. A. C. Analysis of the frequency of biological sample recollections as quality indicators in a clinical laboratory of Distrito Federal, Brazil. J. Bras. Patol. e Med. Lab. 52, 11–16 (2016).
- Tsai, E. R. et al. A critical review of laboratory performance indicators. Crit. Rev. Clin. Lab. Sci. 56, 458–471 (2019).
- Maronna, A., Souza, R. A. & Montes, F. C. O. F. Description of the quality indicators defined in the national reference laboratory in tuberculosis of CRPHF/Ensp/fiocruz by means of the process mapping methodology. J. Bras. Patol. e Med. Lab. 53, 165–176 (2017).
- Lippi, G. Systematic Assessment of the Hemolysis Index. in 157–170 (2015). doi:10.1016/bs.acc.2015.05.002.
- Heyer, N. J. et al. Effectiveness of practices to reduce blood sample hemolysis in EDs: A laboratory medicine best practices systematic review and meta-analysis. Clin. Biochem. 45, 1012–1032 (2012).
- Stankovic, A. K. & Smith, S. Elevated Serum Potassium Values. Pathol. Patterns Rev. 121, S105–S112 (2004).
- Lippi, G. et al. Preanalytical quality improvement. In pursuit of harmony, on behalf of European Federation for Clinical Chemistry and Laboratory Medicine (EFLM) Working group for Preanalytical Phase (WG-PRE). Clin. Chem. Lab. Med. 53, (2015).
- Simundic, A.-M., Baird, G., Cadamuro, J., Costelloe, S. J. & Lippi, G. Managing hemolyzed samples in clinical laboratories. Crit. Rev. Clin. Lab. Sci. 57, 1–21 (2020).
- Lippi, G. et al. Recommendations for detection and management of unsuitable samples in clinical laboratories. Clin. Chem. Lab. Med. 45, (2007).
- Zapelini, R. M. et al. Analysis of laboratory tests results of patients submitted to a clinical screening program. J. Bras. Patol. e Med. Lab. 52, 374–381 (2016).
- Codagnone, F. T. et al. The use of indicators in the pre-analytical phase as a laboratory management tool. J. Bras. Patol. e Med. Lab. 50, 100–104 (2014).
- Delanghe, J. R. & Speeckaert, M. M. Preanalytics in urinalysis. Clin. Biochem. 49, 1346–1350 (2016).
- Norma, N. & Urina, E. De. ABNT NBR 15.268:2005. 2005 (2005).
- Mrazek, C. et al. Errors within the total laboratory testing process, from test selection to medical decision-making – A review of causes, consequences, surveillance and solutions. Biochem. medica 30, 020502 (2020).
- Agarwal, R. Measurement of Errors in Clinical Laboratories. Indian J. Clin. Biochem. 28, 227–234 (2013).
- Lima-Oliveira, G. de S., Picheth, G., Sumita, N. M. & Scartezini, M. Controle da qualidade na coleta do espécime diagnóstico sanguíneo: iluminando uma fase escura de erros pré-analíticos. J. Bras. Patol. e Med. Lab. 45, 441–447 (2009).
- Laboratorial, S. B. D. P. C. / M. & Sociedade Brasileira de Patologia Clínica / Medicina Laboratorial. Coleta de Sangue Venoso. (2005).
- Narayanan, S. Preanalytical Issues Related to Blood Sample Mixing. Bloodgas.Org Classen, D. C., Resar, R., Griffin, F., Federico, (2005).
- Wagar, E. A., Stankovic, A. K., Raab, S., Nakhleh, R. E. & Walsh, M. K. Specimen Labeling Errors: A Q-Probes Analysis of 147 Clinical Laboratories. Arch. Pathol. Lab. Med. 132, 1617–1622 (2008).
- Dock, B. Improving the accuracy of specimen labeling. Clin. Lab. Sci. 18, 210–212 (2005).
- Lima-Oliveira, G. et al. Impact of the phlebotomy training based on CLSI/NCCLS H03-A6 – procedures for the collection of diagnostic blood. Biochemia Medica 342–351 (2012) doi:10.11613/BM.2012.036.
- Laboratory, C. and & Standards Institute. H03 A6 Procedures for the Collection of Diagnostic Blood Specimens by Venipuncture; Approved Standard. vol. 27 (2014).
- Laboratory, C. and & Institute, S. H18-A3 Procedures for the Handling and Processing of Blood Specimens ; Approved Guideline — Third Edition. CLSI document H18-A4 vol. 24 (2004).
- Laboratory, C. and & Institute, S. H21 A5 -Collection , Transport, and Processing of Blood Specimens for Testing Plasma-Based Coagulation Assays and Molecular Hemostasis Assays; CLSI Approved Guideline-Fifth Edition. H21-A5. Nccls vol. 28 H21-A5 (2008).
Correspondência
Vanessa da Silva Brito
Escola Bahiana de Medicina e Saúde Pública
Curso de Especialização em Análises Clínicas e Gestão Laboratorial
Av. Dom João VI, 275 – Brotas
Salvador – BA, CEP: 40290-000
E-mail: [email protected]
