Efetividade da administração de Omalizumabe para tratamento de pacientes com urticária crônica espontânea
Effectiveness of Omalizumabe administration for treatment of patients with spontaneous chronic urticaria
Débora Laureano de Souza1
Jhonata Pereira Muniz1
Thiago Mamoru Sakae2
Mariana Mangilli de Menezes3
1Estudante de Medicina da Universidade do Extremo Sul Catarinense – UNESC – Criciúma-SC, Brasil.
2Professor da Universidade do Sul de Santa Catarina – UNISUL – SC, Brasil.
3Professora da Universidade do Extremo Sul Catarinense – UNESC – Criciúma-SC, Brasil.
Instituição: Universidade do Extremo Sul Catarinense – UNESC – Criciúma-SC, Brasil.
Artigo recebido em: 05/03/2018
Artigo aprovado: 29/05/2019
DOI: 10.21877/2448-3877.201900682
INTRODUÇÃO
Urticária Crônica Espontânea (UCE) é uma doença cutânea caracterizada pelo desenvolvimento de lesões maculopapulares eritematosas, podendo estar associada ou não a angioedema durante um período superior a seis semanas. Algumas outras características, como urtica e angioedema (Quadro 1), são importantes para a diferenciação de outras patologias que cursam com as mesmas lesões elementares, como síndromes autoinflamatórias e angioedema hereditário.(1)
Estima-se que a prevalência da UCE gire em torno de 0,5%-1% na população geral, sendo, de longe, a forma mais comum de urticária não aguda (66%-93%).(2,3) Os principais desafios desse tipo de urticária são a falha em identificar-se um fator desencadeante e o comportamento não previsível da doença, acabando por promover frustração, tantos nos pacientes, quanto em seus médicos.(3) Importante destacar também o grande impacto na qualidade de vida do acometido devido ao caráter crônico da doença.(1,4)
Em uma consulta ao banco de dados da Editora Internacional Elsevier (Scopus), pelo termo “Chronic Spontaneous Urticaria” em títulos, resumos e palavras-chaves de artigos ou revisões, obteve-se resultado de 587 documentos, sendo, 293 (50%) publicados nos últimos três anos.(5) Com este dado, é possível observar-se a escassez literária sobre o tema e o interesse científico atual, o qual busca elucidar informações importantes no que diz respeito às urticárias, tais como sua etiologia, fisiopatologia e condutas terapêuticas mais eficazes.(1) Além disso, o desenvolvimento de duas ferramentas para a verificação da sintomatologia – UAS – e qualidade de vida – DLQi – dos acometidos pela UCE, têm contribuído de maneira significativa no avanço do tratamento e manejo desta patologia.(6)
Quanto à terapêutica, é consensual o uso de anti-histamínicos H1 de segunda geração como tratamento de primeira linha, podendo as doses ser aumentadas até quatro vezes para controle dos sintomas. Todavia, nem todos os pacientes atingem resolução satisfatória da UCE, mesmo após sucessivos ajustes nas doses medicamentosas, troca do agente anti-histamínico, uso de corticoesteroides sistêmicos, ansiolíticos, antileucotrienos e associação de múltiplos fármacos. Nesses casos, o tratamento com Omalizumabe, um anticorpo monoclonal anti-imunoglobulina E (IgE) revela-se como importante alternativa para o manejo da UCE.(6) Tal droga parece agir por dois mecanismos distintos, não totalmente compreendidos: ligando-se à IgE livre circulante; e causando downregulation dos receptores de alta afinidade à IgE (FccRI) dos basófilos.(2)
O objetivo do presente estudo foi avaliar o impacto na qualidade de vida e no grau de atividade da urticária do Omalizumabe em nossa população.

MATERIAL E MÉTODOS
Este trabalho trata-se de um estudo de coorte aberta, observacional, descritivo, exploratório, com abordagem quantitativa, realizado em uma clínica particular na cidade de Criciúma, Santa Catarina, Sul do Brasil. Após aprovação pelo comitê de ética em pesquisa institucional (2.272.096), foram analisados prontuários médicos dos pacientes com diagnóstico de UCE e baixa resposta ao tratamento polimedicamentoso (n = 07) no período de abril de 2017 a outubro de 2017.
As variáveis analisadas obtidas por meio do prontuário do paciente foram sexo, faixa etária, nível de IgE, sintomas e medicações prévias para UCE. O corticoesteroide utilizado foi a prednisona com dose em miligramas. A resposta ao Omalizumabe, o qual foi aplicado, em média, a cada quatro semanas em dose de 300 mg por via subcutânea, foi avaliada por meio de variáveis dependentes de escore de atividade da urticária (Urticaria Activity Score – UAS) e de qualidade de vida (Dermatology Life Quality Index – DLQI), verificados antes da primeira aplicação e após as aplicações posteriores de 2 a 7 meses de tratamento.
O UAS,(7) um questionário previamente validado, é composto por duas variáveis: número de lesões urticariformes (0-3 pontos) e a intensidade do prurido (0-3 pontos). O paciente deve ser instruído a avaliar cada variável uma vez por dia, no mesmo horário, por sete dias consecutivos. O resultado final pode variar de 0 a 21 pontos para cada variável e quantifica a atividade da UCE durante a semana.
O DLQi avalia como a alteração dermatológica impacta o dia-a-dia do paciente em seis domínios: sintomas e sentimentos, atividades diárias, lazer, trabalho e escola, relacionamento pessoal e tratamento, e aceita como respostas: realmente muito (3), bastante (2), um pouco (1), nada ou sem relevância (0). O escore varia de 0-30, sendo escores maiores apontando maior impacto na qualidade de vida. A soma é interpretada como em níveis de comprometimento na qualidade de vida: sem comprometimento na qualidade de vida (0-1), comprometimento leve (2-5), comprometimento moderado (6-10), comprometimento grave (11-20) e comprometimento muito grave (21-30).
Os dados coletados foram analisados com auxílio do programa Microsoft Excel utilizando-se a estatística descritiva. As variáveis quantitativas foram testadas nas comparações de antes e depois da intervenção com o Omalizumabe pelo teste t pareado. O nível de confiança adotado foi de 95% (p<0,05).
ÉTICA
O projeto foi aprovado pelo Comitê de Ética em Pesquisa institucional (protocolo 2.272.096) da Universidade do Extremo Sul Catarinense (UNESC).
RESULTADOS
As características gerais da amostra (n=7) consistiram em idades de 22 a 66 anos e 71,4% do sexo feminino (Tabela 1).
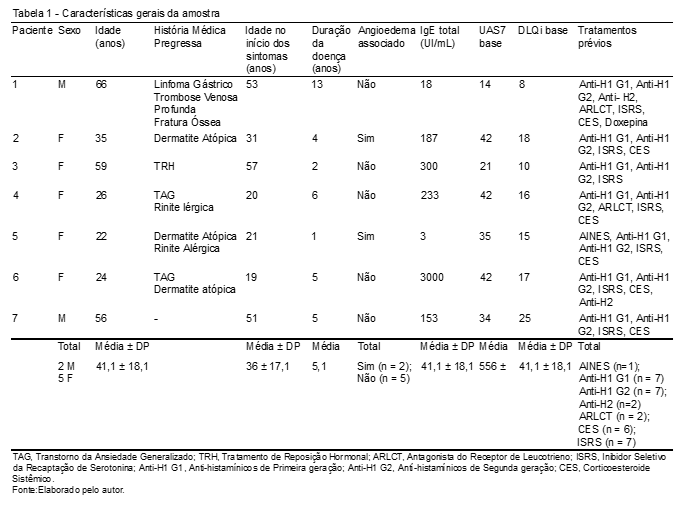
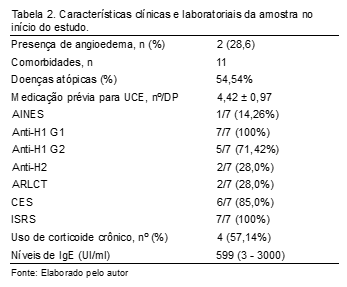
Entre as características clínicas e laboratoriais da amostra (Tabelas 1 e 2), observou-se a presença de angioedema em 28,6% dos pacientes e 71,4% deles apresentavam comorbidades, sendo 54,54% de origem atópica (rinite alérgica, dermatite atópica e asma). Antes do uso de Omalizumabe, os pacientes estavam sendo polimedicados, em média, com 4,42 medicamentos. As medicações mais prevalentes foram os anti-histamínicos H1 de primeira geração (Anti-H1 G1) (100%), antidepressivos inibidores seletivos da receptação de serotonina (ISRS) (100%), cortico-esteroide (CES) (85%) e anti-histamínico H1 de segunda geração (Anti-H1 G2) (71,42%). O uso de CES crônico foi realizado por 57,14% dos pacientes e um paciente apresentou múltiplas fraturas ósseas. O nível de IgE médio inicial foi de 599 UI/mL.
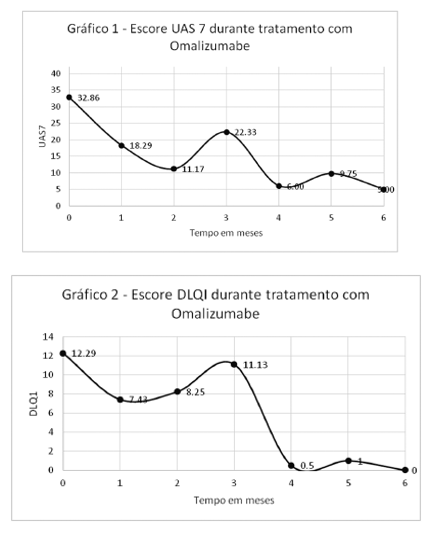
Após o tratamento com Omalizumabe, a resposta de cada paciente foi avaliada com o DLQI e UAS(7) antes e após o tratamento. Antes da primeira aplicação com Omalizumabe, o escore UAS(7) teve média de 32,86 (n=7); no primeiro mês após a aplicação foi de 18,29 (n=7), no segundo mês foi de 11,7 (n=6), no terceiro mês foi de 22,33 (n=3), no quarto mês foi de 6 (n=4), no quinto mês, de 8,33 (n=2) e no sexto mês, de 4 (n=1) (Gráfico 1). O score DLQI, por sua vez, foi de 12,29 (n=7) antes da aplicação, no primeiro mês após a aplicação foi de 7,43 (n=7), no segundo mês foi de 8,25 (n=4), no terceiro mês, de 11,13 (n=3), no quarto mês, de 0,5 (n=2), no quinto mês, de 1 (n=3) e no sexto mês, de 0 (n=1) (Gráfico 2).
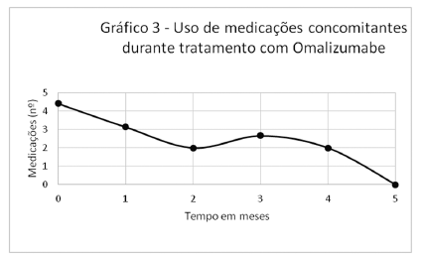
As medicações usadas durante o tratamento com Omalizumabe estão evidenciadas no Gráfico 3. Todos os pacientes usavam medicações, antes do tratamento, na média de 4,42; no primeiro mês após a aplicação do imunobiológico, a média de medicações foi de 3,14 (n=7), após a segunda aplicação foi de 2 (n=5), após a terceira aplicação, de 2,66 (n=3), após a quarta aplicação, de 2 (n=2) e, ao quinto mês, os pacientes não fizeram mais uso de medicações concomitantes (n=2) (Gráfico 3).
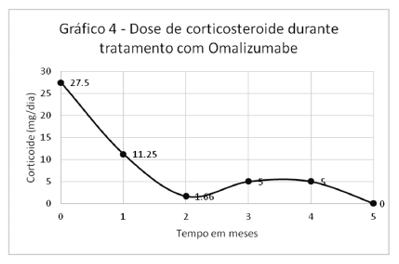
Analisaram-se as doses de CES utilizadas cronicamente pelos pacientes (n=4) antes do uso de Omalizumabe, as quais eram, em média, de 27,5 mg. No primeiro mês após a aplicação, houve redução para 11,25 mg (n=4), no segundo mês a dose foi de 1,66 mg (n=3) e no terceiro mês a dose foi de 5 mg (n=1) e, partir do quinto mês, o uso de CES foi suspenso (Gráfico 4). Efeitos colaterais (n=2) apresentados pelos pacientes ao uso de CES a longo prazo foram fraturas ósseas e infecção fúngica disseminada.
Os efeitos colaterais de eritema papular no local da aplicação e tosse em resposta ao Omalizumabe foram apresentados por 28% dos pacientes.
DISCUSSÃO
A UCE foi mais prevalente no sexo feminino com idade predominante entre 21 e 40 anos, resultado semelhante a estudo realizado na Espanha,(8) o qual aponta a prevalência da doença duas vezes maior em mulheres do que em homens. Também se assemelhou na faixa etária a estudos (9,10) que descrevem a maior prevalência entre a segunda e quinta décadas de vida.
O angioedema, que se associa a um curso mais prolongado e piora da doença(11,12) esteve presente em 28,6% dos pacientes, pouco abaixo dos 35% dos casos de UCE com concomitância de angioedema.(13) As doenças atópicas, por sua vez, também estiveram associadas à UCE,(14) assim como o evidenciado no presente estudo.
Os pacientes com UCE refratária ao tratamento convencional possuem indicação de tratamento com Omalizu-mabe pela falência dos tratamentos prévios ou pela presença de efeitos colaterais a eles.(15)
Sobre a efetividade do medicamento, 42% obtiveram controle dos sintomas da doença, evidenciado por um escore do UAS7£ 6, além de 66% da melhora de qualidade de vida, demonstrado pela diminuição do DLQI. Os valores foram um pouco menores do evidenciado em estudo fase 2 de posologia do Omalizumabe (71% e 78%, respectivamente).(16) Tal divergência pode dar-se pela diferença do período de seguimento das amostras.
O número de medicações anteriores usadas pelos pacientes do presente estudo foi de 4,42±0,97, muito semelhantes aos valores basais de um estudo randomizado placebo controlado com 323 pacientes (média de 4,32 ± 2,67).(16) Após o uso de Omalizumabe, ao quinto mês foi suspenso o uso de medições concomitantes.
O uso de corticoide sistêmico é indicado de sete a dez dias,(17,18) porém pacientes com UCE refratária o fazem cronicamente(19) – 57,1% dos pacientes do presente estudo –, o que é preocupante, dado os efeitos colaterais em potencial associado ao uso crônico, como diabetes melitus, hipertensão, osteoporose e sangramentos gastrointestinal.(20) A maior complicação do uso crônico de CES, a fratura óssea resultante de perda óssea,(21) foi apresentada por um paciente do estudo. Outro paciente apresentou pitiríase versicolor disseminada predisposta pelo CES, uma vez que este facilita infecções fúngicas pelo efeito inibidor do sistema imunológico e da resposta inflamatória.(22)
Em comparação ao estudo de Sussman,(23) todos os pacientes utilizaram anti-histamínicos, assim como no estudo comparativo 85% usaram corticoide sistêmico versus 97%, 28% usavam antileucotrienos versus 16%, anterior ao tratamento com Omalizumabe. O uso de Omalizumabe reduziu a necessidade de corticosteroides em 85%, resultado superior a estudos com outras drogas poupadoras de corticoides, como o metotrexato e ciclosporina.(24,25) O efeito colateral de anafilaxia ao Omalizumabe não foi apresentado no presente estudo, característica que favorece a consagração recente do imunobiológico como opção de tratamento segura para UCE refratária.(26)
Os principais fatores limitantes do uso do imunobiológico encontradas no estudo foram o alto custo da medicação e a disponibilidade baixa no mercado.
CONCLUSÃO
O Omalizumabe mostrou-se uma opção terapêutica segura e eficaz, apresentando efeitos benéficos para os pacientes, como melhora da qualidade de vida, melhora dos sintomas de UCE e diminuição importante da necessidade de uso de medicações concomitantes.
Novos estudos se fazem necessários para a elucidação do mecanismo de ação do Omalizumabe e dos fatores que identifiquem bons respondedores ao imunobiológico para, assim, reduzir o período de latência para o início de um tratamento efetivo nesses pacientes e evitar os efeitos colaterais de uma das principais medicações adjuvantes da UCE refratária usado pelos pacientes, o corticoesteroide sistêmico.
Abstract
Introduction: Chronic Spontaneous Urticaria (CEU) is a disease that affects a significant portion of the population, generating negative impacts on quality of life and psychosocial performance. Lack of response to first-line treatment imposes an imminent need for novel therapeutic strategies. The treatment of these patients with Omalizumab has shown a promising effect. Objective: To evaluate the clinical response of patients diagnosed with Chronic Urticaria Spontaneous to the use of Omalizumab in patients followed at a private clinic in the South of Brazil. Methods: Observational, open cohort study, descriptive, exploratory. The validated questionnaires Dermatology Life Quality Index (DLQI) and Urticaria Activity Score (UAS) for seven patients were evaluated. Results: The CEU was verified in the ages between 22 and 66 years and more prevalent in the female (71.4%). All patients were being treated with at least three CEU medications without improvement. After the use of Omalizumab, a statistically significant decrease at a dosage of corticosteroids (27.5mg±15.0 to 0±0) and DLQI questionnaires scores (12.29±9.46 to 4.85±7.96) and UAS (32.86±10.37 to 12.57±13.32) over the six-month follow-up. Conclusion: Omalizumab proved to be a safe and effective therapeutic option, with benefits such as improved quality of life, improvement of symptoms and decreased use of concomitant medications.
Keywords
Urticaria; monoclonals antibodies; histamine antagonists; adrenal cortex hormones; quality of life; corticosteroids
REFERÊNCIAS
- Zuberbier T, Aberer W, Asero R, Bindslev-Jensen C, Brzoza Z, Canonica GW, et al. The EAACI/GA2LEN/EDF/WAO Guideline for the definition, classification, diagnosis, and management of urticaria: The 2013 revision and update. Allergy Eur J Allergy Clin Immunol [Internet]. 2014 Jul [cited 2017 Oct 21];69(7):868-87. Available from: http://doi.wiley.com/10.1111/all.12313
- Kaplan AP, Giménez-Arnau AM, Saini SS. Mechanisms of action that contribute to efficacy of omalizumab in chronic spontaneous urticaria. Allergy Eur J Allergy Clin Immunol. 2017;72(4):519-33.
- Maurer M, Weller K, Bindslev-Jensen C, Giménez-Arnau A, Bousquet PJ, Bousquet J, et al. Unmet clinical needs in chronic spontaneous urticaria. A GA2LEN task force report. Allergy Eur J Allergy Clin Immunol. 2011;66(3):317-30.
- Criado PR, Martins EJC, Criado FRJ, Maruta CW, Rivitti EA. Urticaria. An Bras Dermatol [Internet]. 2005;1(6):613-32. Available from: http: //www.scielo.br/pdf/abd/v80n6/en_v80n06a08.pdf
- Scopus [Internet]. Amsterdã: Elsevier; 2017. Available from: https://www.scopus.com/results/results.uri?numberOfFields =0&src=s& clickedLink=&edit=t&editSaveSearch=&origin=searchbasic&authorTab=&affiliationTab=&advancedTab=&scint=1&menu=search&tablin=&searchterm1 =chronic+ spontaneous+ urticaria & field1=TITLE_ABS_KEY&dat
- Costa C et al. Abordagem Diagnóstica e Terapêutica da Urticária Crónica Espontânea. Recomendações em Portugal. Acta Med Port [Internet]. 2016;29(11):763-81. Available from: http://www. actamedicaportuguesa.com/revista/index.php/amp/article/viewFile/8294/4830
- Mynek A, Zalewska-Janowska A, Martus P, Staubach P, Zuberbier T, Maurer M. How to assess disease activity in patients with chronic urticaria? Allergy. 2008 Jun;63(6):777-80. Available from: https://www.ncbi.nlm.nih.gov/pubmed/18445192
- Gaig P, Olona M, Muñoz Lejarazu D, Caballero MT, Domínguez FJ, Echechipia S, et al. Epidemiology of urticaria in Spain. J Investig Allergol Clin Immunol [Internet]. 2004 [cited 2017 Oct 21];14(3):214-20. Available from: http://www.jiaci.org/issues/vol14issue03/214-220.pdf
- Ferrer M. Epidemiology, healthcare, resources, use and clinical features of different types of urticaria. Alergologica 2005. J Investig Allergol Clin Immunol. 2009;19 Suppl 2:21-6.
- Zhong H, Song Z, Chen W, Li H, He L, Gao T, et al. Chronic urticaria in Chinese population: A hospital-based multicenter epidemiological study. Allergy. 2014 Mar;69(3):359-64,
- Cooper KD. Urticaria and angioedema: Diagnosis and evaluation. J Am Acad Dermatol. 1991 Jul;25(1 Pt 2):166-74. Available from: http://dx.doi.org/10.1016/0190-9622(91)70184-4
- Champion RH, Roberts SOB, Carpenter RG, Roger JH. Urticaria and Angioedema: a Review of 554 Patients. Br J Dermatol. 1969;81(8): 588-97.
- Najib U, Bajwa ZH, Ostro MG, Sheikh J. A retrospective review of clinical presentation, thyroid autoimmunity, laboratory characteristics, and therapies used in patients with chronic idiopathic urticaria. Ann Allergy Asthma Immunol. 2009 Dec;103(6):496-501. Available from: http://dx.doi.org/10.1016/S1081-1206(10)60266-9.
- Duarte P. Urticária Crónica: Experiência da Consulta nos CHUC. 2014 [cited 2017 Oct 21]; Available from: https:// estudogeral.sib. uc.pt/bitstream/10316/37446/1/Urticaria cronica experiencia da consulta nos CHUC.pdf
- Metz M, Maurer M. Omalizumab in chronic urticaria. Curr Opin Allergy Clin Immunol. 2012;12(4):406-11.
- Maurer M, Rosén K, Hsieh H-J, Saini S, Grattan C, Gimenéz-Arnau A, et al. Omalizumab for the Treatment of Chronic Idiopathic or Spontaneous Urticaria. N Engl J Med [Internet]. 2013 [cited 2017 Oct 21];368(10):924-35. Available from: http://www.nejm.org/doi/pdf/ 10.1056/NEJMoa1215372
- Maurer M, Magerl M, Metz M, Zuberbier T. Diagnostik und therapie der chronischen urtikaria – Was wird von revision und aktualisierung der internationalen leitlinie erwartet? Ein report der öffentlichen konsensuskonferenz “URTICARIA 2012.” Allergo J. 2013;22(5): 324-9.
- Mehta A, Godse K, Patil S, Nadkarni N, Gautam M. Treatment of Refractory Chronic Urticaria. Indian J Dermatol. 2015 [cited 2017 Oct 21];60(3):230-7. Available from: http://www.ncbi.nlm.nih.gov/pubmed/26120147
- Agondi RC, Crispim L, Almonfrey FB, Kalil J, Motta, Motta AA. Urticária crônica espontânea refratária aos anti-histamínicos: opção por ciclosporina. Arq Asma Alerg Imunol. 2017;1(2):212-6. Acessível em: https://docplayer.com.br/52521950-Urticaria-cronica-espontanea-refrataria-aos-anti-histaminicos-opcao-por-ciclosporina.html
- Criado PR, Criado RF, Maruta CW, Reis VM. Chronic urticaria in adults: State-of-the-art in the new millennium. An. Bras. Dermatol. [Internet]. 2015 Feb [cited 2017 Oct 21; 90(1):74-89. ]. Available from: http://dx.doi.org/10.1590/abd1806-4841.20153509
- Eastell R, Reid DM, Compston J, Cooper C, Fogelman I, Francis RM, et al. A UK Consensus Group on a management of glucocorticoid-induced osteoporosis: an update. J Intern Med. 1998 Oct;244(4):271-92. Available from: https://www. ncbi.nlm.nih.gov/pubmed/9797491
- Cardozo Pereira AL, Bolzani FCB, Stefani M, Charlín R. Uso sistêmico de corticosteroides: revisão da literatura. Med Cutan Iber Lat Am. 2007;35(1):35-50. Available from: www.saudedireta.com.br/docsupload/134442634406-091.pdf
- Sussman G, Hébert J, Barron C, Bian J, Caron-Guay RM, Laflamme S, et al. Real-life experiences with omalizumab for the treatment of chronic urticaria. Ann Allergy Asthma Immunol. 2014 Feb;112(2):170-4. Available from: http://www.annallergy.org/article/S1081-1206(13)00926-5/pdf
- Perez A, Woods A, Grattan CE. Methotrexate: A useful steroid-sparing agent in recalcitrant chronic urticaria. Br J Dermatol. 2010 Jan;162(1):191-4
- Toubi E, Blant A, Kessel A, Golan TD. Low-dose cyclosporin A in the treatment of severe chronic idiopathic urticaria. Allergy. 1997;52(3):312-6.
- Kaplan AP. Chronic Spontaneous Urticaria: Pathogenesis and Treatment Considerations. Allergy Asthma Immunol Res. 2017 Nov;9(6):477-482. Available from: https://synapse.koreamed.org/DOIx.php?id=10.4168/aair.2017.9.6.477&vmode=PUBREADER
Correspondência
Mariana Mangilli de Menezes
Universidade do Extremo Sul Catarinense – UNESC
Unidade Acadêmica em Ciências da Saúde – UNASAU
Curso de Medicina,
Criciúma – SC, Brasil
(48) 3437-4588
