Avaliação da qualidade e da estabilidade de amostras de soro humano para análise e armazenamento em biorrepositório
Evaluation of the quality and the stability of human samples for analysis and storage in biorepository
Leonardo André Lange1
Caroline Galgowski1
Anna Cecília Roncalio1
Fabiana Sehnem1
Grabriela Borgmann1
Caio Mauricio Mendes de Cordova2
- Universidade Regional de Blumenau – Blumenau-SC, Brasil.
- Doutor pela Universidade de São Paulo – USP – São Paulo-SP, Brasil. Professor.
Instituição: Universidade Regional de Blumenau – Blumenau-SC, Brasil.
Suporte Financeiro: Edital FAPESC/PPSUS 2012; FURB; PIBIC/CNPq.
Artigo recebido em 02/11/2017
Artigo aprovado em 08/01/2018
DOI: 10.21877/2448-3877.201800637
Resumo
Objetivo: O Estudo das Condições de Vida e Saúde de Pomerode, SC (SHIP-Brasil), conduzido pela Universidade Regional de Blumenau, visa estratificar os fatores de risco e genéticos eventualmente existentes na gênese das mais variadas doenças. Para tal são necessários exames laboratoriais, antropométricos, genéticos e de imagem para a definição das mesmas e o acompanhamento de sua evolução. Este trabalho teve como objetivo avaliar a qualidade das amostras armazenadas no biorrepositório do estudo, que podem ser utilizadas para pesquisas de biomarcadores no futuro. Métodos: Foram avaliadas amostras de soro em jejum de 56 voluntários. Os analitos estudados foram glicose, colesterol total, creatinina e transaminase glutâmico-pirúvica (ALT), após 1, 2 e 3 anos de armazenamento a -80ºC. Os resultados foram analisados com o Teste t de Student e de acordo com o Erro Permitido Máximo para cada analito. Resultados: Não encontramos evidências de que as amostras do Estudo SHIP-Brasil possam perder a sua qualidade após serem armazenadas por longos períodos. Conclusão: Os Procedimentos Operacionais Padrão (POPs) estabelecidos estão adequados para o processamento e preservação das amostras.
Palavras-chave
Estudos de coortes; Marcadores biológicos; Bancos de espécimes biológicos; Estabilidade proteica; Preservação de amostras; Manejo de espécimes
INTRODUÇÃO
O presente trabalho faz parte de um estudo de coorte na população de Pomerode, SC (SHIP-Brasil; Study of Health in Pomerode), conduzido pela Universidade Regional de Blumenau, a fim de estratificar os fatores de risco e genéticos eventualmente existentes na gênese das mais variadas doenças. Para tal são necessários exames laboratoriais, antropométricos, genéticos e de imagem para a constatação dos mesmos e o acompanhamento de sua evolução. O estudo em Pomerode é um estudo multicêntrico tendo como âncora o projeto SHIP SC (Study of Health in Pomerania) conduzido na região da Pomerânia Alemã.(1) Este estudo já se encontra em andamento há mais de 15 anos, na Universidade de Greifswald, e a colaboração dos pesquisadores de lá conosco permitirá também a utilização dos dados obtidos na Alemanha para efeitos de comparação. Pomerode é uma cidade fundada por imigrantes pomeranos que mantêm vivas a tradição e a cultura germânicas. Do ponto de vista da saúde, apresenta algumas particularidades, como elevadas taxas de suicídios e de câncer de pele e elevada mortalidade por doenças cardiovascular entre outras, combinadas com indicadores sociais considerados de primeiro mundo.
Os objetivos do trabalho foram avaliar a estabilidade das amostras de soro e assim a garantia da qualidade do processamento destas amostras para exames e armazenamento no biorrepositório do estudo, possibilitando o estabelecimento futuro de parâmetros hematológicos e bioquímicos básicos para a definição das condições de saúde e doença. Foram criados e implantados os Procedimentos Operacionais Padrão (POPs) para a realização dos exames bioquímicos e hematológicos necessários ao estudo SHIP-Brasil, no que tange aos aspectos pré-analíticos e pós-analíticos, notadamente os POPs para a operacionalização da coleta, transporte e processamento das amostras biológicas do estudo, os POPs para a operacionalização do Biorrepositório de Amostras Biológicas do estudo SHIP-Brasil, bem como o sistema de registro e controle das amostras e alíquotas armazenadas no Biorrepositório.
Foi assim conduzido um estudo da estabilidade das amostras de soro armazenadas no Biorrepositório do SHIP-Brasil. Para este fim, biomarcadores de diferentes naturezas químicas foram avaliados em amostras de soro armazenadas para verificar se estas mantêm a sua estabilidade durante um longo período de armazenamento após o processamento a que foram submetidas. Os biomarcadores avaliados foram glicose como representante dos carboidratos, colesterol total como representante dos lipídios, creatinina representando um catabólito nitrogenado não proteico e alanina aminotransferase (ALT) como enzima.
MATERIAL E MÉTODOS
– Amostragem: A população do SHIP-Brasil constituiu-se de amostragem aleatória simples por sete estratos de faixa etária e sexo a partir de 20 anos, com intervalos de 10 anos; considerando a população por sexo de cada faixa etária, prevalência de 50%, precisão de 5% (IC de 95%), 20% para perdas e 20% para análise de confundimento, calculada em 3.091 pessoas da população de 27.759 habitantes de Pomerode, SC (IBGE 2010). Para minimizar problemas com perdas e baixa adesão, a amostragem da população a ser convidada a participar do estudo foi aumentada para 4.000 indivíduos. Foram incluídos no estudo os indivíduos que residem no município há pelo menos seis meses, com 20 anos de idade ou mais. São excluídos do estudo os indivíduos que possuem qualquer limitação de ordem física ou mental que o impeçam de responder aos questionários, realizar exames, ou que se recusaram a assinar o TCLE. É aplicado um amplo questionário geral com variáveis socioeconômicas, demográficas, de estilo de vida, médico-assistenciais e mentais. São realizados ainda exames de ultrassonografia de fígado e carótidas, abdômen total e de calcâneo (para estimativa de risco de fratura óssea). A participação dos indivíduos no estudo SHIP-Brasil, bem como o uso das amostras biológicas e seus resultados, foi aprovada pelo Comitê de Ética em Pesquisa da Universidade Regional de Blumenau sob o nº 33/2012. O estudo é financiado pelo Edital FAPESC/PPSUS 2012.
– Amostras biológicas: Dos participantes que assim o autorizam, são coletadas amostras de sangue total, soro, plasma, urina, saliva, swab nasal, de orofaringe, de língua, de bolsas gengivais (quando detectadas), raspado endocervical e fezes.(1) As amostras são processadas e armazenadas em ultrafreezer a -80ºC.(2) Dos voluntários do projeto SHIP-Brasil, foram selecionados vinte do ano de 2014, formando o Grupo 1, vinte do ano de 2015, formando o Grupo 2, e vinte do ano de 2016, formando o Grupo 3. O critério de exclusão para os Grupos 1 e 2 foi o de não haver resultados laboratoriais no banco de dados do estudo, e no Grupo 3 também o de não terem sido realizados os exames no mesmo laboratório encarregado de realizar os testes a partir de 2016. O número total de amostras obtido foi 56. Cada amostra foi testada em uma nova alíquota, a partir do primeiro semestre de 2016 (2016/1), a cada seis meses (2016/2 e 2017/1), de forma a verificar uma eventual tendência significativa de alterações dos resultados. Para a análise estatística, foram excluídos os dados das dosagens discrepantes (outliers) cuja diferença de resultado entre o valor de referência (primeira dosagem realizada no laboratório de rotina) tenha ultrapassado 1,96 vezes o desvio padrão médio dos primeiros resultados, pela maior probabilidade de se tratarem de erros aleatórios dentro de um intervalo de confiança de 95%.
– Processamento das amostras: As amostras biológicas utilizadas foram de soro coletado em jejum. Essas amostras foram separadas em até 12 alíquotas de 500 uL em criotubos e armazenadas em freezer a -80ºC. A cada seis meses, uma destas alíquotas foi retirada do freezer -80ºC para a realização das determinações laboratoriais.
– Avaliação laboratorial das desordens metabólicas e danos em órgãos: Os distúrbios metabólicos e danos em órgãos nos voluntários do Estudo SHIP-Brasil foram avaliados inicialmente através dos resultados laboratoriais de hemoglobina glicada (HbA1c), glicemia em jejum, glicemia pós-sobrecarga, ALT, gama-GT, colesterol total, triglicerídeos, HDL-c, e creatinina sérica. Os testes foram realizados por laboratório clínico de rotina e calibrados com padrão rastreável a material de referência internacional, de acordo com as instruções dos fabricantes. Os procedimentos para o controle de qualidade dos processos foram realizados de acordo com as normas do Programa Nacional de Controle de Qualidade (PNCQ), e das normas ISO 15.189 e NBR 14.500.
– Estudo de estabilidade: Os exames de glicose e colesterol total foram realizados segundo metodologia Labtest (Lagoa Santa, MG, Brasil); já os exames de creatinina e ALT foram realizados segundo a metodologia da Kovalent (São Gonçalo, RJ). Nos Grupos 1 e 2 foram feitas as determinações da concentração de glicose, colesterol total e creatinina; no Grupo 3 também foi avaliada a atividade de ALT, estabelecendo-se curvas de tendência para estimativa da estabilidade dos analitos em relação aos limites de variabilidade aceitos, para que os resultados não ultrapassem o erro total permitido para as diferentes análises laboratoriais.(3)
– Análise estatística: Os dados obtidos foram tratados por estatística paramétrica, como o Teste t de Student, média, desvio padrão e diferença média, com o auxílio do programa MS Excel, considerando o intervalo de confiança, de acordo com as recomendações do grupo STARD.(4)
RESULTADO E DISCUSSÃO
As Tabelas 1 a 4 a seguir apresentam os resultados das dosagens de glicose, colesterol total, creatinina e ALT determinadas em novas alíquotas a cada seis meses (2016/2 e 2017/1), em comparação com os resultados laboratoriais originais determinados em 2016/1. Os dados são apresentados como média e desvio padrão, valor de P calculado pelo Teste t de Student entre cada análise, bem como a diferença média entre os resultados obtidos a cada semestre para efeitos de comparação com o Erro Permitido Máximo para cada analito, ou seja, 7% para Glicose, 9% para Colesterol e Creatinina, e 27,5% para ALT.(3)
Observando os dados é possível perceber que as análises realizadas em nosso laboratório de pesquisa (2016/2 e 2017/1) apresentaram, de maneira geral, diferenças em relação aos valores originais determinados pelo laboratório clínico de rotina.
Essas diferenças aparentam ser uma combinação de erro aleatório e erro sistemático. O erro aleatório fica evidente pelo maior desvio padrão em muitos de nossos resultados (Figura 1), e o erro sistemático pela discrepância de valores que não se explica por uma linha de tendência condizente com uma eventual degradação das amostras.
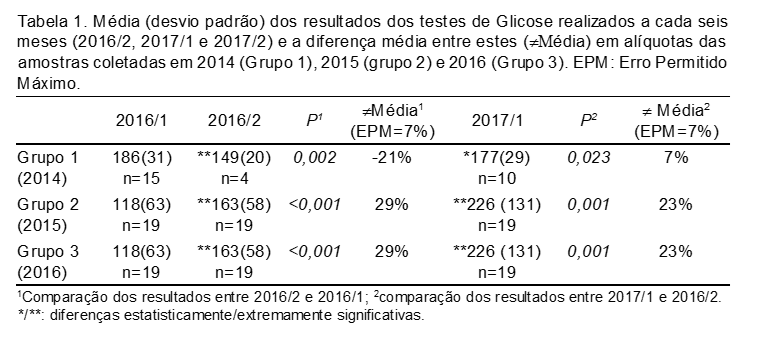
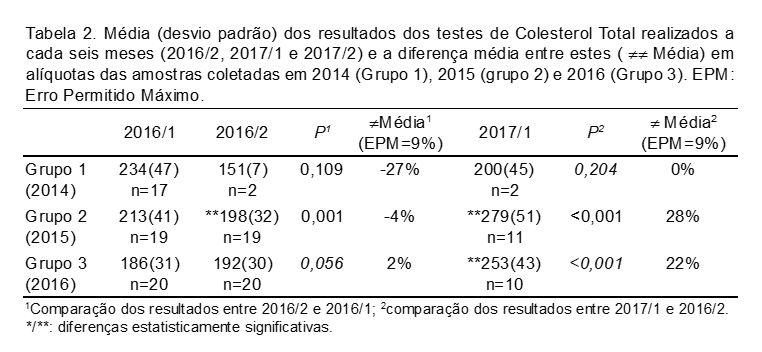
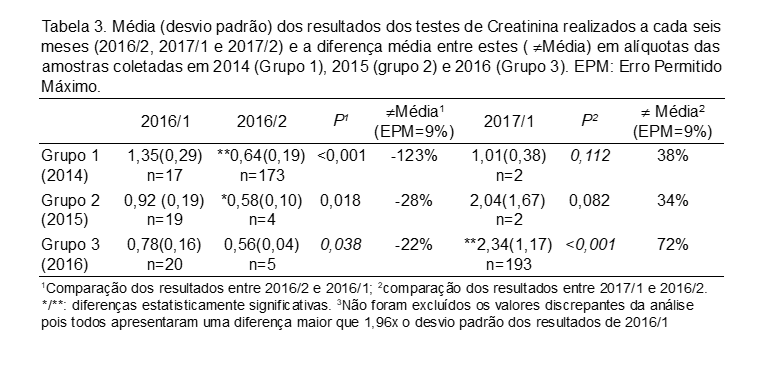
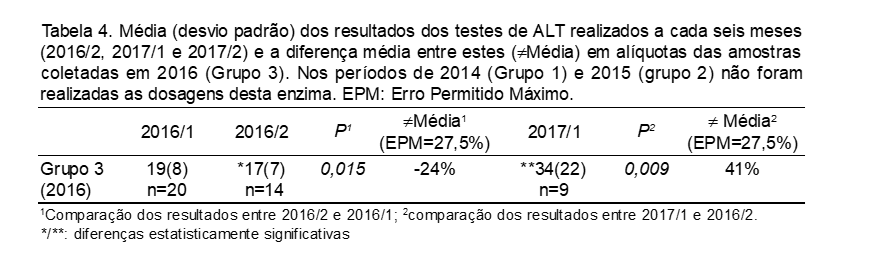
Por exemplo, os valores de glicose tiveram uma diminuição significativa de 2016/1 para 2016/2 no Grupo 1, o que poderia indicar uma degradação do analito na amostra, mas a diferença foi inversa nos Grupos 2 e 3, o que só poderia ser explicado por uma concentração dos analitos por evaporação da amostra, por mal fechamento dos criotubos. Entretanto, essa concentração teria que ocorrer também com os tubos armazenados desde 2014 (Grupo 1), e não somente nos tubos de amostras mais recentes (2015 e 2016). Esse padrão, que poderia explicar uma concentração da amostra, não se observa para os resultados de colesterol entre 2016/1 e 2016/2 nos Grupos 2 e 3, observando-se o mesmo bias (erro sistemático) negativo no Grupo 1 neste período. Inclusive, entre 2016/1 e 2016/2, nos Grupos 2 e 3 as diferenças médias para o colesterol estão dentro no Erro Permitido Máximo (EPM), mas não em 2017/1 em relação a 2016/2, exceto no Grupo 1. Assim, é evidente uma combinação de erros sistemáticos e aleatórios em nossas análises, como causa da variabilidade observada. O mesmo se observa com os resultados de creatinina, com uma diferença bem maior em relação ao EPM. Para ALT, foi possível fazer a avaliação apenas no Grupo 3, pois os demais não tiveram este analito determinado em suas amostras por questões operacionais. No primeiro período (2016/1 e 2016/2, o EPM ficou dentro do limite estabelecido, apesar de o Teste t indicar que a diferença foi significativa para os novos valores menores). No segundo período (2016/2 versus 2017/1) observamos resultados maiores, o que seria indicativo de concentração da amostra, o que não é corroborado pelos resultados do primeiro período.
Para essas variações foram encontradas as seguintes possibilidades. O espectrofotômetro que foi utilizado para as análises desta pesquisa é um aparelho utilizado em aulas práticas de graduação, já um tanto antigo e que não sofre manutenção periódica e nem é submetido a um processo de controle de qualidade interno e externo. Da mesma forma, as micropipetas utilizadas têm mais de 10 anos de uso e não calibradas. Além disso, nesta pesquisa foram utilizados reagentes e padrões de marcas diferentes daqueles utilizados nos testes de rotina, o que acarreta uma variabilidade adicional.
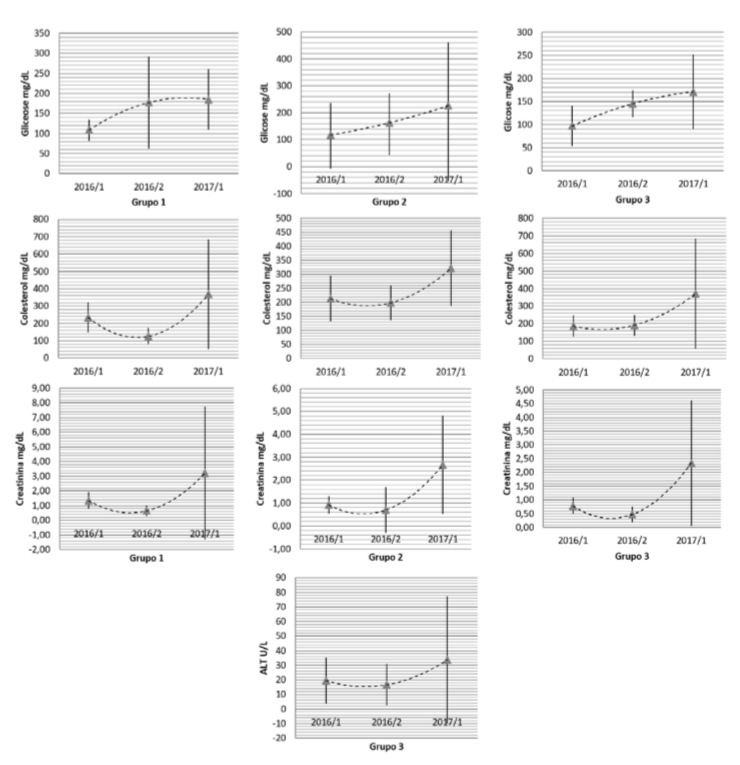
Figura 1. Distribuição com média e 1,96 vezes o desvio padrão dos resultados obtidos pelo laboratório clínico de referência (2016/1) e os dados de nosso laboratório de pesquisa (2016/2 e 2017/1), para os valores de Glicose, Colesterol, Creatinina e ALT nas amostras avaliadas, com linha de tendência polinomial. Todos os dados estão representados, sem exclusão dos valores discrepantes (outliers).
Assim, estes dados não demonstram evidências de degradação das amostras acondicionadas no biorrepositório do Estudo SIP-Brasil, com uma linha de tendência consistente de aumento ou diminuição dos resultados ao longo do tempo.
Protocolos padronizados são necessários para obter perfis imparciais em várias dosagens em longos períodos de tempo e permitir análises estatísticas confiáveis. Fatores já determinados que podem causar variabilidade são o tempo de coagulação da amostra de sangue e temperatura a que as amostras são submetidas.(5) O processamento pré-analítico é essencial para a manutenção da qualidade das amostras para a determinação de biomarcadores séricos, e mesmo assim ainda não foi totalmente caracterizado. Por exemplo, o armazenamento a temperatura ambiente, ao invés de refrigeração, antes da centrifugação, pode afetar significativamente os níveis de muitos metabólitos.(6) Foi demonstrado que a coagulação do sangue a temperatura ambiente resulta em concentrações maiores de metabólitos do que sob refrigeração.(7) Além disso, o tipo de tubo utilizado afeta os resultados. A utilização de tubos com gel de polímero afeta a concentração de metabólitos dos aminoácidos como alanina, prolina e treonina, de glicerolípidos e metabolitos primários como ácido aconítico e ácido lático, em comparação ao uso de tubos convencionais.(8) Assim, vemos que padronização é essencial. É muito importante também que o processo garanta que as amostras venham a ser armazenadas a -80ºC e o mais rapidamente possível, uma vez que muitos analitos podem não ser estáveis a temperaturas mais baixas.(9) O congelamento imediato das amostras após a centrifugação é um aspecto chave, pois alguns analitos podem apresentar alteração se a demora chegar a 24 horas.(10) Não só amostras com marcadores sensíveis, como de estresse oxidativo, mas também proteicos como Proteína C Reativa, homocisteína e ALT devem ser armazenadas a -80ºC.(11) Entretanto, é necessário prever que o armazenamento a longo prazo a -80º pode preservar metabólitos e mesmo DNA por muitos anos, mas o RNA se torna instável em 5 anos de armazenamento. E de maneira geral, permanece não resolvido se o armazenamento a partir de -150°C proporciona vantagens significativas em relação a -80°C.(12) Outros analitos, como marcadores urinários, podem não ser estáveis em períodos maiores que 5 anos.(13) Entretanto, para a maioria dos analitos séricos, incluindo hormônios, se espera estabilidade por ao menos 3 décadas de armazenamento, exceto alguns, que podem apresentar alteração significativa já a partir de 15 anos, como lipídeos (exceto colesterol total), apolipoproteínas, e prolactina.(14)
Apesar destas informações, continua a haver uma falta de padronização no gerenciamento de qualidade entre os biobancos e consenso sobre quais indicadores de qualidade fornecem ferramentas de desempenho ideal e informações para amostras biológicas. Ainda, é improvável que um único marcador forneça a informação ideal sobre as amostras, mas sim um painel de marcadores que avalie a integridade molecular do seu tempo de vida parece ser necessário. (15) Como se vê, a obtenção de amostras de alta qualidade requer a implementação de procedimentos operacionais padrão para controlar as variáveis pré-analíticas nos biobancos. Atualmente, a maioria dos biobancos não controla estas variáveis ao coletar, processar e armazenar suas amostras.(16)
De qualquer maneira, é salutar a repetição do presente estudo nesta linha, com um maior financiamento, e fazendo todas as dosagens em um laboratório clínico de referência, com um sistema de controle de qualidade analítico bem instituído, e preferencialmente o mesmo laboratório onde as determinações originais foram realizadas, para confirmar a estabilidade das amostras submetidas ao processo de aliquotamento e armazenamento do Estudo SHIP-Brasil.
Gostaríamos de ressaltar que o escopo, a natureza e a oportunidade deste estudo são inéditos no Brasil. Não se identificou na literatura revisada estudo epidemiológico nacional que além de medir a incidência ou prevalência de uma grande gama de doenças e condições, também estudasse sua possível causalidade genética, cultural e ambiental. A opção pelo município de Pomerode para este estudo justifica-se pela oportunidade de se realizar um estudo multicêntrico com o SHIP-Study of Health in Pomerania realizado na região da Pomerânia na Alemanha, que será capaz de fornecer dados para dimensionar a associação do fator genético, semelhante nessa população, com fatores de ordem ambiental, distintos nos dois grupos. A Universidade Regional de Blumenau possui convênio com a Ernst-Moritz-Arndt Universität Greifswald para diversas áreas de atuação e neste estudo multicêntrico.
Este projeto representa uma grande oportunidade ao permitir comparações entre populações que apresentam grandes semelhanças relacionadas ao fator genético e cultural e grandes diferenças em relação ao fator ambiental. Os dados obtidos nesse estudo, de base populacional para Pomerode-SC, poderão servir de base para o planejamento da atenção em saúde do município. Pomerode conta com cobertura total do município com equipes de Estratégia Saúde da Família cadastradas em sistema informatizado único.
Além disso, os dados obtidos poderão servir para o controle de qualidade dos sistemas municipais, além de permitir a construção de indicadores de saúde mais precisos, e subsidiar o monitoramento e o planejamento da atenção em saúde do município, extrapolados para o Estado e o País, com base nos indicadores sociodemográficos existentes. Entretanto, para isso, é necessário que os resultados laboratoriais gerados sejam confiáveis, e que as amostras biológicas coletadas tenham sua estabilidade garantida para a realização de exames laboratoriais adicionais, à medida que novas verbas forem captadas, ou novas tecnologias e novos biomarcadores forem sendo descobertos.
Agradecimentos
O estudo SHIP-Brasil foi financiado pelo Edital FAPESC/PPSUS 2012. Agradecemos à Universidade Regional de Blumenau pelo suporte à implantação do estudo, e em especial a todos os alunos e colaboradores envolvidos.
Abstract
Objective: The Study of Health in Pomerode, SC (SHIP-Brazil), conducted by the University of Blumenau, aism to stratify the genetic and risk factors eventually existing in the genesis of the most varied diseases. Laboratory, anthropometric, genetic and imaging examinations are necessary to verify them and to monitor their evolution. This work aimed to evaluate the quality of the samples stored in biorepositories, such as samples of the SHIP Brazil project, which can be used for future research. Methods: Fasting serum samples from 56 volunteers were evaluated. Glucose, total cholesterol, creatinine and glutamic-pyruvic transaminase (ALT) were measured after 1, 2 and 3 years of storage. The results were analyzed using Student’s t-Test and Maximum Permitted Error for each analyte. Results: It was found no evidence that the SHIP-Brazil Study samples may lose their quality after being stored for long periods. Conclusion: The Standard Operating Procedures (SOPs) established are suitable for the processing and preservation of samples.
Keywords
Cohort studies; Biological markers; Biological specimen banks; Protein stability; Sample preservation; Specimen handling
REFERÊNCIAS
- Völzke H, Alte D, Schmidt CO, Radke D, Lorbeer R, Friedrich N, et al. Cohort Profile: The Study of Health in Pomerania. Int J Epidemiol. 2011;40(2):294-307.
- Haverstick DM & Groszbach AR. Coleta de espécimes, processamento e outras variáveis pré-analíticas. In: Tietz Fundamentos de Química Clínica e Diagnóstico Molecular. Eds.: Burtis CA, Bruns DE. 7a ed., eBook, Rio de Janeiro: Elsevier, 2016, p. 15-61.
- Westgard JO. Managing quality vs. measuring uncertainty in the medical laboratory. Clin Chem Lab Med 2010;48(1):31-40. https://www.westgard.com/biodatabase1.htm).
- Bossuyt PM, Reitsma JB, Bruns DE, Gatsonis CA, Glasziou PP, Irwig L, et al; STARD Group. STARD 2015: An Updated List of Essential Items for Reporting Diagnostic Accuracy Studies. Clin Chem 2015;61(12):1446-52.
- Hirayama A, Sugimoto M, Suzuki A, Hatakeyama Y, Enomoto A, Harada S, et al. Effects of processing and storage conditions on charged metabolomic profiles in blood. Electrophoresis. 2015, doi: 10.1002/elps.201400600.
- Nishiumi S, Suzuki M, Kobayashi T, Yoshida M. Differences in metabolite profiles caused by pre-analytical blood processing procedures. J Biosci Bioeng. 2017 Dec 16. pii: S1389-1723(17) 30900-3.
- Jørgenrud B, Jäntti S, Mattila I, Pöhö P, Rønningen KS, Yki-Järvinen H, et al. The influence of sample collection methodology and sample preprocessing on the blood metabolic profile. Bioanalysis. 2015;7(8):991-1006.
- López-Bascón MA, Priego-Capote F, Peralbo-Molina A, Calderón-Santiago M, Luque de Castro MD. Influence of the collection tube on metabolomic changes in serum and plasma. Talanta. 2016 1; 150:681-9.
- Jansen EHJM, Beekhof PK, Viezeliene D, Muzakova V, Skalicky J. Long-term stability of oxidative stress biomarkers in human serum. Free Radic Res. 2017;51(11-12):970-97.
- Mechanic L, Mendez A, Merrill L, Rogers J, Layton M, Todd D, et al. Planned variation in preanalytical conditions to evaluate biospecimen stability in the National Children’s Study (NCS). Clin Chem Lab Med. 2013;51(12):2287-94.
- Jansen E, Beekhof P, Viezeliene D, Muzakova V, Skalicky J. Long-term stability of cancer biomarkers in human serum: biomarkers of oxidative stress and redox status, homocysteine, CRP and the enzymes ALT and GGT. Biomark Med. 2015;9(5):425-32.
- Shabihkhani M, Lucey GM, Wei B, Mareninov S, Lou JJ, Vinters HV, et al. The procurement, storage, and quality assurance of frozen blood and tissue biospecimens in pathology, biorepository, and biobank settings. Clin Biochem. 2014;47(4-5):258-66.
- Schuh MP, Nehus E, Ma Q, Haffner C, Bennett M, Krawczeski CD, Devarajan P. Long-term Stability of Urinary Biomarkers of Acute Kidney Injury in Children. Am J Kidney Dis. 2016;67(1):56-61.
- Gislefoss RE, Grimsrud TK, Mørkrid L. Stability of selected serum hormones and lipids after long-term storage in the Janus Serum Bank. Clin Biochem. 2015;48(6):364-9.
- Caixeiro NJ, Lai K, Lee CS. Quality assessment and preservation of RNA from biobank tissue specimens: a systematic review. J Clin Pathol. 2016;69(3):260-5.
- Zhou JH, Sahin AA, Myers JN. Biobanking in genomic medicine. Arch Pathol Lab Med. 2015;139(6):812-8.
Correspondência
Caio Mauricio Mendes de Cordova
Rua São Paulo 2171, Campus 3
Lab. de Bioquímica Clínica, sala A-503
89030-001 – Blumenau-SC, Brasil
E-mail: [email protected]
