Segurança transfusional no Brasil: dos primórdios ao NAT
Transfusion security in Brazil: from the beginnings to NAT
Thalita Soares Martins1
Juliana Oliveira de Toledo Nóbrega2
1Discente no Centro Universitário do Distrito Federal (UDF) – Brasília-DF, Brasil.
2Docente. Centro Universitário do Distrito Federal (UDF) – Brasília-DF, Brasil.
Instituição: Centro Universitário do Distrito Federal (UDF) – Brasília-DF, Brasil.
Conflito de interesses: Não há conflito e interesses
Recebido em 07/04/2018
Artigo aprovado em 07/11/2018
DOI: 10.21877/2448-3877.201800693
INTRODUÇÃO
A transfusão de sangue é largamente utilizada como tratamento coadjuvante de diversas doenças. Milhões de unidades de sangue de doadores são coletadas por ano e esse valor ainda é pequeno frente à demanda global, milhões ainda precisam ser coletados para atender à necessidade e garantir o fornecimento suficiente de hemocomponentes nos hemocentros, tanto públicos quanto privados, do mundo.(1) Em hemocentros de todo o mundo é realizado rígido controle para assegurar a qualidade dos serviços hemoterápicos e selecionar os doadores considerados aptos para se oferecer, cada dia mais, uma maior segurança ao receptor dos hemocomponentes.(2)
A Portaria n° 158 de 4 de fevereiro de 2016(3) torna imprescindível a quem pretende realizar uma doação de sangue efetuar o processo de triagem clínica, e somente passarão pela triagem sorológica aqueles que forem considerados aptos clinicamente. O ciclo hemoterápico, nome dado às séries de procedimentos pelos quais a amostra passa nos hemocentros brasileiros, consiste em triagem clínica, sorológica e imunológica, processamento das bolsas doadas, dispensação das idôneas e avaliação pós-transfusão.(4)
Quando se trata de hemoterapia, seus preceitos, quando seguidos à risca, trazem maior segurança ao paciente, pois diminuem a sua exposição a patógenos diversos.(4) A primeira etapa do ciclo hemoterápico é responsável pelo maior índice de inaptidão dos candidatos à doação e é de grande auxílio para reduzir a taxa de transmissão de doenças infecciosas em locais epidêmicos.(5) Porém, esta pode ser uma etapa passível de erro, portanto, o uso dos testes laboratoriais torna-se essencial para manter a segurança dos pacientes.
Os testes laboratoriais vêm sendo aperfeiçoados ao longo do tempo e se tornando cada vez mais sensíveis e específicos para detecção dos antígenos.(6) O teste mais sensível disponível no mercado é o Teste do Ácido Nucleico (NAT). Ele veio como uma solução para o problema de resultados falso-negativos, obtidos devido ao período de incubação, ou janela imunológica, período no qual ainda não existe a possibilidade de detecção de anticorpos no sangue.(7)
MATERIAl E MÉTODOS
Este trabalho constitui uma revisão bibliográfica realizada entre 2017 e início de 2018. Foram realizadas buscas em artigos científicos das principais plataformas aonde se encontram periódicos médicos como Lilacs, PubMed, NCBI, BVSMS, também SciELO e MedLine, utilizando-se ainda teses e dissertações relevantes sobre o tema.
A pesquisa foi realizada utilizando, principalmente, as palavras-chave “Doação de sangue”, “Serviços de Hemoterapia”, “Segurança”, “Doenças Sexualmente Transmissíveis”. O critério para a inclusão dos artigos no presente estudo foi o destaque que a pesquisa apresentou sobre a importância da doação de sangue assim como seus riscos e as melhorias que foram implementadas ao longo do tempo.
Leis e portarias sancionadas pelo governo foram selecionadas com base em cronologia e inovações que trouxeram para os hemocentros brasileiros.
No total foram selecionadas 36 referências entre artigos, teses e leis.
RESULTADOS E DISCUSSÃO
História do Banco de Sangue
A transfusão de sangue é um procedimento que se tornou indispensável quando se pensa em cuidados com a saúde. A cada segundo diversas pessoas necessitam de transfusão sanguínea, e este recurso salva milhões de pessoas por ano em todo o mundo.(8) Sua utilização como tratamento é diversificada, sendo usada em procedimentos cirúrgicos de risco, doenças sanguíneas como anemia aplásica, leucemias, emergências obstétricas, entre outras.(8) É um feito da medicina moderna que permite aumentar a expectativa e qualidade de vida de quem necessita deste procedimento como coadjuvante a outros ou mesmo para o sucesso de seu tratamento.(9)
O primeiro banco de sangue foi fundado por Percy Oliver, secretário de Estado na época, em 1921, na cidade de Londres. Sua criação veio decorrente da necessidade de soldados feridos na Primeira Guerra Mundial, obrigando-o a criar uma “lista de voluntários” que poderiam ser chamados assim que surgisse a necessidade por mais hemocomponentes. Na época, apenas se utilizavam, como triagem, exames físicos e testes laboratoriais para definir a tipagem sanguínea e a presença de sífilis no doador que, em caso positivo, era excluído da “lista de voluntários”. Esse sistema de serviço foi denominado British Red Cross Blood Transfusion Service, em tradução livre Serviço de Transfusão de Sangue da Cruz Vermelha. Outros países da Europa como França, Bélgica, Áustria e Alemanha empregaram sistemas semelhantes em seu sistema de saúde. Em 1937, na cidade de Chicago, finalmente, tem-se a estocagem de doações de sangue, a qual deu origem ao sistema de banco de sangue que temos atualmente.(10)
No Brasil, o primeiro relato de transfusão sanguínea bem-sucedida foi realizado pelo professor baiano Garcez Fróes em 1916 na Bahia. A partir do sucesso deste procedimento até então inovador, começa-se a montar um sistema simples com doadores universais e utilizando como metodologia a transfusão direta do doador ao receptor, pois ainda não se tinha a tecnologia de anticoagulação para preservação da amostra biológica. Em 1942, na cidade do Rio de Janeiro criou-se o primeiro banco de sangue brasileiro no Instituto Fernandes Figueira com a finalidade de auxiliar na recuperação de soldados enviados à Segunda Guerra Mundial.(11) Nesta época, a doação de sangue era um ato remunerado, porém, em 1949 surgiu o movimento contra a negociação desta amostra biológica. A Associação de Doadores Voluntários de Sangue dá início ao voluntariado e reforça a importância de ser um ato altruísta. No final da década de 40, a hematologia e hemoterapia tornou-se uma especialidade médica, contando com cursos e congressos.(12)
Histórico de leis que regem a doação de hemocomponentes
Em 1950 foi promulgada a Lei nº 1075, de 27 de março de 1950, sendo a primeira lei federal que regulamenta a doação de sangue no Brasil. Ela dispõe sobre a doação voluntária de sangue e a garantia ao trabalhador de ser dispensado de suas devidas funções trabalhistas no dia da doação.(13)
Na década de 60, apesar de existir a lei que regulamenta a doação, ainda ocorriam diversos erros, entre eles a comercialização ilegal do insumo biológico; o mais grave deles, no entanto, era o risco de transmissão de doenças via transfusão. Dentre as infecções transmissíveis, as principais são propagadas pela presença no sangue do Vírus da Imunodeficiência Humana – HIV, Vírus da Hepatite Humana B – HBV e Vírus da Hepatite Humana C – HCV e do Treponema pallidium.(12,14) O número de pessoas infectadas aumentou significativamente em decorrência de uma triagem que deixava a desejar.(12) O sistema brasileiro carecia de fiscalização mais rígida e a Organização Mundial da Saúde (OMS) enviou um representante para avaliar as questões relacionadas à hemoterapia no Brasil. Com os indicadores de qualidade muito abaixo do esperado, a necessidade de uma reformulação política ficou evidente.(15)
Desta forma, criou-se a Associação Brasileira de Doadores Voluntários (ABDVS) e sancionou-se o decreto-lei Nº 53988, de 30 de junho de 1964, no qual se reforça o ato de doação voluntária e cria-se o “Dia Nacional do Doador Voluntário de Sangue”.(16) Em 1965 foi criada a Comissão Nacional de Hemoterapia pelo Sistema Único de Saúde (SUS), cujo objetivo era regulamentar os serviços hemoterápicos nos hemocentros do Brasil. Segundo Junqueira e colaboradores,(11) “a Comissão Nacional de Hemoterapia e o Ministério da Saúde, através de decretos, portarias e resoluções, estabeleceu o primado da doação voluntária de sangue e a necessidade de medidas de proteção a doadores e receptores, disciplinou o fornecimento de matéria-prima para a indústria de fracionamento plasmático e a importação e exportação de sangue e hemoderivados”.
Com o passar do tempo, leis e decretos foram sendo criados para regularizar e atualizar o fluxo de etapas das doações de sangue. Focando cada vez mais na segurança do receptor dos hemocomponentes, entra em vigor a Portaria nº 1376 de 19 de novembro de 1993, que aprova Normas Técnicas para coleta, processamento e transfusão de sangue a fim de que se obtenha maior garantia da qualidade nos processos de hemoterapia.(17) A Portaria nº 127 de 24 de novembro de 1995 institui que todos os bancos de sangue do Brasil devem implementar e seguir as “Normas Gerais de Garantia de Qualidade para Unidades Hemoterápicas”.(18) A lei mais completa e atual que está em vigor no Brasil é a Portaria 158 de 2016.
De acordo com a Portaria n° 158 de 4 de fevereiro de 2016, a doação de sangue é uma atitude altruísta, voluntária, sigilosa e é vetado ao doador receber qualquer benefício advindo de seu ato. É indispensável que o doador passe por triagem clínica, hematológica e sorológica (Figura 1).(19) A triagem clínica é um processo de identificação do doador, onde se analisa o perfil do candidato através do preenchimento de formulários. O segundo passo é uma entrevista sigilosa para a análise do histórico de saúde e hábitos de vida para se determinar se o doador tem perfil para a doação.(4) Em caso de todos os parâmetros estarem em conformidade com a Portaria 158/16, o doador é encaminhado para a coleta sanguínea e são realizados os testes sorológicos, cujo objetivo é evitar a infecção dos indivíduos que receberão os hemocomponentes, garantindo assim sua proteção.(20) A limitação do processo de triagem clínica e entrevista vem da possibilidade de omissão de fatos, muitas vezes por vergonha por parte do doador ou mesmo por olvidar situações passadas. Logo, a triagem laboratorial torna-se imprescindível para a segurança do paciente, uma vez que testes laboratoriais são mais exatos e precisos do que a memória humana.
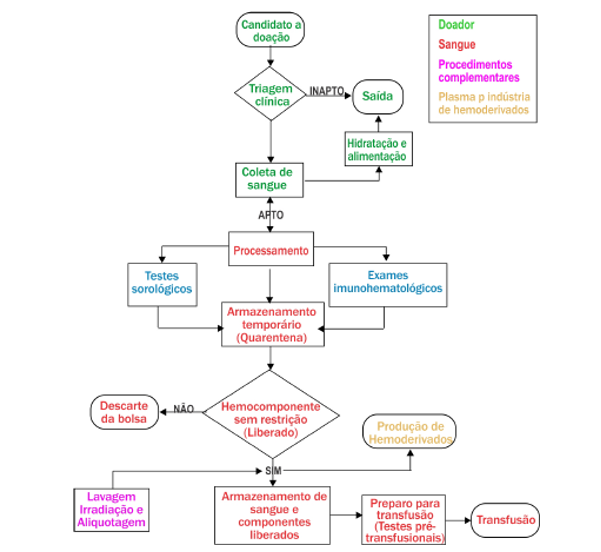
Figura 1. Fluxograma do ciclo do sangue.
A importância da segurança transfusional
É indiscutível a importância que a transfusão de sangue tem no tratamento de pacientes, no entanto, essa prática não está livre de riscos, existem múltiplos fatores que podem levar o paciente a apresentar uma complicação pós-transfusional.(21) Dentre as diversas preocupações com a segurança do paciente a mais iminente é o risco de contaminação de doenças infecciosas. O primeiro caso conhecido de contaminação efetiva de doença via transfusão de sangue foi em 1943 com a transmissão da hepatite B. Após este caso ser difundido à população, diversos outros casos foram relatados e publicados relacionando o aparecimento de hepatites virais logo após a transfusão sanguínea.(22) Segundo Carrazzone e colaboradores (2004),(4) “a transmissão de patógenos através da transfusão necessita basicamente que o doador tenha o agente circulante em seu sangue, que os testes de triagem sorológica não sejam capazes de detectá-lo e que o hospedeiro seja susceptível”.
Com o envelhecimento populacional e o aumento do número de acidentes, houve, por consequência, o aumento da demanda por hemocomponentes assim como a preocupação pela segurança transfusional. Para tal, os parâmetros de qualidade tornaram-se mais rígidos e específicos para que se tenha maior qualidade nos exames e precisão nos diagnósticos.(2)
O Brasil tem aproximadamente quatro milhões de coletas e doações por ano. A qualidade na detecção de patógenos é uma preocupação crescente nas últimas décadas pois se trata de segurança na saúde pública.(23) Embora os progressos na área sejam significativos, a maior ameaça à segurança transfusional é a doação por parte de pessoas contaminadas com HIV, HBV e HCV, que estão passando por soroconversão, visto que é um período assintomático.(24-26)
Suárez e colaboradores(27) destacam que atenção, cuidados e investimento nesta área reduzem significativamente os riscos inerentes à recepção de hemocomponentes. As estratégias para identificação de doadores capazes de infectar os receptores dos hemocomponentes são modificadas ao longo do tempo de acordo com o avanço da tecnologia, que possibilita a melhora de estratégias e exames laboratoriais disponíveis nos hemocentros.(6)
O teste do Ácido Nucleico
Neste contexto, novas pesquisas de diagnósticos possibilitaram a utilização de testes que detectam anticorpos formados pelo sistema imunológico após a infecção, os quais se tornaram padrão ouro. Logo após, surgiram os testes para detecção de antígenos e, por volta da década de 90, veio o surgimento do Teste de Amplificação do Ácido Nucleico, do inglês Nucleic Acid-AmplificationTesting (NAT).(28)
O NAT é uma técnica implementada nos hemocentros públicos e privados de diversos países desde 1997, sendo a hemorrede da Inglaterra a pioneira na sua utilização, seguida dos Estados Unidos da América, e com a qual se analisaram todas as doações voluntárias para HCV e HIV do tipo 1.(29) A decisão da sua implementação se baseou na sua alta especificidade e capacidade técnica de detectar a presença do antígeno antes da soroconversão, o que reduz consideravelmente o risco remanescente de transmissões virais adjuntas à janela de conversão.(30) No Brasil, sua utilização começou a partir de 2004, quando o governo, por meio da portaria nº 112/2004,(31) determinou a implantação em toda a Hemorrede Nacional a realização dos testes de NAT para HIV, HBV e HCV em todas as amostras de sangue doadas. A RDC nº 57 da Agência de Vigilância Sanitária (Anvisa) de 16 de dezembro de 2010(32) reafirma a necessidade da utilização do NAT e afirma que a técnica é complementar a outros testes imunológicos de detecção de anticorpos, tornando-se um teste padrão ouro e confirmatório em caso de dúvidas em outros testes.
O NAT se baseia na detecção do genoma viral utilizando a metodologia Reação em Cadeia da Polimerase em Tempo Real (RT-PCR) para amplificar o ácido ribonucleico (RNA) viral presente em amostras contaminadas. O kit NAT utilizado atualmente nos hemocentros brasileiros é a Plataforma NAT HIV/HCV Bio-Manguinhos®. De acordo com Petry,(33) “o ensaio consiste na preparação de um pool ou conjunto de seis amostras juntamente com uma partícula calibradora biossegura, a extração automatizada de ácidos nucleicos e a sua purificação. A partícula calibradora adicionada ao pool de amostras participa de todas as etapas do processo de testagem. Trata-se de um vírus HIV/HCV mimético, biosseguro que exerce a função de controlar as condições ideais da reação, funcionando como um controle intraensaio. Este calibrador interno possui mutações genômicas, o que o diferencia estruturalmente das características comuns do vírus selvagem tornando-o não infeccioso”.
Ainda de acordo com o autor, para que se tenha a extração e a purificação do RNA viral, as amostras são expostas (com solução tampão e carreador de RNA) à quebra do RNA devido ao aquecimento. Logo após retira-se uma parte da solução e ocorre a lavagem do produto restando o RNA viral purificado.
Por detectar a presença do antígeno, a metodologia NAT é altamente sensível e específica e, exatamente por isso, ela apresenta uma vantagem que a torna indispensável nos hemocentros brasileiros: ela diminui consideravelmente a janela imunológica.(29)
Por janela imunológica entende-se o período entre a infecção com o antígeno e a produção de anticorpos pelo organismo. Nesse período, que varia para cada agente viral, os testes que visam à detecção de anticorpos tornam-se falhos, podendo apresentar resultados falsos negativos uma vez que a amostra sanguínea não possui quantidade considerável de marcadores sorológicos, e a consequência dessa falha é a possível contaminação do receptor da amostra biológica.(33)
Para se compreender o período de janela imunológica, deve-se atentar para a resposta do homem frente ao vírus. A infecção viral pode ser separada em quatro fases tais como:(34)
- a) Fase da infecção: o vírus entra no organismo por um pequeno foco inicial de replicação e se espalha por via linfática ou venosa, atingindo células saudáveis e as utilizando para se multiplicar.
- b) Fase de eclipse: é a fase após aquela na qual o hospedeiro acabou de se infectar com o vírus. Aqui se apresenta o período de janela imunológica. O vírus se replica lentamente, e o hospedeiro ainda não apresenta quantidade significativa de antígenos e anticorpos no organismo a ponto de testes sorológicos menos sensíveis os detectarem. Nesta fase, a imunidade natural do organismo tenta combater o vírus com todo o seu potencial.
- c) Fase de crescimento exponencial: nesta fase tem-se o crescimento acentuado da população viral. As células alvo são infectadas em proporção maior do que o sistema imunológico do indivíduo infectado consegue combatê-lo. Nesta fase se apresentam sinais e sintomas da infecção e antígenos e anticorpos são detectáveis em exames sorológicos.
- d) Fase plateau: nesta fase, a carga viral diminui e se estabiliza no organismo do indivíduo infectado devido a mecanismos de defesa do sistema imunológico. Em infecções crônicas tem-se o estado estacionário, também conhecido como “ponto de ajuste”; em infecções curadas tem-se a eliminação total do vírus do indivíduo.
De acordo com pesquisas de Kumar e colaboradores, a janela imunológica do HIV passa de 15-20 dias para 4, aproximadamente; para o HBV, de 50-150 dias tornam-se 14 dias, aproximadamente; para o HCV transforma-se de 26 semanas para dois dias, aproximadamente.(35)
Desta forma, a técnica NAT permite a verificação de forma fidedigna, como consequência da diminuição drástica da janela imunológica, casos de sorologia negativa que, com outras metodologias, passariam despercebidos.(6)
CONSIDERAÇÕES FINAIS
Como visto, desde a criação do banco de sangue a transmissão de DSTs era um problema a ser superado e o que se tinha de conhecimento e tecnologia na época permitia a realização de testes para detecção de sífilis. O controle de DSTs é, ainda hoje, um grande problema de saúde pública no Brasil. Segundo Araújo & Silveira,(36) “vários fatores interferem para o seu controle, tendo, como destaque, o comportamento da população, as questões de gênero, a cultura, os costumes”.
A crescente taxa de índices de DSTs, principalmente AIDS, juntamente com aumento da demanda por hemocomponentes por diversos motivos, trouxe um cenário de preocupação pela segurança transfusional, fazendo com que esse assunto ganhasse evidência. Para tal, os parâmetros de qualidade tornaram-se mais rígidos e específicos.
Mesmo sem descartar a possibilidade de infecção verifica-se que, com o aumento da biotecnologia nas últimas décadas, houve grande diligência dos serviços de hemoterapia em produzir testes de triagem cada vez mais rígidos. Os testes de análise sorológica empregados na pesquisa de antígenos atualmente aplicados em bancos de sangue públicos e privados foram ganhando características para se obter alta sensibilidade e, assim, fornecer maior confiabilidade nos seus resultados.(34)
Mantendo essa preocupação com os serviços hemoterápicos, a Hemorrede brasileira implantou em sua rotina laboratorial o que há de mais moderno no mercado: a pesquisa de ácidos nucleicos por métodos de biologia molecular.
É nítido que o NAT veio para trazer a segurança que faltava, não com 100% de certeza, mas com precisão e eficácia não vistas até então.
Abstract
Currently, blood donation is currently considered a voluntary and unpaid act. Millions of blood bags are collected annually and their quality is decisive for the treatment of many people. Ensuring a good origin of these bags is of fundamental importance, and Brazilian blood centers follow a protocol of measures called hemotherapy” cycle in which the clinical, immunological and serological analysis of these bags is simultaneously. The aim of this study was to present the historical context of the creation of blood banks and to make a parallel between the deficiencies and margins of error left by the serological tests and the Nucleic Acid Test (NAT), as the latest in screening tests in blood banks today.
Keywords
Blood donors; Hemotherapy service; Sexually transmitted diseases
REFERÊNCIAS
- Shenga N, Thankappan KR, Kartha CC, Pal R. Analyzing sociodemographic factors amongst blood donors. J Emerg Trauma Shock. 2010;(3):21-5.
- Ferreira DM, Griza D, Sisti E. Análise dos aspectos epidemiológicos, hematológicos e sorológicos presentes em doadores de sangue do Hemocentro Regional de Cruz Alta/ RS. Rev Bras Anal Clin. (Rio de Janeiro) 2012;44(1):10-4.
- Ministério da Saúde (Brasil). Portaria no. 158, de 04 de fev de 2016. Aprova o Regulamento Técnico de Procedimentos Hemoterápicos. Diário Oficial da União 05 de feb 2016; seção 2.
- Carrazzone CFV, Brito AM, Gomes YM. Importância da avaliação sorológica pré-transfusional em receptores de sangue. Rev. Bras. Hematol. Hemoter. [periódicos na internet]. 2004;26(2):93-98. Disponível em: http://www.scielo.br/scielo.php?script=sci_ arttext&pid=S1516-84842004000200005& lng=en.
- Bastos MRD. Principais causas de inaptidão clínica entre doadores de sangue no HBH entre Janeiro e Junho de 2007. Jornal Hemominas. 2007;18(3):6.
- Velati C, Romanò L, Fomiatti L, Baruffi L, Zanetti AR; SIMTI Research Group. Impact of nucleic acid testing for hepatitis B virus, hepatitis C virus, and human immunodeficiency virus on the safety of blood supply in Italy: a 6-year survey. Transfusion. 2008 Oct;48(10):2205-13. doi: 10.1111/j.1537-2995.2008.01813.x.
- Kupek E. Residual risk of hepatitis-B-infected blood donations: estimation methods and perspectives. International Scholarly Research Notices. v. 2013. Article ID 839896, 15 pages. Avaiable from: http://dx.doi.org/10.5402/2013/839896
- World Health Organization (WHO). Universal Access to Safe Blood Transfusion, 2008.Global Consultation on Universal Access to Safe Blood Transfusion, 9-11 June 2007..[acesso em 17 de mar 2017]. Disponível em: http://www.who.int/bloodsafety/ publications/UniversalAccesstoSafeBT.pdf.
- Salazar M. Guías para la transfusión de sangre y sus componentes. Rev Panam Salud Publica. 2003;13(2/3)183-90.
- Giangrande PLF. The history of blood transfusion.Br J Haematol. 2000 Sep;110(4):758-67. doi: 10.1046/j.1365-2141.2000.02139.x
- Junqueira PC, Rosenblit J, Hamerschlak N. História da Hemoterapia no Brasil. Rev. Bras. Hematol. Hemoter. [periódicos na internet]. 2005 Sep;27(3):201-7. Available from: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1516-84842005000300013 &lng=en. http://dx.doi.org/10.1590/S1516-84842005000300013.
- Pereima RSMR, Reibnitz KS, Martini JG, Nitschke RG. Doação de sangue: solidariedade mecânica versus solidariedade orgânica. Rev Bras Enferm. 2010 mar-abr;63(2):322-7. Disponível em: http://www.scielo.br/pdf/reben/v63n2/24.pdf.
- Brasil, Lei no. 1075 de 27 de março de 1950. Dispõe sobre a doação voluntária de sangue. Diário Oficial da União 12 mar 1950; seção 1.
- Chandekar SA, Amonkar GP, Desai, HM, Valvi N, Puranik GV. Seroprevalence of transfusion transmitted infections in healthy blood donors: A 5-year Tertiary Care Hospital experience. J Lab Physicians. 2017 Oct-Dec;9(4):283-7. doi: 10.4103/0974-2727.214246.
- Pereima RSMR, Arruda MW, RKS, Gelbcke FL. Projeto Escola do Centro de Hematologia e Hemoterapia de Santa Catarina: uma estratégia de política pública. Texto contexto – enferm. [periódicos na internet]. 2007 Sep [acesso em 16 de set 2017];16(3):546-52. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext &pid=S0104-07072007000300022&lng=en.
- Brasil, Decreto-Lei no. 53988 de 30 de junho de 1964. Institui o Dia Nacional do Doador Voluntário de Sangue. Diário Oficial da União 30 jun 1964; seção 1.
- Ministério da Saúde (Brasil). Portaria no. 1376 de 19 de novembro de 1993. Aprova alterações na Portaria no. 721/GM, de 09.08.89, que aprova Normas Técnicas para coleta, processamento e transfusão de sangue, componentes e derivados, e dá outras providências. Diário Oficial da União 02 dez de 1993; seção 1.
- Agência Nacional de Vigilância Sanitária (Brasil). Portaria no. 121 de 24 de novembro de 1995. Normas gerais de garantia na qualidade em unidades hemoterápicas. Diário Oficial da União, 30 Nov 1995.
- Agência Nacional de Vigilância Sanitária (Anvisa). Manual técnico para investigação da transmissão de doenças pelo sangue. Brasília: Ministério da Saúde, 2004;
- Borelli, SD, Mazzola JC, Matta ACG, Takemoto AY, Bértoli M. Blood discard rate and the prevalence of infectious and contagious diseases in blood donors from provincial towns of the state of Parana, Brazil. Rev Bras Hematol Hemoter. 2013;35(6):395-9. doi: 10.5581/1516-8484.20130126.
- Ferreira O, Martinez EZ, Mota CA, Silva AM. Avaliação do conhecimento sobre hemoterapia e segurança transfusional de profissionais de enfermagem. Rev. Bras. Hematol Hemoter. [periódicos na internet] 2007 Jun [acesso em 10 set 2018]; 29(2): 160-7. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid= S1516-84842007000200015&lng=en.
- Souza MA. Avaliação da segurança transfusional por meio do estudo soroepidemiológico das Hepatites Virais B, C, de HIV-I/II e de citomegalovírus em doadores de sangue do Hemocentro Regional de Lages. Florianópolis. Dissertação [Mestrado em análises clínicas]. Universidade Federal de Santa Catarina (UFSC); 2004.
- Levi JE, Pereira RA, Polite MB, Mota MA, Nunez SP, Pinho JR, et al. One window-period donation in two years of individual donor-nucleic acid test screening for hepatitis B, hepatitis C and human immunodeficiency virus. Rev Bras Hematol Hemoter. 2013;35(3): 167-70.
- Schreiber GB, Busch MP, Kleinman SH, Korelitz JJ. The risk of transfusion-transmitted viral infections. The Retrovirus Epidemiology Donor Study. N Engl J Med. 1996 Jun;334(26):1685-90.
- Zheng X, Ding W, Li G, Wu Y, Wu D, Zhu H, et al. Seroprevalence of Transfusion-Transmissible Infectious Agents among Volunteer Blood Donors between 2006 and 2012 in Zhejiang, China. Blood Transfus. 2015 Jul;13(3):401-10. doi: 10.2450/2015.0271-14.
- Mühlbacher A, Schennach H, van Helden J, Hebell T, Pantaleo G, Bürgisser P, et al. Performance evaluation of a new fourth-generation HIV combination antigen-antibody assay. Med Microbiol Immunol. 2013 Feb;202(1):77-86. doi: 10.1007/s00430-012-0250-5.
- Suárez G, Eranilde L, Freitas F, Henry A, Hannaoui R, Erika J, Gómez A, Lisbeth J. Prevalencia de enfermedades infecciosas de transmisión sanguínea endonantes que asisten al Banco de Sangre del Hospital Universitario Antonio Patricio de Alcalá, Cumaná, Estado Sucre. Kasmera. 2007;35(1):56-64.
- Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção Hospitalar e de Urgência. Implantação e rotina dos testes de ácidos nucleicos (NAT) em serviços de hemoterapia – manual operacional. Brasília, Ministério da Saúde, 2013.
- Hans R, Marwaha N. Nucleic acid testing-benefits and constraints. Asian J Transfus Sci. 2014 Jan-Jun;8(1):2-3. doi: 10.4103/0973-6247.126679.
- Stramer SL, Glynn SA, Kleinman SH, Strong DM, Caglioti S, Wright DJ, et al; National Heart, Lung, and Blood Institute Nucleic Acid Test Study Group. Detection of HIV-1 and HCV infections among antibody-negative blood donors by nucleic acid-amplification testing. N Engl J Med. 2004 Aug;351(8):760-8.
- Agência Nacional de Vigilância Sanitária (Brasil). Portaria no. 112, de 29 de janeiro 2004. Dispõe sobre a implantação, no âmbito da Hemorrede Nacional, da realização dos testes de amplificação e detecção de ácidos nucléicos (NAT), para HIV e HCV. Diário Oficial da União 30 de jan 2014; Seção 1.
- Agência Nacional de Vigilância Sanitária (Brasil). RDC no. 57 de 16 de dezembro de 2010. Determina o Regulamento Sanitário para Serviços que desenvolvem atividades relacionadas ao ciclo produtivo do sangue humano e componentes e procedimentos transfusionais. Diário Oficial da União 16 de dez 2010; seção 1.
- Petry A. Implantação dos testes de amplificação de ácidos nucléicos HIV/HCV Bio-Manguinhos na triagem de doadores de sangue: questões epidemiológicas e logísticas. Florianópolis. Tese [Doutorado em Saúde Coletiva]. Universidade Federal de Santa Catarina. Florianópolis; 2013.
- Kleinman SH, Lelie N, Busch MP. Infectivity of human immunodeficiency virus-1, hepatitis C virus and hepatitis B virus and risk of transmission by transfusion. Transfusion. 2009 Nov; 49 (11):2454-89. doi: 10.1111/j.1537-2995.2009.02322.x.
- Kumar R, Gupta S, Kaur A, Gupta M. Individual donor-nucleic acid testing for human immunodeficiency virus-1, hepatitis C virus and hepatitis B virus and its role in blood safety. Asian J Transfus Sci. 2015 Jul-Dec;9(2):199-202. doi: 10.4103/0973-6247.154250.
- Araújo MAL, Silveira CB, Vivências de mulheres com diagnóstico de doença sexualmente transmissível – DST. Esc. Anna Nery [periódicos na internet]. 2007 Sep;11(3):479-486. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1414-81452007000300013&lng=en.
Correspondência
Thalita Soares Martins
Centro Universitário do Distrito Federal
SEP/SUL EQ704 / 904 Conj.A
70390-045 Brasília – DF, Brasil
