Perfil de suscetibilidade a antimicrobianos de cepas de Acinetobacter baumannii e Pseudomonas aeruginosa isoladas em amostras de lavado traqueal
Antimicrobial resistance profile of Acinetobacter baumannii and Pseudomonas aeruginosa strains isolated from tracheal lavage samples
Patricia Guedes Garcia1
Tais Reis Chain2
Amanda do Carmo Gusmão3
Leonardo Romaniello Gama de Oliveira3
1Coordenadora do Programa de Residência Multiprofissional em Saúde da Faculdade de Ciências Médicas e da Saúde de Juiz de Fora – Suprema, vinculada ao Hospital e Maternidade Therezinha de Jesus (HMTJ). Juiz de Fora-MG, Brasil.
2Programa de Residência Multiprofissional em Análises Clínicas da Faculdade de Ciências Médicas e da Saúde de Juiz de Fora – Suprema, vinculada ao Hospital e Maternidade Therezinha de Jesus (HMTJ). Juiz de Fora-MG, Brasil.
3Faculdade de Ciências Médicas e da Saúde de Juiz de Fora – Suprema, Curso de Medicina – Juiz de Fora.
Instituição: Faculdade de Ciências Médicas e da Saúde de Juiz de Fora – Suprema. Juiz de Fora-MG, Brasil.
Conflito de interesses: não há conflito de interesses.
Suporte financeiro: financiamento próprio.
Recebido em 05/11/2020
Aprovado em 14/01/2021
DOI: 10.21877/2448-3877.202000918
INTRODUÇÃO
A pneumonia é a principal causa de infecções relacionadas à assistência à saúde (IRAS), sobretudo em Unidades de Terapia Intensiva (UTIs). Essa patologia ocorre em mais de 90% dos casos que envolvem pacientes submetidos à intubação endotraqueal e à ventilação mecânica (VM). A pneumonia associada à ventilação mecânica (PAV) é de grande preocupação devido à sua alta incidência, a qual está associada ao aumento da mortalidade, dos custos e do tempo de internação hospitalar.(1) A PAV ocorre geralmente em pacientes submetidos à VM após 48 horas.(2,3)
Cerca de 10% a 20% dos pacientes que necessitam de VM desenvolvem pneumonia, que, normalmente, associa-se a altas taxas de mortalidade.(4) Os agentes etiológicos da PAV incluem patógenos hospitalares comuns, tais como: Pseudomonas sp., Acinetobacter sp. e outros membros da família Enterobacteralis, Staphylococcus aureus e Candida sp.(4) Segundo Parisi et al.,(2) a PAV é a infecção mais grave associada à assistência à saúde e é a principal causa de morbimortalidade por infecções relacionadas a dispositivos.(2)
O surgimento de cepas multirresistentes associadas à PAV está intimamente relacionado ao uso excessivo de antibióticos de amplo espectro no início da terapia intensiva. Esse fato decorre do uso empírico em larga escala, o qual é um entrave para a saúde pública e, portanto, não pode ser negligenciado.(4,5)
Dessa forma, é de grande importância dos programas locais de vigilância da PAV, cujo objetivo é orientar corretamente a terapia empírica. Dessa forma, estudos epidemiológicos em pacientes sob VM são de extrema necessidade, a fim de se obter maior conhecimento acerca da microbiota local, bem como de seus perfis de resistência para uso racional de antibióticos hospitalares.(6,7)
Assim sendo, é essencial que se investigue a preva-lência de bactérias patogênicas em secreções respiratórias de pacientes ventilados, com o objetivo de avaliar o perfil de suscetibilidade destes aos antimicrobianos. Tendo em vista que as bactérias não fermentadoras como Acinetobacter baumannii e Pseudomonas aeruginosa apresentam elevada prevalência como agentes de PAV, este estudo objetiva avaliar seus padrões de resistência aos antimicrobianos em amostras de lavado traqueal de pacientes hospitalizados em UTIs de um hospital de ensino da cidade de Juiz de Fora, Minas Gerais, Brasil.
MATERIAL E MÉTODOS
Trata-se de um estudo retrospectivo, transversal, descritivo, no qual foram coletados os resultados de cultura de aspirado traqueal, utilizando o banco de registros do Serviço de Controle de Infecção Hospitalar (SCIH) de um hospital público na cidade de Juiz de Fora, MG, no período de janeiro a dezembro de 2018.
Incluíram-se neste estudo amostras de pacientes maiores de 18 anos, de ambos os sexos, que estavam sob ventilação mecânica por mais de 48 horas em UTIs e com suspeita clínica de pneumonia. Foram excluídas as amostras dos indivíduos provenientes da enfermaria hospitalar e da UTI neonatal.
As amostras de aspirado traqueal foram obtidas por meio de sonda de aspiração de pacientes intubados e em uso de aparelho de ventilação mecânica. A coleta foi realizada em frasco estéril acoplado a um sistema de sucção.(8,9)
As amostras foram semeadas em Ágar Sangue e Ágar Mac Conckey(RenyLab®, Química e Farmacêutica), utilizando-se alça calibrada de 1 microlitro. As placas foram incubadas em estufa de aerobiose (Fanem® 502 São Paulo – Brasil) por 24/48 horas a 37oC ± 1oC. As colônias isoladas foram previamente caracterizadas macroscopicamente pela observação de sua morfologia e aspecto e, quando necessário, pela morfologia e coloração de Gram. Foram consideradas contagens maior ou igual a 105 UFC/mL.(8,9)
Para se identificarem os bacilos gram-negativos (BGN) foram utilizados o meio IAL (Instituto Adolfo Lutz), citrato e os aminoácidos lisina, ornitina e arginina. As bactérias não fermentadoras foram identificadas pelo crescimento em ágar MacConkey, prova da oxidase, motilidade, OF glicose e IAL.(10) O Teste de Sensibilidade aos Antimicrobianos (TSA) foi realizado pela técnica de disco-difusão em placa e os possíveis mecanismos de resistência foram identificados de acordo com o Clinical and Laboratory Standards Institute (CLSI).(11)
Frequências absolutas e relativas foram utilizadas para análise descritiva por meio do software Statistical Package for the Social Sciences (SPSS) for Windows versão 17.0.
Ética
Este estudo foi previamente aprovado pelo Comitê de Ética Institucional, conforme a resolução 466/12 do Conselho Nacional de Saúde.
RESULTADOS
Foram analisadas 469 amostras de lavado traqueal de pacientes adultos (>18 anos) internados em UTIs de um hospital público, de janeiro a dezembro de 2018. Em 198 (42,21%) não houve crescimento de nenhum micro-organismo. Em 29 (6,18%) houve cultura mista, com crescimento de mais de três tipos de micro-organismos e foram consideradas amostras contaminadas.
Houve crescimento microbiano em 242 amostras de lavado traqueal, Destas, 230 foram monomicrobianas e 12 revelaram dois micro-organismos, que foram considerados por apresentarem contagem ³106 UFC/mL. Por conseguinte, essas amostras totalizaram 254 cepas com crescimento microbiano, e, destas, 237 eram cepas bacterianas e 17 cepas fúngicas, que não foram objeto deste estudo. A Figura 1 apresenta as prevalências dos micro-organismos isolados em amostras de lavado traqueal com contagem >106 UFC/mL.
Além destas, obtiveram-se 25 cepas de Staphylococcus aureus, oito de Candida albicans, oito de Serratia sp., sete de Acinetobacter sp., sete de Proteus mirabilis, sete de Enterobacter cloacae, seis de Escherichia coli, cinco de SCN, cinco de Streptococcus pneumoniae, cinco de Stenotrophomonas sp., quatro de Klebsiella aerogenes, duas de Providencia sp., uma de Klebsiella oxytoca, uma de Klebsiella ozaenae, uma de Morganella morgani, uma de Proteus sp., uma de Streptococcus sp.
Das 237 cepas isoladas, foi avaliado o perfil de suscetibilidade aos antimicrobianos de Acinetobacter baumannii e Pseudomonas aeruginosa. A frequência de Acinetobacter baumannii isolado foi de 59 (24,89%), enquanto de Pseudomonas aeruginosa foi de 45 (18,98%). Estes dados estão representados no Gráfico 1.
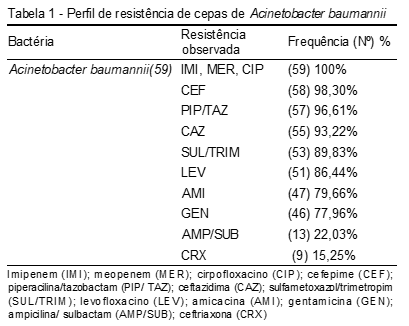
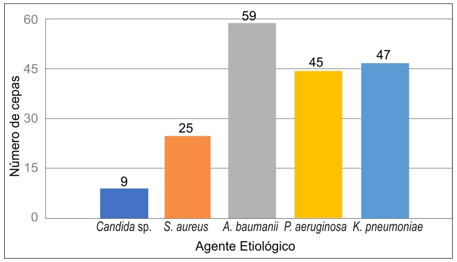
Gráfico 1. Maiores prevalências de cepas encontradas em mostras de lavado troqueal
Foram testados para Acinetobacter baumannii os antimicrobianos: ceftazidima (CAZ), cefepime (CEF), ceftriaxona (CRX), amicacina (AMI), ampicilina/ sulbactam (AMP/SUB), cirpofloxacino (CIP), levofloxacino (LEV), gentamicina (GEN), sulfametoxazol/trimetropim (SUL/TRIM), piperacilina/tazobactam (PIP/ TAZ), imipenem (IMI) e meropenem (MER). O perfil de resistência está representado na Tabela 1.

Nota-se que todas as cepas (100%) de A. baumannii foram resistentes aos carbapenêmicos testados (Imipenem e meropenem) e também à quinolona (ciprofloxacino). Já a fluorquinolona (levofloxacino) apresentou taxa de resistência de 86,44%. Também mostraram altas taxas de resistência às cefalosporinas de 3ª e 4ª gerações, ceftazidima e cefepime, respectivamente (93,22% e98,3%). Com relação aos aminoglicosídeos (amicacina e gentamicina), os micro-organismos apresentaram altas taxas de resistência (79,66% e 77,76%). As associações piperacilina + tazobactam (96,61%) e sulfametoxazol+trimetropim (89,83%) tampouco se mostraram eficazes. Ampicilina + sulbactam, 22,03% e ceftriaxona, 15,25%.
Foram testados para Pseudomonas aeruginosa os antibióticos: ceftazidima (CAZ), cefepime (CEF), amicacina (AMI), ciprofloxacino (CIP), levofloxacino (LEV), gentamicina (GEN), piperacilina/tazobactam (PIP/TAZ), imipenem (IMI) e meropenem (MER). O perfil de resistência encontra-se na Tabela 2.
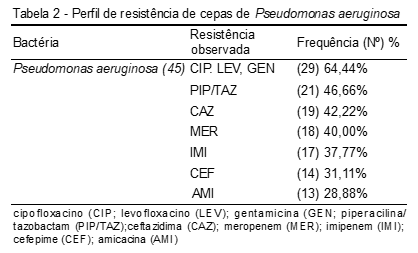
Nos isolados de Pseudomonas aeruginosa, 64,44% foram resistentes a ciprofloxacino, levofloxacino e gentamicina; 46,66% a piperacilina + tazobactam, 42,22% a ceftazidima. Já em relação aos carbapenêmicos, 40% foram resistentes ao neropenem e 37,77% ao imipenem. Ceftriaxona 31,11% e amicacina 28,88%.
DISCUSSÃO
Desde o início da terapia intensiva, uma das principais complicações durante a internação é a pneumonia hospitalar. A pneumonia é a principal causa de IRAS e ocorre frequentemente em pacientes submetidos à VM.(12,14) Apesar de a VM ser uma ferramenta essencial das UTIs modernas, ela está associada a um risco substancial de PAV, que é a infecção nosocomial mais comum em UTIs, com uma taxa de incidência variando de 7% a mais de 40% dos pacientes intubados por mais de 48 horas, associando-se a altos custos de assistência à saúde, aumento da morbidade, hospitalização prolongada, além de ser a causa número um de morte por infecção nosocomial nos Estados Unidos.(3,13,16) Devido à sua relevância clínica e seu perfil epidemiológico, a PAV é estudada com particularidade dentro das pneumonias nosocomiais, representando um dos principais desafios atuais da clínica médica.(14)
O Acinetobacter baumannii é um dos mais importantes patógenos causadores de IRAS.(13) São bactérias ubíquas e colonizam superfícies, pele e trato gastrointestinal de seres humanos, além de serem encontradas também em instrumentos no ambiente hospitalar. São considerados patógenos oportunistas, raramente causando infecções comunitárias.(18) O Acinetobacter sp. acomete, principalmente, pacientes hospitalizados que foram submetidos a procedimentos invasivos ou imunodeprimidos. Essa bactéria é responsável por diferentes tipos de infecção, dentre elas: pneumonias, septicemias, meningites e infecções urinárias.(16,18) O gênero Acinetobacter sp. possui elevada versatilidade nutricional e metabólica, podendo adaptar-se facilmente a diferentes ambientes, além de ser resistente ao ressecamento e a amplas faixas de temperatura e de pH.(16,18) A formação de biofilme facilita a adesão bacteriana a materiais plásticos como cateteres e tubos de VM, favorecendo a colonização e infecção dos pacientes.(15,18)
As infecções por Acinetobacter sp. são cada vez mais graves e mais difíceis de controle devido à sua sobrevivência ambiental prolongada, cuja disseminação tem sido associada à contaminação de equipamentos hospitalares e/ou através das mãos colonizadas da equipe assistencial.(15,16,18) Algumas espécies foram isoladas de objetos inanimados, como bancadas, leitos, ventiladores etc.(18) Desde o início da década de 1970, isolados de Acinetobacter baumannii e Pseudomonas aeruginosa têm progressivamente acumulado resistência a múltiplos agentes antimicrobianos, tais como penicilinas, cefalos-porinas, quinolonas e aminoglicosídeos.(13,18,19) Sendo assim, o tratamento é tão crítico que os carbape-nê-micos são a terapia de escolha para essas infecções.(13,18,19)
O aumento da frequência de infecções hospitalares associadas a espécies de Acinetobacter e Pseudomonas e a resistência dos mesmos aos antimicrobianos têm se tornado um grave problema de saúde pública.(16,19) Essa ameaça crescente em pacientes hospitalizados gera aumento da morbimortalidade relacionada à alta pressão seletiva de antimicrobianos comumente usados.(13,19) Sabe-se que a terapia antimicrobiana empírica inadequada afeta adversamente o desfecho na PAV e precisa ser adaptada à ecologia microbiana da instituição e ao tempo que o paciente ficou hospitalizado antes que a pneumonia se desenvolva.(13,19) Assim, o entendimento dos mecanismos de resistência, responsáveis por esta situação, e de práticas adequadas de controle de infecção são de fundamental importância para o melhor manejo das infecções hospitalares.(16,19)
Opções terapêuticas tornam-se progressivamente mais limitadas e a resistência antimicrobiana destes micro-organismos está associada a diversos mecanismos.(17) O principal método de resistência a b-lactâmicos é a produção de b-lactamases. A resistência aos carbapenêmicos pode ocorrer pela combinação de diferentes mecanismos: diminuição da permeabilidade das membranas externas, alteração na afinidade das proteínas ligadoras de penicilinas e, raramente, pelas bombas de efluxo. No entanto, as principais formas de resistência aos carbapenêmicos é a expressão de metalo-b-lactamases (MBL) e de oxacilina-ses (OXA).(17,18,19)
Este estudo mostrou que todas as cepas de A. baumannii foram resistentes aos carbapenêmicos testados e também ao ciprofloxacino. Ademais, 86,44% das cepas desta bactéria mostraram-se resistentes ao levofloxacino. Também mostraram altas taxas de resistência as cepas expostas às cefalosporinas de 3ª e 4ª gerações, ceftazidima e cefepime, respectivamente. As cepas expostas aos aminoglicosídeos apresentaram altas taxas de resistência, por volta de 80%.Piperacilina + tazobactam e sulfametoxazol + trimetropim, da mesma forma, não se mostraram eficazes, com resistência bacteriana próxima de 90%. Pode-se notar que a associação de ampicilina + sulbactam testada em todas as cepas apresentou baixa resistência (22%), podendo ser considerada uma possível opção terapêutica de sucesso contra infecções traqueais causadas por esse patógeno.
Para P.aeruginosa, embora seja um bacilo Gram-negativo, não fermentador, de grande importância clínica em UTIs e também causador de PAV, este estudo mostrou alta prevalência, todavia com menores taxas de resistência aos antibióticos testados. Nos isolados de Pseudomonas aeruginosa, a maior resistência apresentada foi a ciprofloxacino, levofloxacino e gentamicina, (64,44%), seguidas de piperacilina + tazobactam 46,66%, e 42,22% de resistência a ceftazidima. Em relação aos carbapenêmicos, 40% foram resistentes ao meropenem e 37,77% ao imipenem. Ceftriaxona, 31,11% e amicacina, 28,88%.
Outros autores encontraram resultados que corroboram com os achados do presente estudo. Os achados de Balkhy et al.(6) mostraram que, em 248 isolados, Acinetobacter sp. (n = 87, 35,1%), P. aeruginosa (n = 63, 25,4%) foram os mais prevalentes. Acinetobacter sp. tiveram cerca de 60%-89% de resistência a todos os antimicrobianos testados, incluindo carbapenêmicos (60%-71%) e P. aeruginosa teve cerca de 13%-31% de resistência a todos os antimicrobianos testados, incluindo carbapenêmicos (31%).(6) Em 2008, Rocha et al. identificaram em 62 PAV um organismo, e em 16 dois diferentes patógenos, sendo que P. aeruginosa (29 casos, 29,0%), Staphylococcus aureus (28 casos, 28,0%), grupo Klebsiella-Enterobacter-Serratia (19 casos, 19,0%) e Acinetobacter sp. (18 casos, 18,0%) foram as principais causadoras de PAV, corroborando com os dados encontrados no presente estudo.(12) Um estudo feito por Souza et al.(13) detectou a presença de Acinetobacter baumannii, Klebsiella pneumoniae e Pseudomonas aeruginosa na cavidade bucal de pacientes em VM. Esse resultado confirma que os pacientes na UTI podem apresentar um nível significativo de patógenos respiratórios em sua microbiota, sendo A. baumannii a espécie bacteriana mais frequentemente isolada (30,77%) nas culturas de secreção traqueal de pacientes com PAV.(13)
Esses resultados são condizentes com os estudos expostos em relação à prevalência dos micro-organismos causadores de PAV, como o estudo feito por Guimarães e Rocco,(15) no qual foram avaliados 278 pacientes sob VM, mostrando que 38,1% dos pacientes desenvolveram PAV e os germes mais isolados foram P. aeruginosa (22%), Acinetobacter sp. (14%) e Staphylococcus aureus resistentes à meticilina (MRSA) (11%), e outros 46 pacientes apresentaram infecção por germes multirresistentes (43,4%).(15) No estudo de Ahmed,(7) os agentes bacterianos mais comumente isolados foram Pseudomonas aeruginosa (26%), Acinetobacter (26%), Klebsiella pneumoniae (26%) também com perfis de multirresistência.(7) Esse resultado foi igualmente observado em Phu et al.,(1) corroborando com os achados deste estudo.
CONCLUSÕES
- baumannii foi o patógeno mais comumente associado à PAV, além de apresentar altas taxas de resistência aos antimicrobianos utilizados na terapia. A frequência de PAVs causadas por Acinetobacter sp. e Pseudomonas sp. é alta e o rápido desenvolvimento de resistência destes micro-organismos é um dos mais graves entraves de saúde pública em todo o mundo. Além destas, foram obtidas 25 cepas de Staphylococcus aureus, oito de Candida albicans, oito de Serratia sp., sete de Acinetobacter sp., sete de Proteus mirabilis, sete de Enterobacter cloacae, seis de Escherichia coli, cinco de SCN,cinco de Streptococcus pneumoniae, cinco de Stenotrophomonas sp., quatro de Klebsiella aerogenes, duas de Providencia sp., uma de Klebsiella oxytoca, uma de Klebsiella ozaenae, uma de Morganella morgani, uma de Proteus sp., uma de Streptococcus sp.
Esses resultados enfatizam a importância da implementação de programas de vigilância de resistência bacteriana, da adoção de medidas de controle de infecção, do manejo da terapia empírica e do uso racional de antimicrobianos. Essas ações objetivam diminuir a pressão seletiva e evitar, ou, ao menos, desacelerar a disseminação desses micro-organismos resistentes, especialmente em infecções como a PAV, em que, geralmente, o diagnóstico etiológico preciso é difícil.
Abstract
Objective: The objective of this study is to evaluate the prevalence and antimicrobial susceptibility profile of strains of A. baumannii and P. aeruginosa isolated from tracheal lavage. Methods: This is a retrospective, cross-sectional, descriptive study where tracheal lavage culture results were collected from patients with VAP admitted to an adult ICU at a public hospital in the city of Juiz de Fora. Data were collected through the records of the Hospital Infection Control Service for the period from January to December 2018. Results: 469 tracheal lavage samples from adult patients admitted to the ICU were analyzed. Positive cultures were considered if ³106CFU / mL, totaling 242 (51.52%) of the tracheal lavage samples were positive; 55 (24.89%) strains of A. baumannii and 45 (18.98%) strains of P. aeruginosa were isolated. According to the CLSI 2018 criteria, A. Baumannii presented 100% of the strains resistant to meropenem, cefepime, ceftriaxone, ceftazidime and piperacillin-tazobactam. Conclusion: A. baumannii and P. aeruginosa are important agents of PAV. Furthermore, A. baumannii was the most commonly associated pathogen and presented multiresistance to the drugs tested, being considered as a public health issue.
Keywords
Pneumonia; mechanical ventication; Acinetobacter baumannii; Pseudomonas aeruginosa; drug resistance
REFERÊNCIAS
- Phu VD, Nadjm B, Duy NHA, Co DX, Mai NTH, Trinh DT, et al. Ventilator-associated respiratory infection in a resource-restricted setting: impact and etiology. J Intensive Care. 2017 Dec 19;5:69. doi: 10.1186/s40560-017-0266-4.
- Parisi M, Gerovasili V, Dimopoulos S, Kampisiouli E, Goga C, Perivolioti E, et al. Use of Ventilator Bundle and Staff Education to Decrease Ventilator-Associated Pneumonia in Intensive Care Patients. Crit Care Nurse. 2016;36(5):e1-e7. doi: 10.4037/ccn2016520.
- Thakuria B, SinghP, Agrawal S, AsthanaV. Profile of infective microorganisms causing ventilator-associated pneumonia: A clinical study from resource limited intensive care unit. J Anaesthesiol Clin Pharmacol. 2013;29(3):361-6. doi: 10.4103/0970-9185.117111.
- Chaudhury A, Rani AS, Kalawat U, Sumant S, Verma A, Venkataramana B. Antibiotic resistance & pathogen profile in ventilator-associated pneumonia in a tertiary care hospital in India. Indian J Med Res. 2016 Sep;144(3):440-446. doi: 10.4103/0971-5916.198679.
- Millot G, VoisinB, Loiez C, Wallet F, Nseir S. The next generation of rapid point-of-care testing identification tools for ventilator-associated pneumonia. Ann Transl Med. 2017;5(22):451. doi: 10.21037/atm.2017.11.05.
- Balkhy HH, El-Saed A, Maghraby R, Al-Dorzi HM, Khan R, Rishu AH, et al. Drug-resistant ventilator associated pneumonia in a tertiary care hospital in Saudi Arabia. Ann Thorac Med. 2014; 9(2):104-11. doi: 10.4103/1817-1737.128858.
- Ahmed NH, HussainT, Biswal I. Antimicrobial resistance of bacterial isolates from respiratory secretions of ventilated patients in amulti-specialty hospital. Avicenna J Med. 2015;5(3):74-8. doi: 10.4103/2231-0770.160233.
- Agência Nacional de Vigilância Sanitária (Anvisa). Microbiologia Clínica para o Controle de IRAS. Brasília: Anvisa, 2013.
- Oplustil CP, Zoccoli CM, Tobouti NR, Scheffer MC. Procedimentos Básicos em Microbiologia Clínica. 3a ed. São Paulo: Sarvier; 2010.
- Koneman. Diagnóstico Microbiológico. 8a ed. Rio de Janeiro: Guanabara-Koogan; 2018.
- Clinical and Laboratory Standards Institute. Performance Standards for Antimicrobial Susceptibility Testing; Twenty-ThirdInformational Supplement. CLSI document M100-S23. Wayne (PA): CLSI; 2018.
- Neto EC, Souza PC, Azevedo F, Lugarinho ME. Ventilator associated pneumonia: confection of a strategy of prophylaxis and management based on the analysis of epidemiology. Rev Bras Ter Intensiva. 2006 Dec;18(4):344-50. [Article in Portuguese]
- Moreira MR, Guimarães MP, Rodrigues AA, Gontijo Filho PP. Antimicrobial use, incidence, etiology and resistance patterns in bacteria causing ventilator-associated pneumonia in a clinical-surgical intensive care unit. Rev Soc Bras Med Trop. 2013;46(1):39-44. doi: 10.1590/0037-868216722013.
- Rodrigues PM, Carmo Neto ED, Santos LR, Knibe MF. Ventilator-associated pneumonia: epidemiology and impact on the clinical evolution of ICU patients. J Bras Pneumol. 2009 Nov;35(11):1084-91. [Article in English, Portuguese]. doi: 10.1590/s1806-37132009001100005.
- Guimarães MM, Rocco JR. Prevalence of ventilator-associated pneumonia in a university hospital and prognosis for the patients affected. J Bras Pneumol. 2006 Jul-Aug;32(4):339-46. [Article in English, Portuguese]
- Rocha Lde A, Vilela CA, Cezário RC, Almeida AB, Gontijo Filho P. Ventilator-associated pneumonia in an adult clinical-surgical intensive care unit of a Brazilian university hospital: incidence, risk factors, etiology, and antibiotic resistance. Braz J Infect Dis. 2008 Feb;12(1):80-5. doi: 10.1590/s1413-86702008000100017.
- Souza LCD, Mota VBRD, Carvalho AVDSZ, Corrêa RDGCF, Libério SA, Lopes FF. Association between pathogens from tracheal aspirate and oral biofilm of patients on mechanical ventilation. Braz Oral Res. 2017 Jun 5;31:e38. doi: 10.1590/1807-3107BOR-2017.vol31.0038
- Sader HS, Mendes RE, Gales AC, Jones RN, Pfaller MA, Zoccoli C, et al. Perfil de sensibilidade a antimicrobianos de bactérias isoladas do trato respiratório baixo de pacientes com pneumonia internados em hospitais brasileiros: resultados do Programa SENTRY,1997 e 1998. J. Pneumologia [Internet]. 2001 Mar; 27 (2:59-67. Available from: http://www.scielo.br/scielo.php? script=sci_arttext&pid=S0102-35862001000200002&lng=en. https://doi.org/10.1590/S0102-35862001000200002.
- Lima JLDC, Alves LR, Paz JNPD, Rabelo MA, Maciel MAV, Morais MMC. Analysis of biofilm production by clinical isolates of Pseudomonas aeruginosa from patients with ventilator-associated pneumonia. Rev Bras Ter Intensiva. 2017 Jul-Sep;29(3):310-316. doi: 10.5935/0103-507X.20170039. [Article in Portuguese, English].
- Martins AF, Barth AL. Acinetobacter multirresistente – um desafio para a saúde pública. Scientia Medica.2013;23(1):56-62.
- Royer S, Faria AL, Seki LM, Chagas TP, Campos PA, Batistão DW, et al. Spread of multidrug-resistant Acinetobacter baumannii and Pseudomonas aeruginosa clones in patients with ventilator-associated pneumonia in an adult intensive care unit at a university hospital. Baz J Infect Dis. 2015;19(4):350-7. doi: 10.1016/j.bjid.2015.03.009
- Gusatti Cde S, Ferreira AE, Fuentefria DB, Corçao G. Resistance to beta-lactams among Acinetobacter spp isolated from hospital sewage in southern Brazil. Rev Soc Bras Med Trop. 2009 Mar-Apr;42(2):183-7. [Article in Portuguese]. doi: 10.1590/s0037-86822009000200018.
- Puzniak L, DePestel DD, Srinivasan A, Ye G, Murray J, Merchant S, et al. A Combination Antibiogram Evaluation for Pseudomonas aeruginosa in Respiratory and Blood Sources from Intensive Care Unit (ICU) and Non-ICU Settings in U.S. Hospitals. Antimicrob Agents Chemother. 2019 Mar 27;63(4):e02564-18. doi: 10.1128/AAC.02564-18.
Correspondência
Patricia Guedes Garcia
Faculdade de Ciências Médicas e da Saúde de
Juiz de Fora – Suprema
Alameda Salvaterra, 200
36033-003 – Juiz de Fora-MG, Brasil
