Avaliação microbiológica da qualidade da água em bebedouros de uma instituição de ensino superior de Caxias do Sul-RS
Microbiological quality evaluation of drinking water fountains in a higher education institution of Caxias do Sul – RS
Daiane Soares Glowacki1
Liziane Bertotti Crippa2
1Acadêmica – Centro Universitário da Serra Gaúcha – Caxias do Sul-RS, Brasil.
2Professora – Centro Universitário da Serra Gaúcha – Caxias do Sul-RS, Brasil.
Instituição: Centro Universitário da Serra Gaúcha Brasil – Caxias do Sul-RS, Brasil.
Conflito de interesses: não há conflito de interesses.
Suporte financeiro: financiamento próprio + Empresa Engequímica, Assessoria, Projetos e Engenharia Química LTDA, Caxias do Sul-RS.
Recebido em 07/07/2018
Artigo aprovado em 27/06/2019
DOI: 10.21877/2448-3877.201900752
INTRODUÇÃO
Segundo a Organização Mundial da Saúde (OMS),(1) pelo menos dois bilhões de pessoas no mundo usufruem de uma fonte de água contaminada com fezes. Estima-se que a água potável contaminada ocasione 502 mil mortes diarreicas por ano. Para padronizar e regulamentar a qualidade da água, a OMS aponta diretrizes internacionais para serem usadas como base em todo o mundo, com a intenção de proporcionar a proteção da saúde pública.
A partir do século XIX, com os conhecimentos de Pasteur e Koch que deram origem à microbiologia, foi possível compreender como a transmissão de doenças infecciosas se processa e hoje é viável a identificação de microrganismos para confirmar a ação dos agentes biológicos, de sua presença na água e de seu papel na transmissão de doenças. Há dois mecanismos principais de transmissão de doenças por via hídrica: através de agentes biológicos patogênicos, como ingestão da água contaminada, e por meio da transmissão que ocorre pela insuficiência da quantidade de água, ocasionando uma higiene deficiente.(2)
Desta forma, é realizada análise de bactérias do grupo coliforme, que se localizam no trato intestinal dos animais de sangue quente e servem como parâmetro de contaminação da água por fezes. Além disso, estão presentes em baixa ocorrência no solo e na vegetação. A principal bactéria deste grupo é a E. coli, que apresenta tempos variáveis de sobrevivência no meio ambiente e pode causar graves problemas intestinais (E. coli 0157:H7).(3)
A portaria nº 2.914/2011 do Ministério da Saúde(4) determina que seja analisada na água disponível para consumo humano a ausência de coliformes totais e Escherichia coli em100mL de amostra e que seja determinada a contagem de bactérias heterotróficas. Esta portaria define que a contagem de bactérias heterotróficas deve ser realizada como um parâmetro para avaliar a integridade do sistema de distribuição (reservatório e rede), e recomenda não exceder a 500 unidades formadoras de colônia por 1 mL de amostra (500 UFC/mL).
A Pseudomonas aeruginosa é caracterizada pelo formato de bacilo, Gram-negativa, produtora de catalase e oxidase. São bactérias patógenas oportunistas, ou seja, causam doenças em pessoas que estão com o sistema imune debilitado, podendo resultar em uma sepse fatal.(5) Para isso, a Agência Nacional da Vigilância Sanitária(6) divulgou a resolução RDC nº 275/2005, que, ao analisar cinco unidades de amostras individualmente, determinou que só poderia haver um resultado positivo, não devendo exceder duas unidades formadora de colônia.
Sem a análise destes parâmetros microbiológicos, a verossimilhança de transmissão de doenças por via hídrica, como gastroenterites, se torna sobressalente, uma vez que a água constitui um elemento fundamental para a manutenção da vida.(7) Compreende-se a importância da água potável para o consumo humano, a qual, se não tratada, tem capacidade de propagar diversos contaminantes microbiológicos. Portanto, é valoroso saber se a água consumida está adequada aos padrões de potabilidade mencionados na legislação.(4)
Assim sendo, o propósito do presente trabalho foi avaliar a qualidade microbiológica da água disponível em bebedouros de uma instituição de ensino superior localizada em Caxias do Sul-RS.
MATERIAL E MÉTODOS
A instituição de ensino superior a ser estudada localiza-se na cidade de Caxias do Sul, Rio Grande do Sul e compreende um total de seis prédios nos quais estão matriculados alunos para vinte cursos de graduação como: administração, arquitetura e urbanismo, biomedicina, ciências contábeis, design, direito, educação física bacharelado, educação física licenciatura, enfermagem, engenharia de produção, engenharia civil, fisioterapia, nutrição, odontologia, psicologia e terapia ocupacional, engenharia ambiental, engenharia mecânica, engenharia elétrica e engenharia de computação, além de disponibilizar diversas especializações como MBAs, Pós-MBAs, extensões e projetos corporativos nas áreas de negócios, design, engenharia, direito, saúde e educação.
Foram analisadas duas amostras de cada um dos quatro bebedouros escolhidos nos prédios que apresentavam maior circulação de estudantes em períodos diferentes, início das aulas (março/2018) e metade do semestre (maio/2018).
Antes de começar a coleta do material para análise, foi realizada a desinfecção das torneiras dos bebedouros com álcool a 70º. Após a coleta de aproximadamente 150 mL de água, as amostras foram encaminhadas a um laboratório externo com certificado de reconhecimento ISSO/17025. Os frascos estéreis foram identificados de acordo com o número do prédio e a data da coleta. Para todas as amostras, foi adicionado 0,1 mL de um agente redutor, o Na2S2O3 – tiossulfato de sódio. O tiossulfato de sódio neutraliza o cloro residual presente na água e impede a continuação da ação bactericida durante o deslocamento da amostra.
Os métodos usados para bactérias heterotróficas, coliformes totais e Escherichia coli visam atender as especificações do Standard Methods for the Examination of Water and Wastewater, publicação da American Public Health Association (APHA), American Water Works Association (AWWA) e Water Environment Federation (WEF),(8) e para Pseudomonas aeruginosa o método utilizado é o Pseudalert da Idexx.(9)
Ao escolher o período de coleta das amostras, considerou-se a época em que as aulas haviam começado recentemente, visando a escassa circulação de estudantes e o período da metade do semestre, quando a circulação encontra-se frequente e intensa.
O método empregado para análise de coliformes totais e Escherichia coli denomina-se Presença-Ausência com substrato enzimático e consiste em uma reação enzima-substrato, resultando a liberação de uma substância cromogênica e fluorgênica com presença de cor amarela (coliformes totais) e fluorescência (Escherichia coli). A amostra deve ser analisada à temperatura ambiente, e após identificar-se um frasco estéril e transparente com o número da amostra medem-se 100 mL de amostra e vertem-se no frasco, adiciona-se o conteúdo de um flaconete de Colilert e homogeneíza-se o frasco com movimentos circulares até completa dissolução do reagente. Incubar em estufa a 35 ± 0,5ºC por 24-28 horas.(8) A leitura se faz conforme Tabela 1.
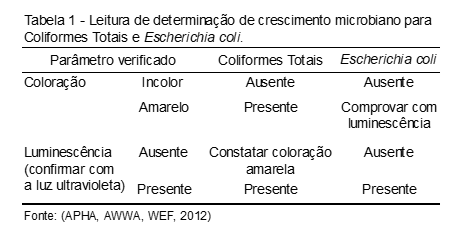
O método utilizado para análise de bactérias heterotróficas é o spread plate, por meio do espalhamento uniforme da solução, pois esta técnica facilita a contagem de bactérias na placa. A amostra deve ser analisada à temperatura ambiente. Separar duas placas de petri contendo ágar padrão para contagem a cada diluição. Na diluição homogeneíza-se a amostra 25 vezes por inversão e próximo ao bico de Bunsen pipeta-se 1 mL para um tubo estéril contendo 9 mL de água autoclavada. Homogeneizar o tubo em vórtex e continuar a diluição seriada até atingir a solução desejada. Para a inoculação, aproximar-se do bico de Bunsen e pipetar 100 uL da amostra no centro de cada placa. Espalhar a amostra movimentando o bastão (embebido em álcool a 96º e flambado) em círculos de dentro para fora da placa. Para cada análise, faz-se um branco, incubando uma placa sem amostra e um controle negativo. Incubam-se as placas invertidas em estufa monitorada a 35 ± 0,5ºC por 48 horas. Passado o tempo de incubação, conta-se o número de colônias presentes nas placas. A ausência de crescimento na placa de branco valida as análises.(8)
O método aplicado para análise de Pseudomonas aeruginosa nomeia-se Presença-Ausência com substrato enzimático e consiste em uma reação enzima-substrato. As cepas de Pseudomonas aeruginosa em crescimento têm uma enzima que cliva o substrato no reagente produzindo florescência azul sob luz ultravioleta. A amostra deve ser analisada à temperatura ambiente, e após identificar um frasco estéril e transparente com o número da amostra medem-se 100 mL de amostra e vertem-se no frasco, adiciona-se o conteúdo de um flaconete de Pseudalert e homogeneíza-se o frasco com movimentos circulares até completa dissolução do reagente. Incubar em estufa a 35 ± 0,5ºC por 24-28 horas. Qualquer fluorescência em azul indica que a amostra é positiva para Pseudomonas aeruginosa.(9)
RESULTADOS
Os resultados obtidos neste estudo foram comparados com a legislação brasileira vigente para água potável. As coletas foram efetuadas em duas etapas estruturadas nas Tabelas 2 e 3.
Na primeira coleta não foram identificados resultados fora do limite, porém, mesmo que dentro dos parâmetros permitidos e em pouca quantidade, a amostra número 4 apresentou contagens para bactérias heterotróficas com 4,5×10¹ UFC/mL. Nas quatro amostras não foram detectadas Pseudomonas aeruginosa e não foram constatadas presenças para coliformes totais e Escherichia coli (Tabela 2).
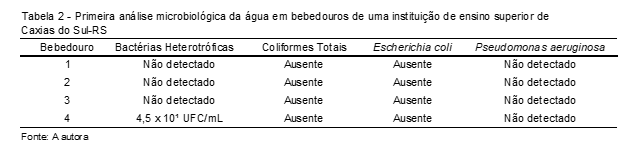
Na segunda etapa, a amostra número 3 revelou bactérias heterotróficas, sem exceder o limite (4,0×10² UFC/mL) e as outras três amostras exibiram contagens de bactérias heterotróficas acima do valor permitido por legislação, sendo a amostra 1 com 1,3×10³ UFC/mL, amostra 2 com 1,4×10³ UFC/mL e amostra 4 com 2,0×10³ UFC/mL; nesta coleta também não foi identificada a presença dos microrganismos Pseudomonas aeruginosa, coliformes totais e Escherichia coli (Tabela 3).
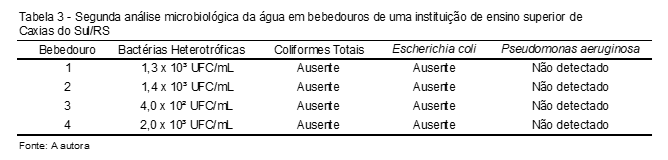
Portanto, a análise microbiológica da água dos bebedouros de uma instituição de ensino superior de Caxias do Sul apontou que das oito amostras coletadas, três delas mostraram-se alteradas conforme os padrões de potabilidade estabelecidos pela portaria 2914/2011 do Ministério da Saúde.
DISCUSSÃO
No estudo de Freitas et al.,(10) 90% das amostras tiveram crescimento de coliformes totais, apresentando um valor médio de 54 UFCs/cm², sendo considerado o valor de referência divulgado pela APHA de no máximo 50 UFC/cm². O estudo de Rocha et al.(11) apresentou grande quantidade de coliformes totais em dois bebedouros destinados ao uso dos alunos, tendo obtido presença em respectivamente 80% e 60% das amostras; já a análise de Escherichia coli apresentou resultados idênticos ao deste estudo, os quais mostraram-se negativos para a presença deste microrganismo.
Os resultados obtidos por Mello e Resende,(12) Castro et al.(13) e Seco et al.(14) corroboram com os resultados contidos neste estudo, onde 100% das amostras tiveram resultados negativos para coliformes totais e Escherichia coli.
Segundo a OMS,(15) o aumento da concentração de bactérias heterotróficas indica uma falha no tratamento da água, contaminação pós-tratamento, presença de depósitos, biofilmes ou corrosão na tubulação. Esses dados fortalecem um estudo que analisou a qualidade da água utilizada na desinfecção do úbere de animais, equipamentos e utensílios de ordenha em propriedades leiteiras, onde, em 51% das amostras, foram encontradas contagens de Escherichia coli, sugerindo descuido na manutenção das caixas d’água, considerando-as possíveis veículos de transmissão de doenças para os animais e até irregularidade na qualidade do leite.(16)
No estudo de Almeida et al.,(17) os resultados foram análogos a este estudo. Três de seis amostras excederam o máximo permitido para bactérias heterotróficas, ou seja, valores acima de 500 UFC/mL, e os autores explicam ainda que devido à falta de tratamento correto, esse fato conspira com a hipótese da influência inibidora que essas bactérias têm sobre outros organismos e sobre o grupo dos coliformes.
É de conhecimento que todos os bebedouros possuem um filtro de carvão ativado localizado em seu interior. Este tipo de filtro favorece a formação de biofilmes,(18) uma vez que ele retém o cloro presente na água, a proliferação de microrganismos se torna elevada, resultando em acúmulo de matéria orgânica depositada no filtro, correspondendo potencialmente à nutrição das bactérias heterotróficas.
Em um estudo realizado para analisar bactérias heterotróficas na água de um caminhão-pipa, foram coletadas amostras que apresentaram resultados relativamente semelhantes em dois horários de coleta, manhã e tarde, mas em ambas as contagens excederam o limite de 500 UFC/mL. Isso justifica o favorecimento da temperatura na multiplicação destes microrganismos e também a falta de manutenção e higiene; além disso, 90% das amostras apresentaram presença de coliformes totais, Escherichia coli e Pseudomonas aeruginosa em incompatibilidade com os padrões estabelecidos pela legislação.(19)
Quiroz(20) diz que a maioria das bactérias heterotróficas geralmente não são patogênicas, mas algumas têm sido responsáveis por infecções oportunistas (como Legionella spp., Micobacterium spp., Pseudomonas spp., Aeromonas spp.) em pacientes hospitalizados, sendo os de maior risco aqueles em uso de antibióticos e em imunodeprimidos.
Uma pesquisa feita por Reis et al.(21) mostrou quantidades aumentadas de contagens de bactérias heterotróficas em relação à primeira e segunda coletas realizadas em bebedouros de parques de Curitiba/PR, em conjunto com o estudo presente, atribuindo-se para esta multiplicação de microrganismos fatores como a limpeza inadequada do local e aumento do número de alunos que utilizam estes bebedouros, visto que na metade do semestre a circulação se torna mais frequente e intensa.
De acordo com a portaria 2914/2011 do Ministério da Saúde,(4) a qual menciona que a água potável deve ter ausência de coliformes totais e Escherichia coli em 100 mL de amostra, sendo que a presença da última é indicadora de contaminação fecal, é legítimo desconsiderar este tipo de contaminação nas amostras coletadas conforme dados da Tabela 2 e 3.
A resolução RDC nº 275/2005 da Agência Nacional da Vigilância Sanitária(6) menciona que, ao se analisarem cinco unidades de amostras individualmente, só poderá haver um resultado positivo, o qual não deve exceder duas unidades formadora de colônia. Este estudo apresentou ausência de Pseudomonas aeruginosa em todas as amostras, porém, no trabalho realizado por Santos e Colombo,(22) 21 amostras positivaram para Pseudomonas aeruginosa. Este resultado é extremamente preocupante, pois entende-se que existe a possibilidade de propagação de infecções atingindo principalmente pessoas imunocomprometidas.(5)
CONCLUSÃO
Esta pesquisa de parâmetros microbiológicos apresentou a presença exclusivamente de bactérias heterotróficas nas águas dos bebedouros. Segundo os resultados obtidos neste estudo e baseado nos padrões de potabilidade estabelecidos pela portaria vigente 2.914/2011 do Ministério da Saúde, das segundas amostras de água coletadas dos quatro bebedouros, ¾ apresentaram quantidades de bactérias heterotróficas superiores ao aceitável pela legislação, na qual se adverte que a contagem não exceda o limite de 500 UFC/mL; portanto, é possível compreender que a água destes bebedouros estava imprópria para o consumo humano.
Apesar dos resultados terem sido negativos para Pseudomonas aeruginosa, coliformes totais e Escherichia coli, que é o principal indicador da qualidade da água, é indispensável a necessidade constante de higienização, assim como a conservação, limpeza e manutenção da água e destes bebedouros para que sejam eliminados os microrganismos presentes.
Logo, as análises microbiológicas foram fundamentais para se averiguar a qualidade da água disponibilizada neste período para alunos, professores e funcionários desta instituição, tendo em mente que é neste ambiente que eles passam o maior tempo do seu dia.
Agradecimentos
À equipe da Empresa Engequímica, Assessoria, Projetos e Engenharia Química Ltda, Caxias do Sul-RS pelo suporte financeiro nesta pesquisa.
Abstract
Objective: To evaluate the microbiological quality of drinking water from drinking fountains intended for human consumption at a higher education institution in Caxias do Sul-RS. Methods: The method used for heterotrophic bacteria was spread plate and for total coliforms, Escherichia coli and Pseudomonas aeruginosa the method is absence or presence with enzyme-substrate. Eight samples were collected, each with approximately 150mL of water in sterilized bottles, after disinfection of the drinking nozzles with 70%. Results: In the first collection, the drinker 4 was the only one that presented alterations, with a presence of 4,5 x 10¹ of heterotrophic bacteria, however this level was in agreement with the quantity allowed. In the second sample, all samples were positive for heterotrophic bacteria, but the number 3 sample was within the limit accepted by the legislation, the others showed results higher than 500 CFU/mL. All Samples were negative for the analyzes of Pseudomonas aeruginosa, total coliforms and Escherichia coli. Conclusion: Although the results were negative for Pseudomonas aeruginosa, total coliforms and for Escherichia coli, three samples presented higher values than those accepted by Ministry of Health Ordinance 2914/2011 for heterotrophic bacteria. It is concluded that this water is considered inadequate for human consumption, based on the potability standards established by the aforementioned ordinance.
Keywords
Pseudomonas aeruginosa; Escherichia coli; heterotrophic bacteria; drinking water
REFERÊNCIAS
- World Health Organization (WHO). Drinking water. Geneva (SWI); 2018.
- Heller L, Pádua VL. Abastecimento de água para consumo humano. 2ª ed. Belo Horizonte: Editora UFMG, 2010.
- Libânio M. Fundamentos de qualidade e tratamento de água. 3ª ed. São Paulo: Editora Átomo, 2010.
- Ministério da Saúde (Brasil). Portaria no. 2.914, de 12 de dezembro de 2011. Dispõe sobre os procedimentos de controle e de vigilância da qualidade da água para consumo humano e seu padrão de potabilidade. Diário Oficial da União 16 dez 2011; seção 1.
- Sarangi PP. Biochemical characterization and antibiotic resistance of some medically important bacterial isolates. Rourkela. Dissertação [mestrado em Life Science] – National Institute of Technology; 2011.
- Agência Nacional de Vigilância Sanitária (Brasil). RDC no. 275, de 22 de setembro de 2005. Dispõe sobre Regulamento Técnico de Características Microbiológicas para Água Mineral Natural e Água Natural [resolução RDC na internet]. Diário Oficial da União 23 set 2005; seção 1.
- Matos, BA. Avaliação da ocorrência e do transporte de microrganismos no aquífero freático do cemitério de Vila Nova Cachoeirinha, município de São Paulo. São Paulo. Tese [Doutorado em Recursos Minerais e Hidrogeologia] – Universidade de São Paulo, Instituto de Geociências; 2001.
- APHA, AWWA, WEF. Standard Methods for the Examination of Water and Wastewater. 22. ed. Washington: American Public Health Association, 2012.
- Idexx. Pseudalert. Idexx Laboratories [Internet]. 2016 [acesso em: 12 jun 2018];33(05):7. Disponível em: https://idexxcom-live-b02da1e51e754c9cb292133b-9c56c33.aldryn-media.com/filer_public/e2/ff/e2fffda2-7443-4613-b8d2-fd0e48420b42/pseudalert-procedure-rev-en.pdf
- Freitas LL, Silva KC, Souza TM, Demarque ILD, Agostinho L, Fernandes F. Quantificação microbiológica de bebedouros de escolas públicas em Muriaé – MG. Revista Científica de Faminas. 2013 Fev; 9(1): 85-6.
- Rocha FAG, Bezerra JRG, Souza JAB, Bezerra LKMR, Pontes EDM, Araújo MFF. Padrão microbiológico de potabilidade da água destinada ao uso humano no IFRN, Câmpus Currais Novos. In: 7º Congresso Norte Nordeste de Pesquisa e Inovação [evento na internet]. 2012 19-21out; Palmas, Tocantins [acesso em 11 jun 2018]. Disponível em: http://propi.ifto.edu.br/ocs/index.php/connepi/vii/ paper/viewFile/1570/1601.
- Mello CN, Resende JCP. Análise microbiológica da água dos bebedouros da Pontifícia Universidade Católica de Minas Gerais campus Betim. Sinapse Múltipla. 2015 Jul; 4(1): 16-28.
- Fabri RL, Castro Ade S, Silva BM da. Avaliação da qualidade físico-química e microbiológica da água dos bebedouros de uma instituição de ensino superior de Juiz de Fora, Minas Gerais. Nutrir Gerais. 2013 Jul;7(12):984-98.
- Seco BMS, Burgos TN, Palayo JS. Avaliação bacteriológica das águas de bebedouros do campus da Universidade Estadual de Londrina – PR. Semina: Ciências Biológicas e da Saúde. 2012 Jul; 33(2): 193-200. doi: 10.5433/1679-0367.
- WHO. Safe piped water, managing microbial water quality in piped distribution systems. World Health Organization [Internet]. 2004 [acesso em: 12 jun 2018];6. Disponível em: http://apps.who.int/iris/bitstream/handle/10665/42785/924156251X.pdf?sequence=1&is Allowed=y.
- Piana SC, Piana SC, Fariña LO, Falconi FA, Busarello JJ. Avaliação da qualidade microbiológica da água de propriedades leiteiras dos municípios de Campo Bonito, Cascavel e Guaraniaçú – PR. Semina: Ciências Biológicas e da Saúde. 2014 Jan;35(1):25-34.doi: 10.5433/1679-0367.
- Almeida TM, Barros RO, Minãm DC, Viterbo DP, Conceição FPS, Silva CS, et al. Avaliação de conformidade dos parâmetros microbiológicos da água utilizada para irrigação, no Riacho do Cascão, Salvador – BA. Candombá. 2011 Jan;7(1):01-9.
- Daschner FD, Rüden H, Simon R, Clotten J. Microbiological contamination of drinking water in a commercial household water filter system. Eur J Clin Microbiol Infect Dis. 1996 Mar;15(3):233-7.
- Mendonça MHM, Roseno SAM, Cachoeira TRL, Silva AFS, Jácome PRLA, Júnior ATJ. Análise bacteriológica da água de consume comercializada por caminhões-pipa. Rev. Ambient. Água [Internet]. 2017 May;12(3):468-475. Available from: http://www.scielo.br/scielo. php? script=sci_arttext&pid=S1980-993X2017000300468& lng=en. doi.org/10.4136/ambi-agua.1934.
- Quiroz CC. Água embotellada y su calidad bacteriológica. Água Latinoamérica [Internet]. 2002 [acesso em: 12 jun 2018]; 38-9. Disponível em: http://www.bvsde.paho.org/bvsacd/cd56/agua.pdf.
- Reis F, Dias CR, Abrahão WM, Murakami FS. Avaliação da qualidade microbiológica de águas e superfícies de bebedouros de parques de Curitiba – PR. Visão Acadêmica. 2012 Jan;13(1): 64-7.
- Santos G, Colombo TE. Prevalência de Pseudomonas aeruginosa em águas e superfície. J Health Sci Inst. 2015;33(4):314-8.
Correspondência
Daiane Soares Glowacki
Rua Os Dezoito do Forte, 2366,
95020-472 – Caxias do Sul-RS, Brasil
