Associação incomum entre fenótipo e genótipo em dois pacientes com câncer hematológico
Unusual association between phenotype and genotype in two patients with hematological cancer
Tiago César Gouvêa Moreira1
Amanda Ribeiro de Oliveira1
Alice Muglia Tomaz da Silva Amancio2
Maurício Drummond Alves3
Luciana de Andrade Agostinho4
1Formação em Biomedicina pelo Centro Universitário Faminas (Unifaminas); Biomédico no Hospital do Câncer de Muriaé – Fundação Cristiano Varella (FCV). Muriaé-MG, Brasil.
2Formação em Ciências Biológicas pela Universidade Estadual do Norte Fluminense (UENF). Campos dos Goytacazes – RJ ; Doutora em Oncologia pela Fundação Antônio Prudente / Hospital A.C.Camargo. São Paulo-SP, Brasil.
3Formação em Medicina pela Universidade Federal do Rio de Janeiro (UFRJ); Residência em Pediatria; Residência Médica com Especialização em Hematologia e Hemoterapia; Médico no Hospital do Câncer de Muriaé- Fundação Cristiano Varella (FCV). Muriaé-MG, Brasil.
4Formação em Biomedicina pela Universidade de Vassouras. Vassouras – RJ; Doutora em Neurologia e Professora convidada do Programa de Pós-Graduação em Neurologia da Universidade Federal do Estado do Rio de Janeiro (UNIRIO).
Instituições:
1- Hospital do Câncer de Muriaé – Fundação Cristiano Varella – Muriaé-MG;
2- Centro Universitário Unifaminas – Muriaé-MG;
3- Programa de pós-graduação em Neurologia da Universidade Federal do Estado do Rio de Janeiro (UNIRIO). Rio de Janeiro-RJ. Brasil.
Recebido em 05/11/2020
Aprovado em 14/01/2021
DOI: 10.21877/2448-3877.202102032
INTRODUÇÃO
A leucemia é uma neoplasia maligna originada das células hematopoiéticas que se diferem de acordo com as células precursoras da medula óssea, tendo como principal característica o aumento de células imaturas no sangue periférico. Sua classificação é com base no tipo celular envolvido e no estado de maturidade das células leucêmicas, podendo ser, desta forma, linfoides ou mieloides, aguda ou crônica.(1) Estima-se, no biênio de 2018-2019, no Brasil, cerca de 5,75 e 4,56 novos casos de leucemia a cada 100 mil homens e mulheres, respectivamente.(2) Dentro da série mieloide, temos a leucemia mieloide crônica (LMC), doença que apresenta como principais sintomas, leucocitose, esplenomegalia e a presença do cromossomo Philadelphia (Ph), proveniente da translocação entre os cromossomos 9 e 22, que afeta diretamente as células tronco hematopoiéticas causando a sintomatologia da doença. Entretanto, o Ph não é restrito aos casos de LMC, pois também pode ser encontrado em alguns casos de leucemia linfoide aguda (LLA).(3) As síndromes mielodisplásicas (SMD) são doenças que se originam da série mieloide e possuem alta frequência entre os tipos de leucemias, apresentando uma taxa de incidência de quatro casos em 100 mil habitantes/ano, alcançando incidência de 40-50/100 mil habitantes/ano em pacientes com mais de 70 anos de idade.(4) Os principais sintomas apresentados pelos pacientes com SMD são sinais de insuficiência hematopoiética (principalmente anemia) e com menor frequência, sinais de sangramento e suscetibilidade às infecções. As SMD são caracterizadas por desordens de maturação e diferenciação no estroma da medula óssea (MO). Portanto, pacientes que apresentam esta doença, demonstram baixas contagens de células sanguíneas e risco elevado de desenvolver leucemia mieloide aguda (LMA).(5) Atualmente, uma pequena parcela dos pacientes diagnosticados com leucemias, apresentam sintomas ao diagnóstico e doença estabelecida. Entretanto, com o aumento do número de pacientes assintomáticos com suspeita clínica de leucemia após a realização de exames periódicos, faz-se necessário a confirmação da doença por outros exames, como a utilização dos exames moleculares e citogenéticos, exames também utilizados para monitoramento da doença durante o tratamento.(6) Devido à escassez de casos relatos sobre leucemias e achados moleculares e citogenéticos incomuns, justifica-se a realização do estudo. O objetivo deste estudo foi relatar dois casos de leucemia, com associação incomum entre o genótipo e fenótipo.
MATERIAL E MÉTODOS
Ambos os pacientes são provenientes do atendimento do setor de Hematologia do Hospital do Câncer de Muriaé-MG – Fundação Cristiano Varella (FCV). Este estudo se encontra aprovado pelo CEP da Faminas sob o número de CAAE: 61078416.5.0000.5105. Os dois indivíduos relatados neste estudo apresentam associação incomum entre genótipo e fenótipo em comparação com a literatura. Para diagnóstico do paciente com LMC utilizaram-se os critérios do Clinical Practice Guidelines da ESMO Guidelines Committee.(7) Para o diagnóstico do paciente com Síndrome Mielodisplásica, utilizaram-se os critérios da Myelodysplastic syndromes: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up da ESMO Guidelines Working Group.(8) Ambos os pacientes se enquadraram dentro dos critérios clínicos, citogenéticos e moleculares presentes em ambos Guidelines. Os dois pacientes foram orientados sobre os objetivos, confidencialidade dos dados, riscos e benefícios da pesquisa e após explicação assinaram o Termo de Consentimento Livre e Esclarecido (TCLE).
RELATO DOS CASOS
Caso clínico 1: Transcrito raro (e1a2) em paciente com Leucemia Mielóide Crônica
Paciente I.S.G, do sexo feminino, de 52 anos de idade, residente da cidade de Divino-MG, foi diagnosticada com LMC no Hospital do Câncer de Muriaé-MG (HCM) – Fundação Cristiano Varella (FCV), em maio de 2017. A paciente foi encaminhada para a FCV, pois há três meses, apresentava alterações no hemograma e dores abdominais. Os valores observados pela análise citológica e bioquímica do sangue fora da normalidade encontram-se descritos na Tabela 1. Apenas a contagem de neutrófilos, eosinófilos, monócitos e basófilos se encontravam dentro do valor de referência. Dentre os exames de bioquímica, foi observada alteração da proteína C reativa com 45,4 mg/L (Ref: < 5 mg/L).
Durante o exame clínico, com apalpamento da região abdominal, observou-se aumento do tamanho do baço em aproximadamente 18 cm do rebordo costal esquerdo (RCE) e do fígado em 7 cm do rebordo costal direito (RCD) atingindo a linha média, considerado quadro sugestivo de esplenomegalia e hepatomegalia. A paciente foi encaminhada para exames de imagem de ultrassonografia abdominal que confirmaram a suspeita (Figura 1A e 1B).
Após a realização dos exames bioquímicos e de imagem, foram administrados dois comprimidos de hidroxiureia 500 mg/dia (Hydrea®) durante 22 dias, com consequente diminuição da leucocitose e aumento da hemoglobina, hematócrito e plaquetas. Ao final do tratamento confirmou-se a presença de neoplasia mieloproliferativa, de acordo com os critérios do Clinical Practice Guidelines da ESMO.(7)
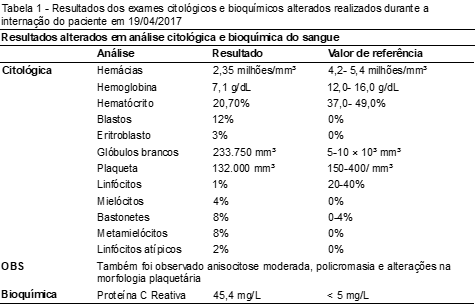
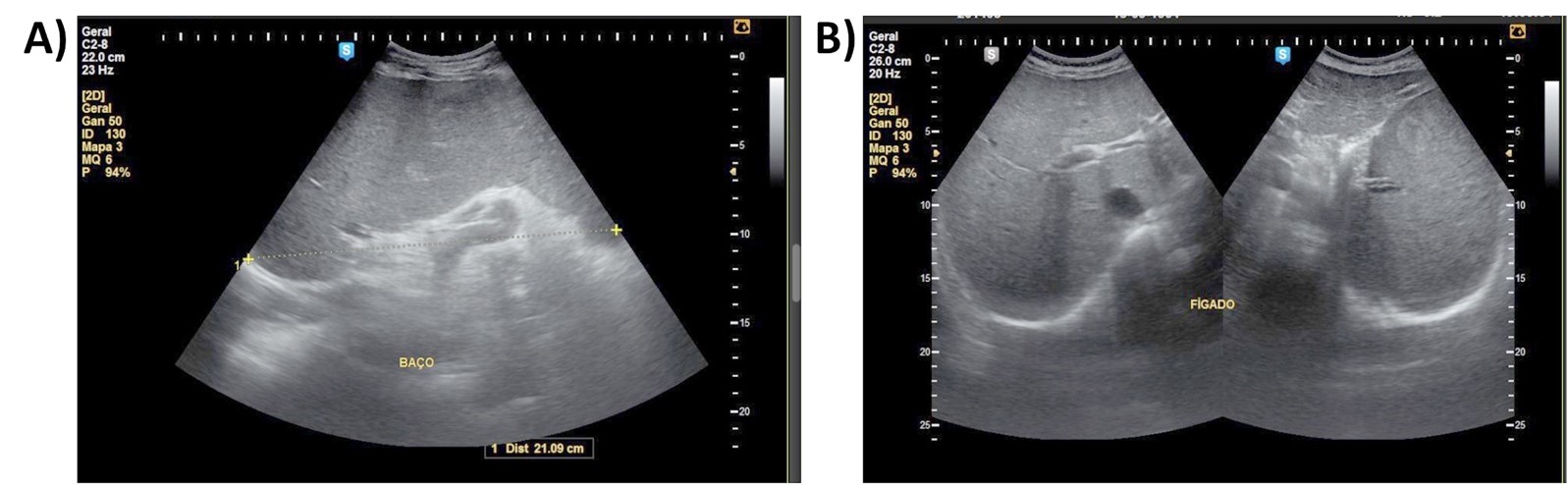
Figura 1. Ultrassonografia abdominal demonstrando esplenomegalia (A) e hepatomegalia (B).
O diagnóstico foi confirmado pela correlação dos achados citogenético, molecular e hematológico, principalmente com a identificação do Ph mediante resultado do cariótipo 46, XX, t(9; 22) (q34; q11.2) [20] (Figura 2) e presença da isoforma p190 no gene quimérico BRC/ABL por teste molecular, geralmente encontrado em pacientes com LLA.
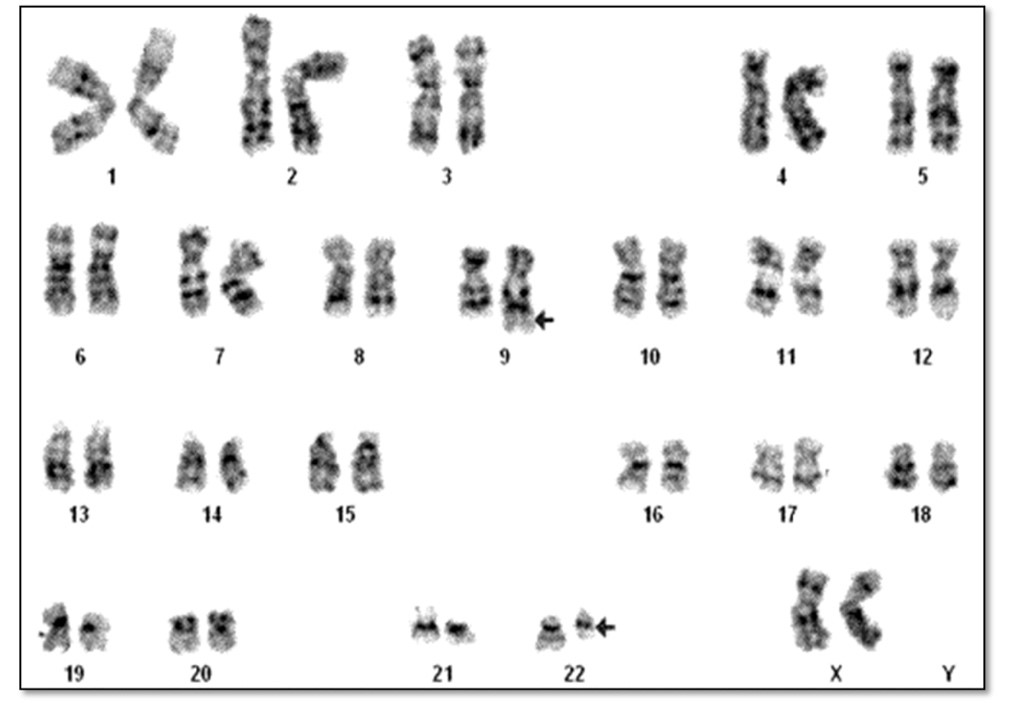 Figura 2. Resultado do cariótipo de medula da paciente I.S.G, demonstrando a translocação entre os cromossomos 9 e 22.
Figura 2. Resultado do cariótipo de medula da paciente I.S.G, demonstrando a translocação entre os cromossomos 9 e 22.
A confirmação do diagnóstico ocorreu em maio de 2017, quando foi iniciado o tratamento com Imatinibe® (400 mg/dia). Entretanto, não houve resposta hematológica completa após três meses de tratamento, devido à diminuição de plaquetas apresentada pelo paciente. Em agosto de 2017, a mesma retornou em consulta com médico hematologista na qual realizou-se a troca de medicação oral para Dasatinibe® 100 mg/dia. A paciente demonstrou excelente resposta hematológica ao medicamento e realiza retornos de 4 em 4 meses para reavaliar os efeitos clínicos da medicação.
Caso clínico 2: Translocação rara (11,17) (q23;q21) em paciente com Síndrome Mielodisplásica
Paciente A.P.M, do sexo masculino, 80 anos, residente da cidade de Laranjal-MG. Foi diagnosticado com mielodisplasia do tipo anemia refratária com excesso de blastos em transformação (AREB- 2) em janeiro/2017 e veio a óbito em março/2018. Em 2016, deu entrada no hospital com queixa de inapetência há15 dias, falta de ar após caminhar há sete dias, e quadro febril há três dias. Durante a primeira consulta, o médico hematologista levantou a suspeita clínica de leucemia mieloide aguda (LMA) baseado no resultado do mielograma, que apresentou blastos de morfologia linfoide compatíveis com leucemia aguda. Entretanto, exame posterior de imunofenotipagem da medula óssea apresentou porcentagem de blastos de 14% e grande quantidade de monócitos, alterando a suspeita clínica para síndrome mielodisplásica. Os valores observados pela análise citológica e bioquímica do sangue fora da normalidade encontram-se descritos na Tabela 2.
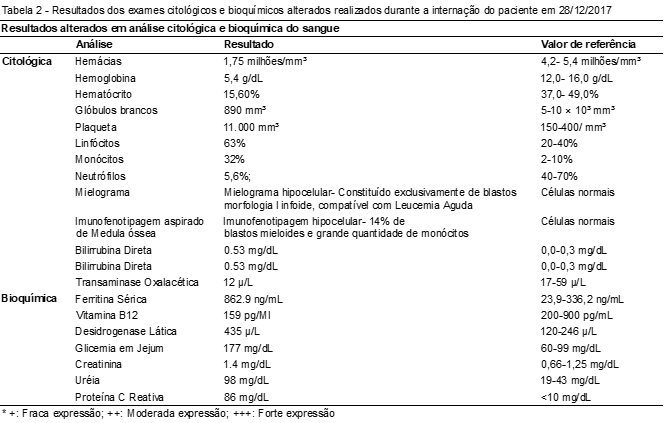
Após avaliação médica, o paciente realizou transfusão sanguínea e exames bioquímicos complementares. No exame de cariótipo, foi observada uma translocação rara em pacientes com SMD, entre os cromossomos 11 e 17: 46, XY, t(11;17) (q23;q21) [13]/ 46, XY [7] (Figura 3). Após a realização de todos os exames, determinou-se o diagnóstico de AREB-2 (CID 46.3) conforme os critérios da Myelodysplastic syndromes: ESMO Clinical Paractice Guidelines for diagnosis, treatment and follow-up da ESMO Guidelines Working Group.(8) Como tratamento, iniciou-se injeção subcutânea do quimioterápico Vidaza® (azacitidina) 150 mg/dia. Este medicamento é a primeira escolha para pacientes idosos (acima de 65 anos de idade) com SMD e que possuem alto risco de evolução da doença.(9)
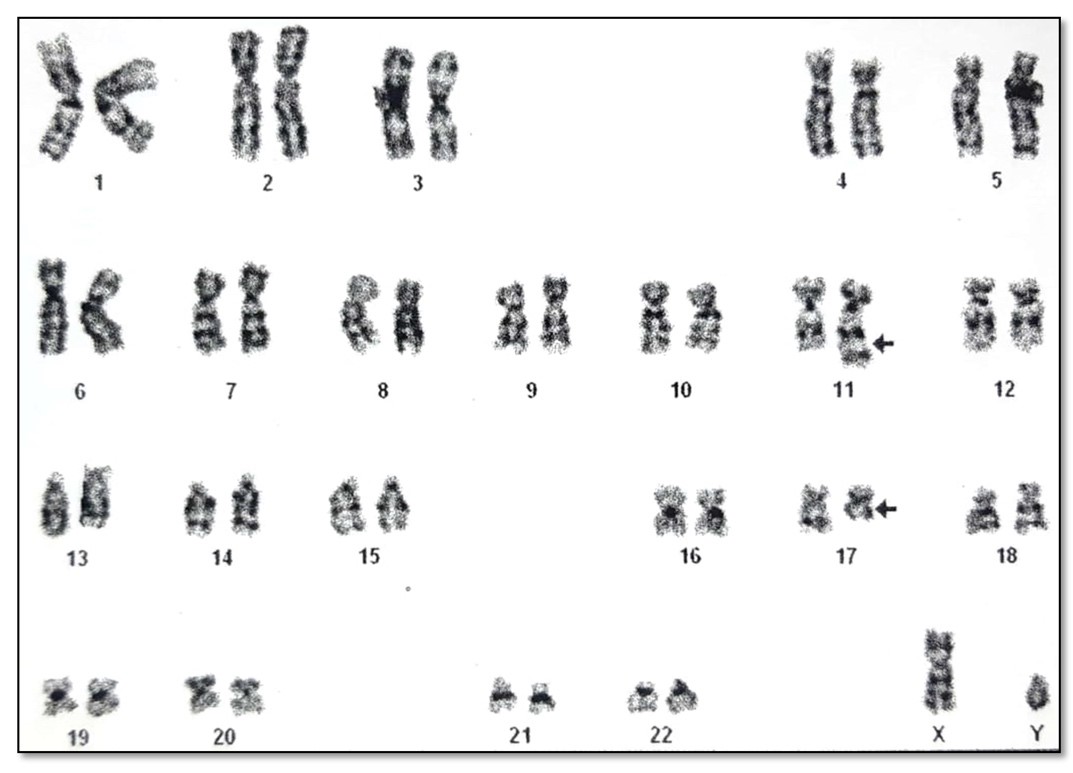
Figura 3. Resultado do cariótipo de medula do paciente A.P.M, demonstrando a translocação entre os cromossomos 11 e 17.
Ao concluir com o diagnóstico de SMD, foi avaliado o International Prognostic Score System (IPSS), escore que avalia a chance de progressão da doença e sobrevida do paciente. O escore determinado foi de 8 pontos, considerado alto de acordo com os padrões do IPSS, o que sugere prognóstico ruim e grandes chances de evolução da doença. Durante o tratamento, o paciente necessitou de várias transfusões de hemocomponentes, pois o mesmo retornava semanalmente com baixa de plaquetas. O paciente evoluiu para LMA após 13 meses de tratamento e veio à óbito após grande piora em seu quadro geral progredindo com um excesso de blastos presentes no sangue periférico, entre 70-90% (CID D463) (Figura 4).
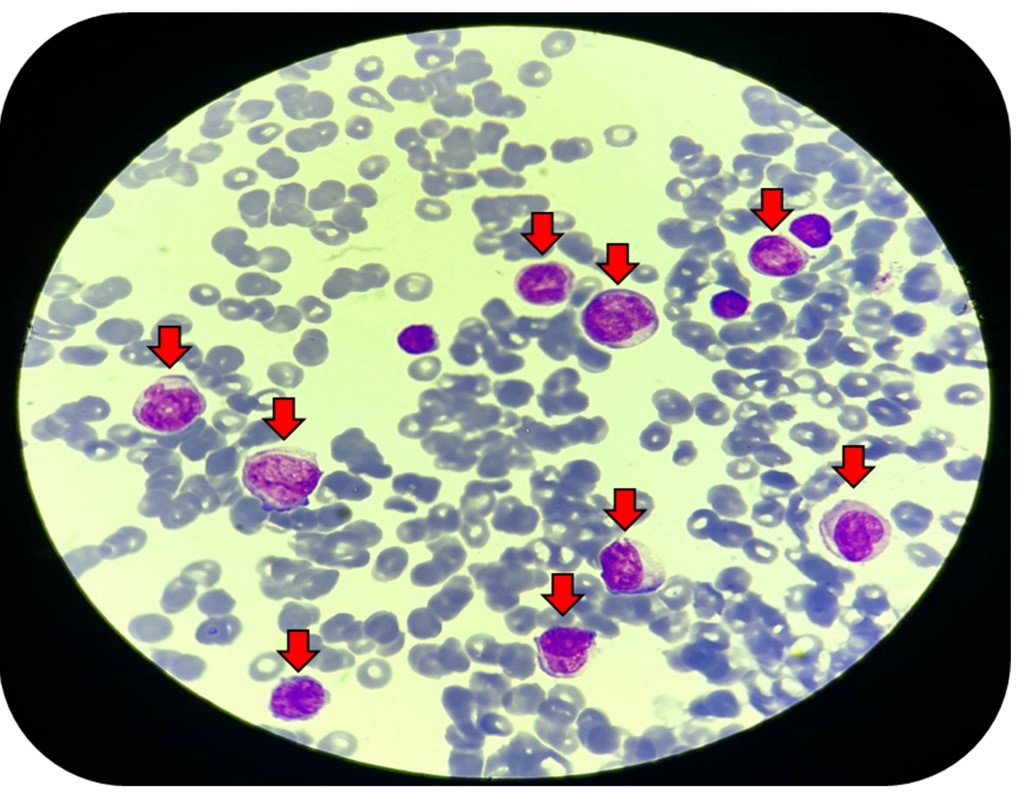
Figura 4. Campo da lâmina hematológica do sangue periférico do paciente A.P.M, vizualizado na objetiva de 100X. As setas demonstram blastos mieloides em excesso devido à evolução da doença para LMA.
Embora existam relatos de pacientes com LMA em literatura científica, não foi encontrado nenhum caso clínico descrevendo a translocação (11,17)(q23;21) em pacientes com SMD do tipo AREB2-t, até o momento da realização deste estudo em novembro de 2019. Durante leitura científica, foram encontrados quatro artigos que citaram a SMD: dois deles relataram que a quebra 11q23 (gene MML) está relacionada com SMD; outro descreve sobre as diferenças do diagnóstico em crianças com SMD e LMA com baixa contagem de blastos, e o último cita a evolução da SMD para LMA e fala sobre os tipos de SMD. Porém, nenhum estudo relata translocação (11,17) (q23;21) em pacientes com SMD do tipo AREB-2 identificada no presente estudo.
DISCUSSÃO
Caso clínico paciente 1: leucemia mieloide crônica com transcrito raro
O diagnóstico dos pacientes com LMC é simples, pois em sua grande maioria são utilizados os achados de hemograma e suas características diferenciais (granulocitose excessiva com desvio à esquerda). A confirmação do diagnóstico é realizada pela identificação do cromossomo Filadélfia (Ph) ou pelo resultado positivo das isoformas resultantes da fusão entre os genes BCR e ABL, ambos realizados pelo sangue periférico ou pelas células da medula óssea. Em cerca de 5% dos casos de LMC, o cromossomo Filadélfia não pode ser detectado pela análise de cariótipo. Assim, o diagnóstico definitivo depende da confirmação da fusão BCR/ABL, detectado pela reação em cadeia da polimerase com transcriptase reversa (RT-PCR).(7)
Dos pacientes com LMC, de acordo com Bollmann e Gligio, aproximadamente 90% são diagnosticados em fase crônica. Em relação aos exames bioquímicos, a proteína C reativa (PCR) foi o único parâmetro alterado deste caso, embora se acredite que a PCR seja um marcador de doenças agudas que pode sofrer interferência caso o paciente apresente processos crônicos.(10) Sendo assim, a PCR se mostra muito inespecífica para determinar um diagnóstico, mas é utilizada para estabelecer linha de base e monitorar a evolução de uma doença. Segundo Duarte e Marques, os portadores de LMC apresentam significante proliferação, aumentando exponencialmente a quantidade de células hematopoiéticas. Tal proliferação celular está associada à capacidade das mesmas de apresentarem maior sobrevida com acúmulo em locais como o baço, causando, por exemplo, a esplenomegalia.(11) Cançado e colaboradores citam que o medicamento Hydrea® pode ocasionar a regressão no tamanho e estabilização de danos no baço, resultando na melhora nos parâmetros do hemograma, em concordância com o observado na clínica do paciente neste presente estudo.(12) A formação do cromossomo Ph na LMC e LLA é resultante da translocação recíproca entre os cromossomos 9 e 22, dando origem ao gene quimérico BCR/ABL. Dependendo da região onde ocorrerem as quebras entre o cromossomo 9 e 22, o paciente apresentará diferentes transcritos e isoformas. Na LLA, há maior prevalência do transcrito do tipo e1a2, que dá origem à isoforma p190, e na LMC os transcritos b2a2 ou b3a2 são mais prevalentes, originando a isoforma p210.(13,14) A paciente apresentou o transcrito e1a2, alteração comumente encontrada em pacientes com LLA com prevalência de 1% em pacientes diagnosticados clinicamente com LMC.(15) Esta anomalia também está relacionada à baixa resposta terapêutica aos inibidores tirosino quinase (ITQ). Também está relacionada à progressão para fases blástica ou acelerada em 60% dos pacientes em fase crônica da doença.(14,15) Em pesquisa realizada por Dushyant Verma e colaboradores, foram analisados 1.292 pacientes com LMC, sendo que em somente 14 (1,1%) foram identificados apenas o transcrito e1a2, e nove destes se encontravam em fase crônica (FC), um em fase acelerada e quatro em fase blástica. Dos nove pacientes em FC, quatro demonstraram resposta hematológica completa, dois resposta citogenética completa e dois resposta citogenética parcial. Apenas um deles não respondeu ao Imatinibe, assim como nosso paciente 1 relatado neste caso. Os autores citam que pacientes com alterações raras possuem uma menor resposta ao Imatinibe®.(16) Tal fato foi observado na história clínica da paciente devido à troca do medicamento para o Dasatinibe, sendo este um ITQ de segunda geração. Outros estudos evidenciaram que, apesar do imatinibe® ter proporcionado uma melhora expressiva na evolução dos pacientes com LMC, surgiram mecanismos de resistência ou intolerância, nas quais os ITQ de segunda geração mostram eficácia.(3)
Caso clínico do paciente 2: Síndrome mielodisplásica com translocação rara
Em trabalho realizado por Garcia-Manero e colaboradores, foi proposto um score para segmentação dos pacientes de baixo risco de evolução da doença.(17) Os parâmetros que se associaram com pior sobrevida foram: plaquetopenia, anemia, idade avançada, níveis elevados de beta2-microglobulina e ferritina, excesso de blastos e alterações citogenéticas. Dentre estas alterações, apenas a beta2-mioglo-bulina não se encontrava alterada no paciente do presente estudo. Germing (2008) relata que a baixa contagem de células vermelhas do sangue e a evolução para LMA são um dos principais sintomas observados em pacientes com mielodisplasia por apresentarem desordem na maturação e diferenciação no estroma da MO.(5) Em 1997, foi proposto o International Prognostic Score System (IPSS) tendo como base de avaliação a SMD primária, e este sistema foi revisado posteriormente por Greenberg e colaboradores.(18) O escore avalia o risco sobre a transformação leucêmica e a sobrevida dos pacientes com SMD. Após avaliação do escore do IPSS, observou-se que o paciente apresentava prognóstico ruim e grandes chances de evolução da SMD para LMA, uma vez que escore <6 se associa com sobrevida média de oito meses e 25% destes pacientes evoluem em para LMA em uma média de sete meses após o diagnóstico e tratamento.(8) Em contrapartida, o paciente evoluiu para LMA após 13 meses de tratamento e veio à óbito após 15 meses de tratamento. Não foram encontrados artigos que relatam a translocação (11,17) (q23;21) em pacientes com SMD do tipo AREB-2. Entretanto, de acordo com Strehl e colaboradores, anormalidades estruturais na banda cromossômica 11q23 (gene MLL) são responsáveis por 5%-10% dos rearranjos adquiridos em crianças e adultos na LLA, LMA, SMD, entre outras.(19) A t(11,17)(q23;21) já foi relatada em outros tipos de leucemias e é encontrada frequentemente em pacientes com leucemia promielocítica (LPA), correspondendo a menos que 2% dos casos de LPA.(20) Já Rowley cita que a quebra 11q23 está relacionada com um desfecho clínico ruim.(21)
Em trabalho realizado por Bain e colaboradores em conjunto com a Association with karyotypic abnormalities, também relataram associação da quebra 11q23 com a SMD, embora menos comumente reconhecida, e descreveram as principais alterações citogenéticas envolvendo a região 11q23. Seu estudo avaliou 550 pacientes com SMD e evidenciou, em 28 pacientes (5,1%), o rearranjo cromossômico com o breakpoint 11q23. Entretanto, a translocação (11,17)(q23;21) não foi observada. Em contrapartida, a translocação t(11,17)(q23;q25) foi evidenciada em três pacientes com SMD, sendo dois deles diagnosticados com AREB.(22) Pode-se evidenciar que esta translocação é frequentemente relatada em pacientes que apresentam LLA e em pacientes com LMA, embora não relatada em pacientes com SMD do tipo AREB-2. A presença desta translocação incomum em pacientes com LMA pode ocorrer devido ao diagnóstico tardio de alguns pacientes que apresentam a translocação, ocorrendo a evolução de SMD para LMA. Cerca de 30% dos casos de SMD evoluem para LMA,(23) tendo consequentemente pior prognóstico e sobrevida. Existem algumas principais diferenças clinicas entre os pacientes diagnosticados com SMD e LMA, como a idade de início da doença, na qual os pacientes com SMD possuem início tardio (70 anos de idade) em comparação com os diagnosticados com LMA (45-65 anos de idade), a contagem de blastos na SMD é inferior aos 20%, já em pacientes com LMA é superior ou igual aos 20%.(24,25) O paciente foi diagnosticado como SMD do tipo AREB-2 de acordo com os critérios do Clinical Practice Guidelines da ESMO Guidelines Committee, que foram: a presença de citopenias, quantidade de blastos entre 5%-19% em sangue periférico, quantidade de monócitos <1×109/1. Também foi utilizada a correlação com outros exames, como o resultado do exame citogenético, imunofenotipagem, exames de imagem e bioquímicos.
CONCLUSÃO
Ambos os casos clínicos apresentados possuem relevância científica por se tratarem de dois casos incomuns, possuindo frequência de 1% entre os casos de LMC e por não se encontrar em literatura algum relato de caso de um paciente com SMD do tipo AREB-2 com a translocação t(11,17)(q23;q21). Os achados enfatizam a necessidade em se correlacionar a clínica apresentada pelo paciente com os exames obtidos como os hematológicos, citogenéticos e moleculares para a determinação fidedigna do diagnóstico e prognóstico dos pacientes, auxiliando os profissionais da hematologia a realizar conduta clínica adequada com o paciente.
Abstract
Description: Case report of a patient with a rare transcript (e1a2) in Chronic Myeloid Leukemia (CML) and another with a rare translocation in Myelodysplastic Syndrome (SMD). Discussion: The transcript e1a2 has a frequency of 1% in CML cases, whereas t (11,17) (q23; q21) translocation was not observed in a patient with type of Refractory Anemia with Excess Blasts (AREB) type 2. Conclusion: Both cases reported have unusual association between phenotype and genotype. The correlation of the clinic with the laboratory findings is important for the reliable determination of the diagnosis and prognosis of these patients.
Keywords
Leukemia; refractory anemia; genetic translocation
REFERÊNCIAS
- Instituto Nacional Do Câncer. Leucemia 2018 [Available from: https://www.inca.gov.br/tipos-de-cancer/leucemia.
- Instituto Nacional Do Câncer. Estimativa 2018: incidência de câncer no Brasil / Instituto Nacional de Câncer José Alencar Gomes da Silva. 2018.
- Bollmann PW, Giglio AD. Chronic myeloid leukemia: past, present, future. Einstein (Sao Paulo). 2011 Jun;9(2):236-43. [Article in English, Portuguese]. doi: 10.1590/S1679-45082011RB2022.
- Neukirchen J, Schoonen WM, Strupp C, Gattermann N, Aul C, Haas R,, et al. Incidence and prevalence of myelodysplastic syndromes: data from the Dusseldorf MDS-registry. Leuk Res. 2011 Dec; 35(12):1591-6. doi: 10.1016/j.leukres.2011.06.001.
- Germing U, Aul C, Niemeyer CM, Haas R, Bennett JM. Epidemiology, classification and prognosis of adults and children with myelodysplastic syndromes. Ann Hematol. 2008 Sep;87(9):691-9. doi: 10.1007/s00277-008-0499-3.
- Almeida A, Castro I, Coutinho J, Guerra L, Marques H, Pereira AM. Recommendations for diagnosis, treatment and monitoring of chronic myeloid leukemia. Acta Med Port. 2009 Sep-Oct;22(5):537-44. [Article in Portuguese]
- Hochhaus A, Saussele S, Rosti G, Mahon FX, Janssen J, Hjorth-Hansen H, et al; ESMO Guidelines Committee. Chronic myeloid leukaemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2017 Jul 1;28(suppl_4):iv41-iv51. doi: 10.1093/annonc/mdx219. Erratum in: Ann Oncol. 2018 Oct 1;29(Suppl 4):iv261.
- Fenaux P, Haase D, Sanz GF, Santini V, Buske C; ESMO Guidelines Working Group. Myelodysplastic syndromes: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2014 Sep;25 Suppl 3:iii57-69. doi: 10.1093/annonc/mdu180.
- Scott LJ. Azacitidine: A Review in Myelodysplastic Syndromes and Acute Myeloid Leukaemia. Drugs. 2016 May;76(8):889-900. doi: 10.1007/s40265-016-0585-0.
- Aguiar FJ, Ferreira-Júnior M, Sales MM, Cruz-Neto LM, Fonseca LA, Sumita NM, et al. C-reactive protein: clinical applications and proposals for a rational use. Rev Assoc Med Bras (1992). 2013 Jan-Feb;59(1):85-92. [Article in English, Portuguese]
- Duarte NL, Marques MAP. A Leucemia Mielóide Crônica e o uso do mesilato de Imatinibe em seu tratamento. Monografia apresentada como requisito para a conclusão do Curso Técnico de Nível Médio em Laboratório em Biodiagnóstico em Saúde. 2005. Fundação Oswaldo Cruz, Rio de Janeiro.
- Cançado RD, Lobo C, Ângulo IL, Araújo PIC, Jesus JA. Protocolo clínico e diretrizes terapêuticas para uso de hidroxiureia na doença falciforme. Rev. Bras. Hematol. Hemoter. [online]. 2009, vol.31, n.5, pp.361-366. https://doi.org/10.1590/S1516-848420090050000 76.
- Andrade GV. Papel da P190 BCR-ABL como parâmetro de recaída na leucemia mielóide crônica. Rev. Bras. Hematol. Hemoter. [online]. 2008, vol.30, n.4, pp.297-302. http://dx.doi.org/10.1590/S1516-84842008000400013.
- Bortolheiro TC, Chiattone CS. Leucemia Mielóide Crônica: história natural e classificação. Rev. Bras. Hematol. Hemoter. [online]. 2008, vol.30, suppl.1, pp.3-7.https://doi.org/10.1590/S1516-84842008000700003.
- Associação Brasileira de Hematologia e Hemoterapia, Sociedade Brasileira de Patologia, Sociedade Brasileira de Pediatria. Leucemia mieloide crônica [Chronic myeloid leukemia]. Rev Assoc Med Bras (1992). 2013 May-Jun;59(3):220-32. [Article in Portuguese]. doi: 10.1016/j.ramb.2012.08.003.
- Verma D, Kantarjian HM, Jones D, Luthra R, Borthakur G, Verstovsek S, et al. Chronic myeloid leukemia (CML) with P190 BCR-ABL: analysis of characteristics, outcomes, and prognostic significance. Blood. 2009 Sep 10;114(11):2232-5. doi: 10.1182/blood-2009-02-204693.
- Garcia-Manero G, Shan J, Faderl S, Cortes J, Ravandi F, Borthakur G, et al. A prognostic score for patients with lower risk myelodysplastic syndrome. Leukemia. 2008 Mar;22(3):538-43. doi: 10.1038/sj.leu.2405070.
- Greenberg PL, Tuechler H, Schanz J, Sanz G, Garcia-Manero G, Sole F, et al. Revised international prognostic scoring system for myelodysplastic syndromes. Blood. 2012 Sep 20;120(12):2454-65. doi: 10.1182/blood-2012-03-420489.
- Strehl S, Borkhardt A, Slany R, Fuchs UE, Konig M, Haas OA. The human LASP1 gene is fused to MLL in an acute myeloid leukemia with t(11;17)(q23;q21). Oncogene. 2003 Jan 9;22(1):157-60. doi: 10.1038/sj.onc.1206042.
- Sainty D, Liso V, Cantu-Rajnoldi A, Head D, Mozziconacci MJ, Arnoulet C, et al; Groupe Français d’Hématologie Cellulaire; Groupe Français de Cytogénétique Hématologique; UK Cancer Cytogenetics Group; BIOMED 1 European Community-Concerted Action “Molecular Cytogenetic Diagnosis in Haematological Malignancies”. A new morphologic classification system for acute promyelocytic leukemia distinguishes cases with underlying PLZF/RARA gene rearrangements. Blood. 2000;96(4):1287-96.
- Rowley JD. The role of chromosome translocations in leukemogenesis. Semin Hematol. 1999;36(4 Suppl 7):59-72.
- Bain BJ, Moorman AV, Johansson B, Mehta AB, Secker-Walker LM. Myelodysplastic syndromes associated with 11q23 abnormalities. European 11q23 Workshop participants. Leukemia. 1998 May;12(5):834-9. doi: 10.1038/sj.leu.2401020.
- da Silva-Coelho P, Kroeze LI, Yoshida K, Koorenhof-Scheele TN, Knops R, van de Locht LT, et al. Clonal evolution in myelodysplastic syndromes. Nat Commun. 2017 Apr 21;8:15099. doi: 10.1038/ncomms15099.
- Bernasconi P, Klersy C, Boni M, Cavigliano PM, Calatroni S, Giardini I, et al. World Health Organization classification in combination with cytogenetic markers improves the prognostic stratification of patients with de novo primary myelodysplastic syndromes. Br J Haematol. 2007 May;137(3):193-205. doi: 10.1111/j.1365-2141. 2007.06537.x
- Vassallo J, Magalhães SMM. Síndromes mielodisplásicas e mielodisplásicas/mieloproliferativas. Rev. Bras. Hematol. Hemoter. [online]. 2009, vol.31, n.4, pp.267-272. http://dx.doi.org/10.1590/S1516-84842009005000062.
Correspondência
Tiago César Gouvêa Moreira
Av. Cristiano Ferreira Varella, 555 – Universitário
36880-000 – Muriaé-MG, Brasil
