Análise integrada à biologia de sistemas para avaliação de citocinas pró-inflamatórias e anti-inflamatórias na infecção por Zika vírus
Analysis integrated with the systems biology pro-inflammatory and anti-inflammatory cytokine evalution in Zica Virus infection
Nelson Côrtes de Oliveira1
Irmtraut Araci Hoffmann Pfrimer2
1Pontifícia Universidade Católica de Goiás. Goiânia-GO, Brasil.
2Doutora. Pontifícia Universidade Católica de Goiás. Goiânia-GO, Brasil.
Instituição: Pontifícia Universidade Católica de Goiás. Goiânia-GO, Brasil.
Recebido em 22/05/2018
Artigo aprovado em 27/06/2019
DOI: 10.21877/2448-3877.201900708
INTRODUÇÃO
O vírus Zika (ZIKV) é um patógeno veiculado principalmente por mosquitos, tendo sido descoberto em 1947 em macacos “rhesus” na Floresta Zika de Uganda.(1) Pertence à família Flaviviridae que contém diversos vírus relacionados a enfermidades que acometem os seres humanos.(2)
Antes do grande surto que se iniciou no Nordeste brasileiro em 2015 sugestivo de uma interação entre a infecção por ZIKV com a microcefalia fetal e a síndrome de Guillain-Barré, o ZIKV não era considerado um patógeno humano relevante,(3,4) visto que anteriormente os casos de infecção por ZIKV relatados na África, Ásia e Oceania se restringiam a uma febre aguda.(5)
As pesquisas mostram que os vetores relacionados à transmissão do ZIKV são as espécies do gênero Aedes, principalmente o Aedes aegypti e Aedes albopictus.(6) Entretanto, foram descritas na literatura outras vias de transmissão de ZIKV, incluindo a transmissão sexual, perinatal, congênita e por transfusão sanguínea.(7,8) Segundo a atualização epidemiológica da Organização Pan-Americana da Saúde, cinco países das Américas já notificaram casos de transmissão sexual do ZIKV.(9)
Na maioria dos casos, a infecção humana por ZIKV é assintomática, cerca de 20% das pessoas infectadas manifestam algum sintoma,(10) com período de incubação estimado entre 3 a 14 dias.(11) Os sintomas apresentados são cefaleia, artralgia, mialgia, erupção cutânea, conjuntivite não purulenta e mal-estar, sendo estes comuns a outras arboviroses e de curta duração.(12)
Contudo, na Polinésia francesa e nas Américas têm-se relatado síndromes congênitas e condições neurológicas, como a microcefalia, síndrome de Guillain-Barré e encefalopatias associadas à infecção por ZIKV.(13,14) Até o momento, a transmissão autóctone vetorial da doença do ZIKV foi relatada em 48 países e territórios do continente americano desde 2015.(9)
Em virtude desta emergência, os estudos sobre ZIKV foram intensificados com o intuito de comprovar os mecanismos de transmissão e patogênese, encontrar testes diagnósticos precisos, evidenciar a relação etiológica das sequelas neurológicas com a infecção por ZIKV, para então desenvolver tratamentos eficazes e até mesmo métodos profiláticos.(15)
As citocinas são moléculas hidrossolúveis de composição glicoproteica ou polipeptídica extracelulares, de tamanho variável entre 8 e 30 kDa, responsáveis por influenciar a proliferação, diferenciação, atividade e sobrevida das células imunitárias, bem como regular a atividade e síntese de outras citocinas, que podem atenuar (anti-inflamatórias) ou aumentar (pró-inflamatórias) a resposta inflamatória. De modo que o equilíbrio entre essas duas classes de citocinas é fundamental na homeostasia e regulação do sistema imune.(16,17)
A Biologia de Sistemas visa organizar e armazenar os dados biológicos, de forma que são utilizados softwares, no intuito de realizar sondagem de dados, processamento de imagens, simulações computacionais e algoritmos, que dependem de fundamentos teóricos, teoria de sistemas, teoria da informação e da estatística.(18) O MATLAB é um destes softwares da Biologia de Sistemas voltado para o cálculo numérico, contendo em sua plataforma o gráfico “Box Plot” utilizado para avaliar a distribuição empírica dos dados.(19)
Por conta da expansão de casos notificados em diversos países, a infecção pelo ZIKV tem sido considerada uma doença endêmica e emergente.(20) Este trabalho objetivou, através da Biologia de Sistemas, verificar a produção de citocinas pró-inflamatórias (IL-1b, IL-2, IL-5, IL-6, IL-7, IL-9, IL-12p70, IL-15, IL-17A,RANTES, IL-8, TNFa, INF-Y, EOTAXINA e IP-10) e anti-inflamatórias(IL-4, IL-10, IL-13 e IL-1ra), em indivíduos infectados pelo ZIKV, pois a compreensão do padrão imunitário na infecção pode ser benéfico na monitorização do curso da doença e na avaliação da extensão da atividade inflamatória.
Material e Métodos
População de estudo
A pesquisa foi realizada no município de Goiânia, sendo incluídos indivíduos com idade igual ou superior a 18 anos e que apresentavam quadro clínico sintomatológico do ZIKV, e excluídos os que apresentavam comorbidades capazes de propiciar alterações na expressão das citocinas pesquisadas.
Portanto, a população de estudo foi composta por um banco de dados constituído de 176 indivíduos com suspeita de infecção pelo ZIKV, entre fevereiro e março de 2016, que tiveram suas amostras coletadas no Núcleo de Estudo e Pesquisas Imunológicas (NEPY), localizado na área V da Pontifícia Universidade Católica de Goiás, Goiânia, Goiás. Todas as amostras foram analisadas para o ZIKV por PCR em Tempo Real (RT-qPCR). O grupo controle, formado por doadores saudáveis, foi constituído a partir de 49 amostras selecionadas da Central Goiânia de Sorologia e Imunohematologia.
Foram coletados de cada paciente 10 mL de sangue com anticoagulante ácido etilenodiamino tetra-acético – EDTA. Após a coleta, o sangue foi centrifugado por cinco minutos a 2.500 rpm, e conduzido à capela de fluxo laminar para separação do plasma. Esse foi armazenado em freezer -80ºC e posteriormente utilizado para a extração do RNA viral e dosagem de citocinas.
Considerações Éticas
Os indivíduos dispostos a participar voluntariamente da pesquisa assinaram o Termo de Consentimento Livre e Esclarecido sob a prerrogativa do Comitê de Ética da PUC-Goiás pelo parecer CAAE: 57696716.9.0000.
Extração e detecção do RNA Viral
O RNA total foi obtido a partir do plasma dos pacientes, através do kit QIAamp®Viral RNA Mini (QIAGEN, Hilden, Alemanha). Todo o processo de extração ocorreu na capela de fluxo laminar, com todos os cuidados referentes à extração de RNA, como a utilização de microtubos, pipetadores e ponteiras RNase free.
O kit utilizado na detecção do RNA foi o Zika Vírus PCR (Bioclin®, Lote 004, MS: 10269360300, Registro Anvisa 10269360300), desenvolvido segundo as recomendações do CDC (Centers for Disease Control and Prevention, USA) e que apresenta como gene alvo de amplificação a poliproteína 5’ UTR. A detecção do RNA viral e do controle da extração nas amostras foi realizada pelo termociclador PCR Real Time (Light Cycler® 480 II, Roche). A curva padrão e a detecção do ZIKV foram obtidas pelo detector fluorescente FAM (465-510 nm), e o controle pelo VIC (533580 nm).
Quantificação e análise das citocinas
A quantificação de citocinas foi realizada na Fundação Oswaldo Cruz (Fiocruz) do Rio de Janeiro. As concentrações das citocinas foram determinadas no plasma dos pacientes por meio de um imunoensaio com microesferas do tipo multiplex. As amostras foram avaliadas para IL-1b, IL-2, IL-5, IL-6, IL-7, IL-9, IL-12p70, IL-15, IL-17A, IL-4, IL-10, IL-13 e IL-1ra, RANTES, IL-8, TNFa, INF-Y, Eotaxina e IP-10, usando um kit comercial (Lincoplex, Millipore, Missouri, USA) e um analisador Luminex (Luminex®, MiraiBio, Alameda, CA).
As citocinas foram analisadas e apresentadas com o uso da Biologia de Sistemas por meio da técnica de quartis aliado a um gráfico Box Plot gerado pelo software interativo de alta performance voltado para o cálculo numérico MATLAB.
Box Plot
A técnica do Box Plot trabalha com valores máximos (V.máx), medianas, 1º, 2º e 3º quartis e valores mínimos (V. A técnica do Box Plot trabalha com valores máximos (V.máx), medianas, 1º, 2º e 3º quartis e valores mínimos (V.mín). Os valores máximos e mínimos evidenciam o tamanho dos dados que serão trabalhados. A mediana se aplica em séries extensas, sendo a posição central dos dados ordenados de forma crescente ou decrescente, de maneira que demonstra a dispersão de um grupo de dados. Já os quartis são divididos em três conjuntos em que cada um tem 25% dos dados da série. O primeiro quartil (1º Q) está situado entre o (V.mín) e a mediana. O segundo quartil (2º Q) ou mediana define a posição central da série. Já o terceiro quartil (3º Q), está situado entre a mediana e o (V.máx). Os Outliers são valores distantes que compõem a séria, sendo representados pelo símbolo (+). A título de exemplo, segue abaixo uma representação de um Box Plot.(21)
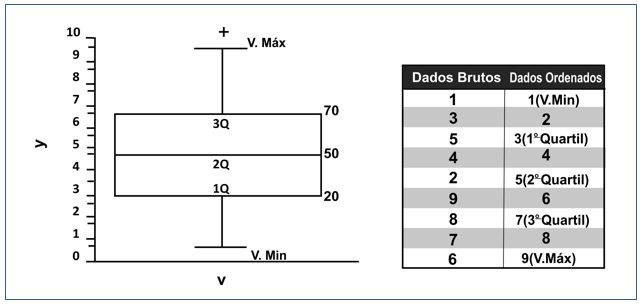
Figura 1. Representação Box Plot para um conjunto de dados arbitrários. Fonte: Galvani & Luchiari (2004).
Resultados
O estudo foi constituído por uma população de 176 indivíduos, 55 homens (31,2%) e 121 mulheres (68,8%), com idade média de 36 anos. Já o grupo controle foi formado por 49 indivíduos com idade média de 35 anos. As 176 amostras que apresentavam suspeita clínica de infecção pelo ZIKV foram submetidas a análise por RT-qPCR, sendo 36 positivas para o ZIKV. As amostras que apresentaram positividade foram colhidas principalmente no 2º dia de manifestação de sinais e sintomas. No entanto, tivemos uma amostra obtida no 15º dia que também foi positiva para o ZIKV.
Foram quantificadas 15 citocinas pró-inflamatórias e 4 anti-inflamatórias nas 36 amostras positivas para o ZIKV e nas do grupo controle.
Quando avaliados os níveis das citocinas pró-inflamatórias, observou-se um aumento de IL-7, IL-9, IL-17a, RANTES e IP-10 nos indivíduos infectados com o ZIKV. Já as citocinas IL-1b, IL-2, IL-5, IL-6 e IL-15, IL-12(P70), IL-8, TNF-a, INF-g e eotaxina não apresentaram resultados com diferenças significativas quando comparadas ao grupo controle. (Figuras 2 e 3).
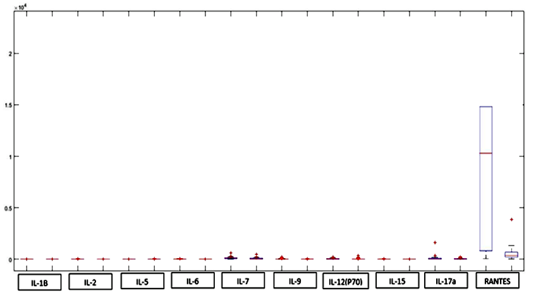
Figura 2. Perfil das citocinas pró-inflamatórias em em indivíduos infectados com o ZIKV e grupo controle. Boxplot (MATLAB).
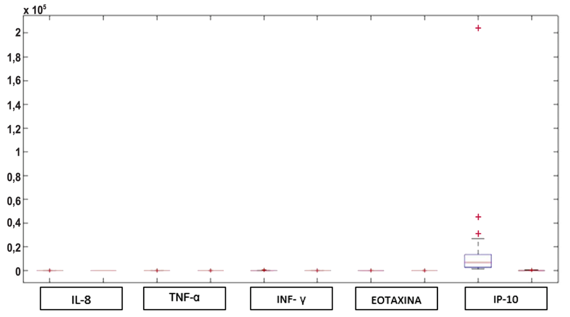
Figura 3. Perfil das citocinas pró-inflamatórias em indivíduos infectados com o ZIKV e grupo controle. Boxplot (MATLAB).
A síntese de IL-7, IL-9, IL-17a, RANTES e IP-10 estava aumentada nos indivíduos positivos para o ZIKV quando comparados aos pacientes do grupo controle. Sendo a citocina RANTES a que apresentou níveis mais elevados variando entre 1.313 a 14.839 pg/mL. (Figuras 4, 5, 6, 7 e 8).
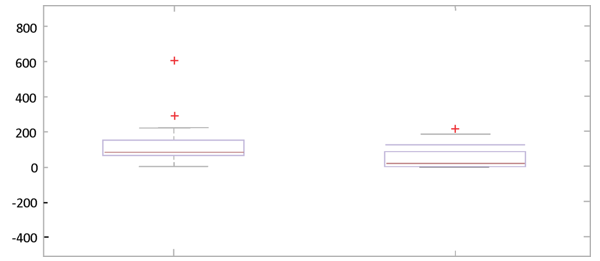
Figura 4. Análise de IL-7. Boxplot (MATLAB).
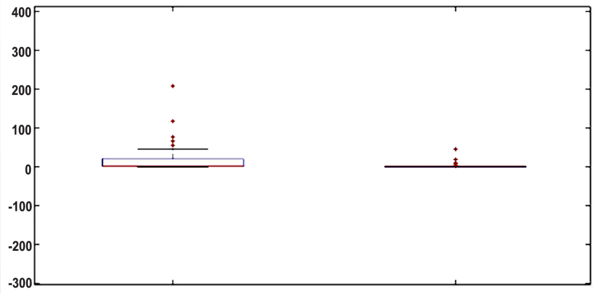
Figura 5. Análise de IL-9. Boxplot (MATLAB).
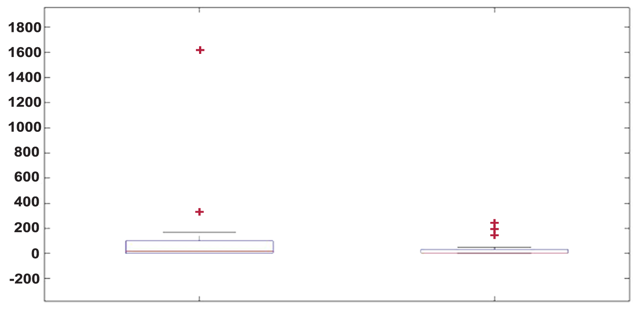
Figura 6. Análise de IL-17a. Boxplot (MATLAB).
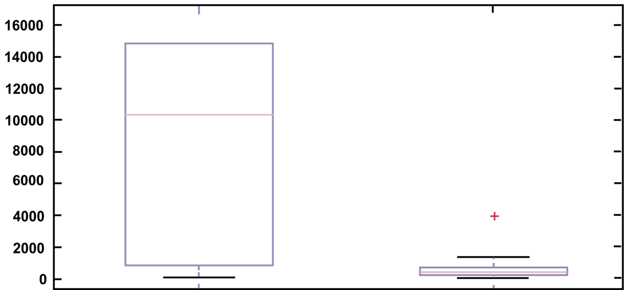
Figura 7 – Análise de RANTES. Boxplot (MATLAB).

Figura 8 – Análise de IP-10. Boxplot (MATLAB).
Na avaliação das citocinas anti-inflamatórias foi observado um perfil elevado da IL-1ra, enquanto que as demais não demostraram nenhuma alteração significativa quando comparadas aos controles. (Figura 9).
A IL-1ra, foi a que apresentou a diferença significativa mais marcante de todo o estudo com níveis que variaram entre 0,603 a 21,060 pg/mL no grupo controle, e 2,110 a 110,807 pg/mL nos indivíduos positivos para o ZIKV.
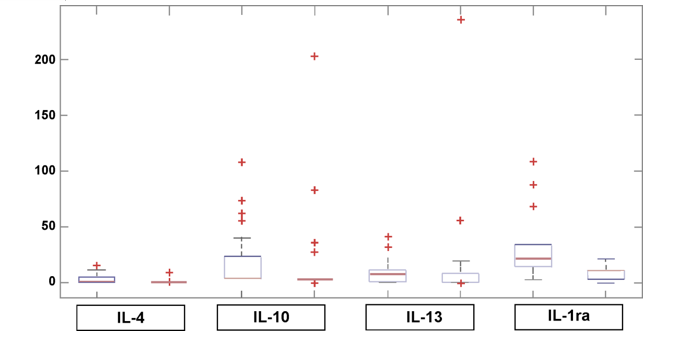
Figura 9 – Perfil das citocinas anti-inflamatórias em indivíduos infectados com o ZIKV e grupo controle. Boxplot (MATLAB).
Discussão
Estando de acordo com as diretrizes da European Centre for Disease Prevention and Control (ECDC, 2016),(22) que definem que para haver um diagnóstico molecular preciso, as amostras sanguíneas devem ser colhidas nos quatro primeiros dias da infecção. Em nosso estudo, as amostras positivas para o ZIKV foram colhidas principalmente no 2º dia de apresentação clínica da doença.
Entretanto, uma de nossas amostras foi positiva no plasma no 15º dia após as manifestações clínicas, sendo um episódio raro, que já foi observado por outros autores no soro e plasma. Como no estudo de Driggers et al.,(23) em que o RNA viral foi detectado no soro de uma gestante com indícios de infecção congênita aproximadamente dez semanas após o início dos sintomas, e no estudo de Mansuy et al.,(24) onde foi observada positividade no plasma até 37 dias após os sinais e sintomas clínicos da doença.
As citocinas são utilizadas em estudos clínicos pelo fato de atuarem como modificadores da resposta imune.(25) Em nossa pesquisa, os níveis das citocinas pró-inflamatórias IL-7, IL-9, IL-17a, RANTES e IP-10 dos indivíduos infectados pelo ZIKV na fase aguda, demonstraram-se elevadas. Essas citocinas estão relacionadas à atividade de linfócitos T e B, por isso, indicam uma possível proliferação desses tipos celulares mediante a infecção pelo ZIKV.(25)
A IL-7 é responsável por estimular a proliferação das células precursoras de linfócitos B e a maturação de megacariócitos, já a IL-9 por estimular a proliferação de células T CD4+, que por sua vez faz com que haja produção de IL-17a. Dados sobre as funções destas citocinas durante a infecção viral humana são escassos, mas demonstram a maturação e ativação das células imunitárias.(26)
Tappe et al.(27) realizaram um estudo semelhante relacionando diretamente às citocinas e à infecção pelo ZIKV em uma coorte, onde também foi demonstrado um aumento significativo de IL-9, IL-17, RANTES e IP-10.
A RANTES e IP-10 em concentrações elevadas sugerem um recrutamento efetivo de células T para sítios de infecção e formação de células T efetoras. Portanto, é necessária a realização de ensaios funcionais e de imunofenotipagem de células T do sangue periférico de pacientes infectados pelo ZIKV, a fim de contribuir para um melhor entendimento sobre o papel da RANTES e IP-10 durante a febre Zika.(28,29)
Estudos correlacionam os níveis de RANTES, que está armazenada em grânulos de plaquetas, com a trombocitopenia, nas infecções por vírus da Dengue, visto que esta é secretada por ativação plaquetária; assim, seria esperado que seus níveis diminuíssem por conta da trombocitopenia. Em contraste, a trombocitopenia grave é raramente observada em pacientes com febre Zika, e a RANTES não mostrou níveis reduzidos quando comparados ao grupo controle.(30)
Os resultados das citocinas anti-inflamatórias foram contrários aos achados de Tappe et al.,(27) visto que o receptor IL-1ra apresentou-se elevado. Contudo, o aumento de IL-1ra explica os baixos níveis de IL-1b, uma vez que b, bloqueando as respostas celulares e fisiológicas dessa citocina. Estudos publicados demonstram este fato, em que os níveis de IL-1b são indetectáveis porque o IL-1ra é um potente inibidor.(31,32) Barros et al.(33) avaliaram a produção de IL-1b por meio de culturas com diferentes Flavivírus, e não constataram nenhuma alteração em sua produção, mesmo diante da estimulação com lipopolissacarídeo bacteriano.
Constatamos que nas infecções pelo ZIKV, não ocorre uma grande liberação de citocinas, o que era esperado devido ao caráter benigno da doença. Diferente do que ocorre no quadro clínico da dengue, que também é um Flavivírus, em que a resposta imune é bastante expressiva.(27)
A realização de estudos biológicos por intermédio da Biologia de Sistemas é pertinente, em razão de que esta pode contribuir de forma a sumarizar e analisar dados quantitativos complexos.
Conclusão
No período de nosso estudo que ocorreu durante os meses de fevereiro a março de 2016, o ZIKV esteve circulante na cidade de Goiânia, e a infecção pelo vírus apresentou uma resposta imune pró e anti-inflamatória moderada na fase aguda, com elevação das citocinas IL-7, IL-9, IL-17a, RANTES, IP-10 e IL-1ra. Portanto, ocorre uma ativação da resposta imune celular e humoral mediada por células T e B no quadro clínico da febre Zika.
Apesar de os pacientes que foram incluídos no estudo apresentarem manifestações clínicas semelhantes à infecção pelo ZIKV, a viremia transitória impossibilitou a detecção do material genético viral e confirmação da doença na maioria deles.
Estudos futuros, por meio de citometria de fluxo e anticorpos monoclonais, são necessários a fim de demonstrar quais linhagens de linfócitos estão ativos na infecção do ZIKV, bem como abordar a resposta destes linfócitos e das citocinas com mais detalhes, incluindo na pesquisa um número maior de pacientes infectados pelo vírus Zika.
Abstract
Objective: The present study objected to analyze the pro and anti-inflammatory cytokines in patients infected with zika vírus. Methods: Through the Systems Biology that contributed in a way to summarize the complex quantitative data. Results: In our study, we observed elevation of the cytokines IL-7, IL-9, IL-17a, RANTES, IP-10 and IL-1ra of the infected individuals by ZIKV in the acute phase, related to T and B lymphocyte activity, which indicate a possible proliferation of these cell types through ZIKV infection. Conclusion: We found that in the infections by the ZIKV, does not occur a great release of cytokines, which was expected due to the benign nature of the disease.
Keywords
Zika virus; cytokines; systems biology
REFERÊNCIAS
- Dick GW, Kitchen SF, Haddow AJ. Zika virus. I. Isolations and serological specificity. Trans R Soc Trop Med Hyg. 1952 ;46(5):509-20.
- Gaunt MW, Sall AA, de Lamballerie X, Falconar AK, Dzhivanian TI, Gould EA. Phylogenetic relationships of flaviviruses correlate with their epidemiology, disease association and biogeography. J Gen Virol. 2001;82(Pt 8):1867-76.
- Ministério da Saúde do Brasil. Ministério da Saúde investiga aumento de casos de microcefalia em Pernambuco. Brasília: Ministério da Saúde, 2015. http://portalsaude.saude.gov.br/index.php/cidadao/principal/agenciasaude/20629ministerio-da-saude-investiga-aumento-de-casos-de-microcefaliaempernambuco. Acesso em: 24 de março de 2017.
- Pan American Health Organization (PAHO). Epidemiological Update: Neurological Syndrome, Congenital Malformations, and Zika Virus Infection.Washington:PAHO,2016.http://www.paho.org/hq/index.php?option=comdocman&task=docdownload&Itemid=&gid=32879&lang=em. Acesso em: 24 de março de 2017.
- World Health Organization (WHO). Zika Virus Fact Sheet. Geneva: WHO, 2016. http://www.who.int/mediacentre/factsheets/zika/en/. Acesso em: 25 de março de 2017.
- Grard G, Caron M, Mombo IM, Nkoghe D, Mboui Ondo S, Jiolle D, et al. Zika virus in Gabon (Central Africa)-2007: a new threat from Aedes albopictus? PLoS Negl Trop Dis. 8(2):e2681, 2014.
- Besnard M, Lastere S, Teissier A, Cao-Lormeau V, Musso D. Evidence of perinatal transmission of Zika virus, French Polynesia, December 2013 and February 2014. Euro Surveill. 2014;19(13). pii: 20751
- Hills SL, Russell K, Hennessey M, Williams C, Oster AM, Fischer M, et al. Transmission of Zika Virus Through Sexual Contact with Travelers to Areas of Ongoing Transmission-Continental United States. MMWR Morb Mortal Wkly Rep. 65(8):215-6, 2016.
- Organização Pan-Americana Da Saúde/Organização Mundial Da Saúde (OPAS/OMS). Zika Epidemiological Update – 9 de fevereiro de 2017. Washington, D.C.
- Musso D, Nhan T, Robin E, Roche C, Bierlaire D, Zisou K, et al. Potential for Zika virus transmission through blood transfusion demonstrated during an outbreak in French Polynesia, November 2013 to February 2014. Euro Surveill. 2014 ;19(14). pii: 20761. Erratum in Euro Surveill. 2014;19(15):pii/20771.
- Krow-Lucal ER, Biggerstaff BJ, Staples JE. Estimated Incubation Period for Zika Virus Disease. Emerg Infect Dis. 2017;23(5):841-845.
- Brasil P, Calvet GA, Siqueira AM, Wakimoto M, de Sequeira PC, Nobre A, et al. Zika Virus Outbreak in Rio de Janeiro, Brazil: Clinical Characterization, Epidemiological and Virological Aspects. PLoS Negl Trop Dis. 10(4):e0004636, 2016a.
- Brasil P, Sequeira PC, Freitas AD, Zogbi HE, Calvet GA, De Souza RV, et al. Guillain-Barré syndrome associated with Zika virus infection. Lancet. 387(10026):1482, 2016b.
- Thiery G, Valentino R, Meddhaoui H. Zika virus-associated Guillain-Barré syndrome: a warning for critical care physicians. Intensive Care Med. 2016 Sep;42(9):1485-6.
- Barzon L, Trevisan M, Sinigaglia A, Lavezzo E, Palù G. Zika virus: from pathogenesis to disease control. FEMS Microbiol Lett. 2016; 363(18). pii: fnw202.
- de Oliveira CM, Sakata RK, Issy AM, Gerola LR, Salomão R. Cytokines and pain. Rev Bras Anestesiol. 2011;61(2):255-9, 260-5, 137-42. [Article in English, Portuguese, Spanish]
- Kidd P. Th1/Th2 balance: the hypothesis, its limitations, and implications for health and disease. Altern Med Rev. 2003; 8(3):223-46.
- Hogeweg P. The roots of bioinformatics in theoretical biology. PLoS Comput Biol. 2011 Mar;7(3):e1002021.
- Mathworks. Disponível em: https://www.mathworks.com/products/matlab.html. Acesso em: 18 de janeiro de 2018.
- Faria NR, Azevedo ROS, Kraemer MU, Souza R, Cunha MS, Hill SC, et al. Zika virus in the Americas: Early epidemiological and genetic findings. Science. 352(6283):345-9, 2016.
- Galvani E, Luchiari A. Critérios para classificação de anos com regime pluviométrico normal, seco e úmido. Aracajú. VI Simpósio Brasileiro de Climatologia Geográfica, p. 20-29, 2004.
- European Centre For Disease Prevention And Control, ECDC. Interim guidance for healthcare providers and Zika virus laboratory diagnosis. Stockholm: ECDC, 2016.
- Driggers RW, Ho CY, Korhonen EM, Kuivanen S, Jääskeläinen AJ, Smura T, et al. Zika virus infection with prolonged maternal viremia and fetal brain abnormalities. N Engl J Med. 2016 Jun 2;374(22): 2142-51.
- Mansuy JM, Mengelle C, Pasquier C, Chapuy-Regaud S, Delobel P, Martin-Blondel G, et al. Zika virus infection and prolonged viremia in whole-blood specimens. Emerg Infect Dis. 2017 May;23(5):863-5.
- Varella PPV, Forte wcn. Citocinas: revisão. Rev. bras. alerg. imunolpatol. 2001;24(4):146-154.
- Shaikh PZ. Cytokines & their physiologic and pharmacologic functions in inflammation: A review. Int J of Pharm & Life Sci (IJPLS), Vol. 2, Issue 11: Nov.: 2011, 1247-1263
- Tappe D, Pérez-Girón JV, Zammarchi L, Rissland J, Ferreira DF, Jaenisch T, et al. Cytokine kinetics of Zika virus-infected patients from acute to reconvalescent phase. Med Microbiol Immunol. 2016 Jun;205(3):269-73.
- Pandey N, Jain A, Garg RK, Kumar R, Agrawal OP, Lakshmana Rao PV. Serum levels of IL-8, IFN g, IL-10, and TGFb and their gene expression levels in severe and non-severe cases of dengue virus infection. Arch Virol. 2015;160(6):1463-75.
- de-Oliveira-Pinto LM, Marinho CF, Povoa TF, de Azeredo EL, de Souza LA, Barbosa LD, et al. Regulation of inflammatory chemokine receptors on blood T cells associated to the circulating versus liver chemokines in dengue fever. PLoS One. 2012;7(7):e38527.
- Rathakrishnan A, Wang SM, Hu Y, Khan AM, Ponnampalavanar S, Lum LC, et al. Cytokine expression profile of dengue patients at different phases of illness. PLoS One. 2012;7(12):e52215.
- Zhang JM, An J. Cytokines, inflammation and pain. Int Anesthesiol Clin. 2007;45(2):27-37.
- Cianciarullo MA, Ceccon MEJ, Yamamoto L, Del Negro GMB, Okay TS. Mediadores pró-inflamatórios e antinflamatórios na sepse neonatal: associação entre homeostase e evolução clínica. Rev. bras. crescimento desenvolv. hum. [online]. 2008, vol.18, n.2 pp. 135-147. Disponível em: <http://pepsic.bvsalud.org/scielo.php?script =sci_arttext&pid=S0104-12822008000200004&lng =pt&nrm=iso>
- Barros VED, Ferreira BR, Livonesi M, Figueiredo LTM. Cytokine and nitric oxide production by mouse macrophages infected with Brazilian flaviviruses. Rev. Inst. Med. trop. S. Paulo [online]. 2009; 51(3): 141-147. Available from: http://www.scielo.br/scielo.php?script=sci_ arttext&pid=S0036-46652009000300004&lng=en.
Correspondência
Irmtraut Araci Hoffmann Pfrimer
Praça Universitária, 1440 – Setor Universitário
74605-010 – Goiânia-GO, Brasil
